Questão número 534785
Considere a mudança de estado de líquido saturado para vapor saturado de uma substância pura que obedece à seguinte relação termodinâmica
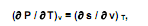
em que P, T, v e s denotam pressão, temperatura, volume específico e entropia específica, respectivamente.
Para estados termodinâmicos na região de saturação, a diferença de entalpia do vapor (hv) e do líquido (hl), representada por hlv = hv - hl, pode ser determinada a partir da inclinação ß = (d P / dT)sat da curva de pressão de vapor e da diferença dos volumes específicos vapor saturado - líquido vlv = vv - vl à temperatura dada. Marque a opção que fornece a expressão correta para o cálculo da diferença de entalpia vapor líquido saturado.
- A.
hlv = ß T vlv
- B.
hlv = ß 1/2 T vlv
- C.
hlv = (ß T) 1/2 vlv
- D.
hlv = (2 ß) 1/2 T vlv
- E.
hlv = 2 ß T vlv


