Questões de Engenharia Química
Lista completa de Questões de Engenharia Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
A reação química A + B 2 → P é elementar e irreversível. Se rP representa a taxa de formação de P, então

- A.
rP= kCP
- B.
rP= kCP2
- C.
rP= kCACB
- D.
rP= k(CP 2 - CACB)
- E.
rP= k(CACB- CP2)
Considere a reação química elementar e irreversível A→ 2 B. A molecularidade e a ordem da referida reação, respectivamente, são
- A.
1 e 1
- B.
1 e 2
- C.
2 e 0
- D.
2 e 1
- E.
2 e 2
Em uma indústria, um reator de mistura ideal com volume V opera em regime permanente ao processar a reação A → P, sendo a conversão de 0,8. Representando por (- rA) a taxa de consumo de A, sabe-se que (- rA) = k CA , onde k é a velocidade específica da reação e CA, a concentração de A em número de mols por litro. Se o referido reator for substituído por outro de volume 3 V que opere na mesma temperatura, com a mesma vazão e concentração de alimentação, a nova conversão será de
- A.
0,951
- B.
0,923
- C.
0,800
- D.
0,751
- E.
0,723
Analise as afirmações a seguir sobre parâmetros indicadores da qualidade das águas e controle de efluentes líquidos:
I - Os principais indicadores de contaminação fecal são os Coliformes Termotolerantes e Cianobactérias.
II - As principais formas de fósforo encontradas nas águas residuárias são os ortofosfatos, os polifosfatos, o fósforo orgânico e o fósforo tenso.
III - A quantidade de Nitrogênio Total dosada em uma amostra é proporcional à soma do Nitrogênio Kjeldahl Total e do Nitrito.
IV - A temperatura é um parâmetro controlado nas águas residuárias porque elas provocam elevações da temperatura do corpo receptor, ocasionando o aumento da solubilidade do oxigênio dissolvido e da taxa das reações químicas e biológicas.
V - A quantidade de Sólidos Totais contida em um efluente é constituída por Sólidos em Suspensão e Sólidos Dissolvidos, sendo as suas características físicas e físico-químicas classificadas em sólidos voláteis e fixos.
É(São) correta(s) APENAS a(s) afirmação(ões)
- A.
V.
- B.
II e IV.
- C.
III e IV.
- D.
I, II e V.
- E.
I, III e IV.
A reação 3 B → R ocorre em fase gasosa, em um reator tubular ideal que opera em regime permanente a temperatura e pressão constantes. O reator é alimentado com B puro na concentração de 660 mol/L e vazão de 600 L/h. Se a taxa de consumo de B é constante e igual a 33 mol L-1 min-1, o volume de reator, em L, necessário para que a concentração de B na saída seja igual 330 mol/L é
- A.
100
- B.
150
- C.
3.000
- D.
6.000
- E.
9.000
Em atendimento às legislações ambientais nacional e estadual vigentes, as indústrias devem tratar seus efluentes líquidos, processar e dispor os resíduos sólidos adequadamente e controlar as suas emissões gasosas. Nesse contexto, considere as afirmações a seguir.
I - As tecnologias que podem ser empregadas para minimizar riscos associados à mobilidade de resíduos sólidos perigosos, quando dispostos no meio ambiente, são: incineração, estabilização, destilação, solidificação e encapsulamento.
II - Os processos oxidativos avançados são processos baseados na geração de íons hidroxila altamente reativos, em decorrência do seu elevado potencial de oxidação.
III - Os sólidos suspensos coloidais podem ser removidos através dos processos de coagulação, floculação e sedimentação.
IV - As emissões atmosféricas contidas em um efluente gasoso são controladas por equipamentos específicos e, no caso da presença de material particulado, dependendo da sua granulometria, podem ser usados equipamentos como ciclone, filtro, precipitador eletrostático ou câmara de sedimentação.
Estão corretas as afirmações
- A.
I e II, apenas.
- B.
I e III, apenas.
- C.
III e IV, apenas.
- D.
I, II e III, apenas.
- E.
I, II, III e IV.
Uma indústria metal-mecânica produz cerca de 5.000 bocais de lâmpadas fluorescentes e incandescentes de um metal "Me". A camada superficial oxidada destas peças é removida por um processo de decapagem química, mergulhando- as durante 3min em um tanque contendo uma solução ácida com pH 3. Após tratamento de 20.000 peças, a solução fica contaminada com o metal dissolvido das peças (Me2+), ocorrendo a diminuição da eficiência do processo da decapagem. Neste estágio, o banho é enviado para um tanque, para a remoção do metal por precipitação como hidróxido, visando ao descarte do efluente.
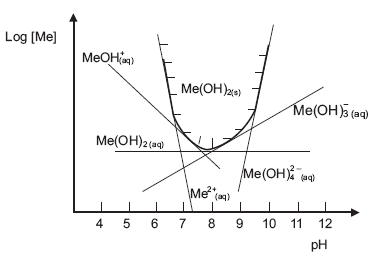
Analisando a figura acima, onde é mostrada a relação de equilíbrio das espécies dissolvidas complexadas do metal (Me) com o seu precipitado na forma de hidróxido, concluise que o metal "Me" pode ser removido por precipitação do seu hidróxido metálico, com uma maior eficiência, através do controle do pH em um valor próximo de
- A.
4
- B.
6
- C.
8
- D.
10
- E.
12
A mistura de hipoclorito de cálcio Ca(ClO)2 e cloreto de cálcio CaCl2 tem sido modernamente usada na desinfecção de reservatórios e esgotos. Com relação à química geral e inorgânica, julgue os itens que se seguem.
O íon cloreto é mais polarizável do que o íon brometo. Isso porque átomos de íons pequenos e leves tendem a ser altamente polarizáveis, uma vez que os orbitais de fronteiras estão muito próximos.
- C. Certo
- E. Errado
A mistura de hipoclorito de cálcio Ca(ClO)2 e cloreto de cálcio CaCl2 tem sido modernamente usada na desinfecção de reservatórios e esgotos. Com relação à química geral e inorgânica, julgue os itens que se seguem.
O estado de oxidação do cloro no Ca(ClO)2 é -2.
- C. Certo
- E. Errado
A mistura de hipoclorito de cálcio Ca(ClO)2 e cloreto de cálcio CaCl2 tem sido modernamente usada na desinfecção de reservatórios e esgotos. Com relação à química geral e inorgânica, julgue os itens que se seguem.
A água pode atuar como agente oxidante quando é reduzida a hidrogênio, mas a água também pode ser oxidada por outras espécies, tal como o Co 3+.
- C. Certo
- E. Errado


