Questões de Engenharia Química da Instituto O Barriga Verde (IOBV)
Lista completa de Questões de Engenharia Química da Instituto O Barriga Verde (IOBV) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
A água, a amônia e o metano têm massas moleculares próximas. Apesar disto, a água possui ponto de ebulição muito mais elevado que os da amônia e do metano. Essas observações experimentais podem ser explicadas porque:
- A. Os tipos de ligações não interferem no ponto de ebulição.
- B. Todos os três compostos apresentados têm ligações covalentes, porém o metano e amônia são polares.
- C. As moléculas de água têm as ligações covalentes oxigênio-hidrogênio facilmente rompíveis.
- D. A água possui moléculas polares que formam ligações de pontes de hidrogênio, aumentando a força de coesão entre as moléculas.
Num determinado tratamento de água, utilizou-se 0,355 mg de cloro (Cl2) por litro de água. O número de moléculas de cloro utilizadas por litro foi de:
- A. 3,01.1018
- B. 3,01.1019
- C. 6,02.1018
- D. 6,02.1023
Um solvente puro tem temperatura de ebulição(te) e temperatura de solidificação (ts). Acondicionando-se soluto não volátil ao solvente, as temperaturas de ebulição e solidificação para a solução serão (te) e (ts), respectivamente. É correto afirmar que:
- A. te < te e ts < ts
- B. te < te e ts > ts
- C. te > ts e ts > ts
- D. te > te e ts < ts
De acordo com a lei de Robert Boyle (1660), para proporcionar um aumento na pressão de uma determinada amostra gasosa numa transformação isotérmica, é necessário:
- A. Diminuir sua massa.
- B. Aumentar a sua temperatura.
- C. Diminuir o seu volume.
- D. Aumentar sua massa.
Uma solução aquosa 0,045 mol/L de ácido acético, CH3COOH, apresenta o ácido 2% dissociado em H+ e CH3COO-. A concentração de cada um desses íons na solução é:
- A. 9.10-4 mol/L
- B. 9.10-6 mol/L
- C. 9.10-2 mol/L
- D. 9.10-1 mol/L
O cloreto de carbonilo gasoso decompõe-se, à temperatura T, em monóxido de carbono e cloro molecular. Este sistema gasoso atinge um estado de equilíbrio, para o qual as espécies têm as seguintes concentrações:
[COCl2] = 1,60 mol/dm3
[CO] = 0,40 mol/dm3
[Cl2] = 0,40 mol/dm3
O valor da constante de equilíbrio é:
- A. 0,5
- B. 10
- C. 0,10
- D. 0,25
O grande volume de esgotos clandestinos lançados nos mananciais da Grande São Paulo é uma das causas das proliferações de algas microscópicas nocivas. Essas algas comprometem a qualidade da água. Concentrações de CO2 acima do limite de 2,5.10-3 mol/L aceleram o crescimento de alguns tipos de algas. Numa represa com 5.000 litros de água, assinale a alternativa correspondente à massa limite (em kg) de CO2 citada acima:
- A. 0,55
- B. 1,10
- C. 2,20
- D. 5,50
Assinale abaixo qual alternativa é incorreta acerca de um equilíbrio químico:
- A. Obrigatoriamente, as concentrações de todas as substâncias participantes do equilíbrio devem ser iguais.
- B. A velocidade da reação direta é igual à velocidade da reação inversa.
- C. Ambas as reações (direta e inversa) ocorrem simultaneamente (trata-se de um equilíbrio dinâmico).
- D. As características macroscópicas do sistema (desde que fechado) não mais se alteram.
A água potável proveniente de estações de tratamento resulta de um conjunto de procedimentos físicos e químicos que são aplicados na água para que esta fique em condições adequadas para o consumo. Esta separação é necessária uma vez que a água de rios ou lagoas apresenta muitos resíduos sólidos, por isso tem que passar por uma série de etapas para que esses resíduos sejam removidos. Neste processo de tratamento a água fica livre também de qualquer tipo de contaminação, evitando a transmissão de doenças. Em uma ETA (estação de tratamento de água) típica, a água passa pelas seguintes etapas: coagulação, floculação, decantação, filtração, desinfecção, fluoretação e correção de pH. Com relação às informações acima, analise as seguintes proposições:
I. Fluoretação: é quando se adiciona flúor na água, cuja finalidade é prevenir a formação de cárie dentária em crianças.
II. Floculação: ocorre em tanques de concreto, logo após a coagulação. Com a água em movimento, as partículas sólidas se aglutinam em flocos maiores.
III. Decantação: nesta etapa, que é posterior â coagulação e à floculação, por ação da gravidade, os flocos com as impurezas e partículas ficam depositados no fundo de outros tanques, separando-se da água. A etapa da decantação pode ser considerada um fenômeno físico.
IV. Filtração: é a etapa em que a água passa por filtros formados por carvão, areia e pedras de diversos tamanhos. Nesta etapa, as impurezas de tamanho pequeno ficam retidas no filtro. A etapa da filtração pode ser considerada um fenômeno químico.
V. Coagulação: é a etapa em que a água, na sua forma bruta, entra na ETA. Ela recebe, nos tanques, uma determinada quantidade de cloreto de sódio. Esta substância serve para aglomerar partículas sólidas que se encontram na água como, por exemplo, a argila.
VI. Desinfecção: é a etapa que cloro ou ozônio é aplicado na água para eliminar microorganismos causadores de doenças.
VII. Correção de pH: esse procedimento serve para corrigir o pH da água e preservar a rede de encanamentos de distribuição. Se a água está básica, é aplicada certa quantidade de cal hidratada ou carbonato de sódio.
Assinale a alternativa que contém somente proposições corretas:
- A. I, II, IV e V
- B. II, III, VII e VII
- C. III, V, VI e VII
- D. I, II, III e VI
A obtenção de água doce de boa qualidade está cada vez mais difícil devido ao adensamento populacional, às mudanças climáticas, à expansão da atividade industrial e à poluição. A água, uma vez captada, precisa ser purificada, o que é feito nas estações de tratamento. Um esquema de tratamento de purificação é:
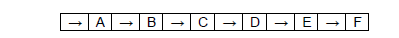
Onde as etapas B, D, e F são:
B adição de sulfato de alumínio e óxido de cálcio;
D filtração em areia;
F fluoretação.
Assim sendo, assinale a alternativa correta em que as etapas A, C e E correspondem respectivamente.
- A. Decantação, cloração e filtração grosseira.
- B. Cloração, neutralização e filtração grosseira.
- C. Filtração grosseira, decantação e cloração.
- D. Filtração grosseira, neutralização e decantação.


