Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Escola de Administração Fazendária (ESAF) - 2012

- A.
- 175 KJ
- B.
- 349 KJ
- C.
- 422 KJ
- D.
- 520 KJ
- E.
- 1040 KJ
Ao borbulhar um fluxo de CO2 numa água que possui elevada concentração de íons Ca+2, devido à dissolução prévia de CaO, um aluno de química experimental observou a formação de um precipitado branco, que é devido à formação da seguinte substância:
- A. CaCl2.
- B. CaCO3.
- C. CO
- D. Na2CO3.
- E. NaHCO3.

Dentre as estruturas apresentadas, aquelas em que todos os seus carbonos possuem o mesmo tipo de orbitais híbridos estão representadas pelas figuras
- A. I e II
- B. II e III
- C. III e IV
- D. I, II e III
- E. I, II e IV
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2012
Com relação ao controle e garantia da qualidade, julgue os itens que se seguem.
O chamado gráfico de farol é um instrumento simples para a verificação do controle de um processo produtivo. O nome do gráfico é devido ao fato de cada vez que o processo sai de controle acende um farol na fábrica e o observador assinala essa ocorrência no gráfico.
- C. Certo
- E. Errado
Utilizando uma corrente de 100 mA, a eletrodeposição de 1,0 g de níquel a partir de Ni2+ (aq), sobre uma bijuteria de aço inox levaria o tempo, em minutos, de
Dados: Massa molar do níquel = 58,7 g/mol Constante de Faraday = 9,65 × 104 C/mol- A.
233.
- B.
354.
- C.
487.
- D.
548.
Em relação à laminação a quente, a laminação a frio gera
- A.
maior ductilidade
- B.
melhor acabamento superficial
- C.
maiores reduções de espessura durante a laminação
- D.
maior equiaxialidade dos grãos
- E.
menor tensão de escoamento
Em relação às propriedades termodinâmicas e à espontaneidade das transformações, analise as assertivas a seguir.
I. Entalpia (H) é uma função de estado que mede a quantidade de calor absorvido ou liberado em qualquer transformação.
II. Entropia (S) é uma função de estado que mede o grau de desordem dos diferentes estados da matéria em uma transformação espontânea.
III. A variação de energia livre de Gibbs (ΔG) é uma medida da entropia total de um sistema, quando a temperatura e a pressão são constantes. As transformações espontâneas, nessas condições, são acompanhadas pelo aumento da energia livre.
IV. Sabendo que a variação de energia livre de Gibbs (ΔG) é dada pela expressão ΔG= ΔH TΔS, uma transformação exotérmica (ΔH<0) acompanhada pela diminuição da entropia (ΔS<0) não pode ser espontânea.
É(São) correta(s) apenas a(s) assertiva(s)
- A.
I.
- B.
II.
- C.
I e II.
- D.
II e III.
- E.
I, II e IV.
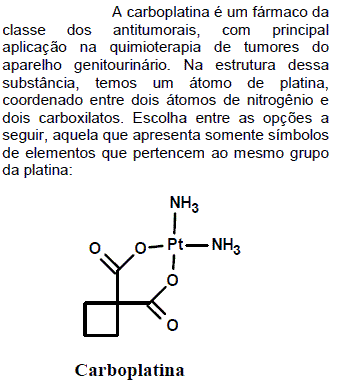
- A. Ni e Pd.
- B. Cl e Br.
- C. Na e Si.
- D. Cs e Sr.
- E. Au e Hg.
Acerca da previsão de séries temporais, julgue os seguintes itens.

- C. Certo
- E. Errado

- A.
chumbo e nitrato de chumbo (II).
- B.
cobre e cloreto de cobre (II).
- C.
magnésio e sulfato de magnésio.
- D.
estanho e sulfato de estanho (II).


