Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Considerando a mesma quantidade dos minerais abaixo, em mol, é esperado obter maior massa do metal ferro a partir de
- A.
limonita, Fe(OH)3 . nH2O.
- B.
pirita, FeS2.
- C.
magnetita, Fe3O4.
- D.
hematita, Fe2O3.
- E.
siderita, FeCO3.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
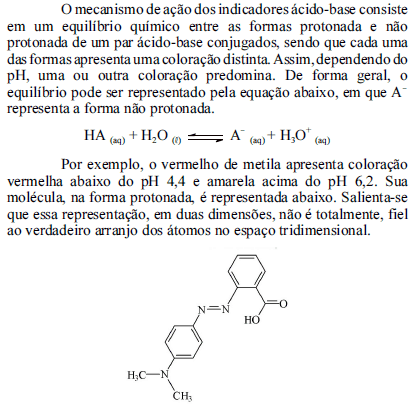
Tendo como referência as informações acima, julgue os itens conseguintes.
Infere-se que a forma protonada do vermelho de metila é a que apresenta coloração vermelha.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
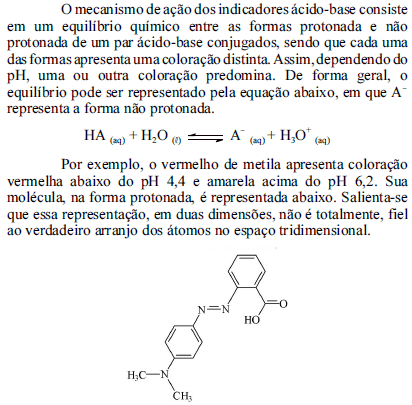
Tendo como referência as informações acima, julgue os itens conseguintes.
Na molécula do vermelho de metila, há dois átomos de nitrogênio com hibridização sp2, os quais se encontram em um mesmo plano em relação aos átomos de carbono dos anéis aromáticos.
- C. Certo
- E. Errado
O extrato de repolho-roxo é um excelente indicador de pH caseiro, muito fácil de utilizar em aula, que apresenta cores diferentes conforme a acidez (tendência ao vermelho) e a basicidade (tendência ao azul-esverdeado) do meio em que se encontra. Observe a tabela abaixo, que traz o resultado de uma experimentação.

Com base no texto e na tabela, está correto:
- A.
A ordem crescente de valores de pH das amostras acima é: detergente, saliva, água de torneira, chuva ácida e suco de limão.
- B.
A água de torneira tem, normalmente, pH neutro.
- C.
A saliva contém substâncias de caráter básico.
- D.
O suco de limão pode ser considerado um doador de prótons.
- E.
Os detergentes são formados de substâncias mais ácidas.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
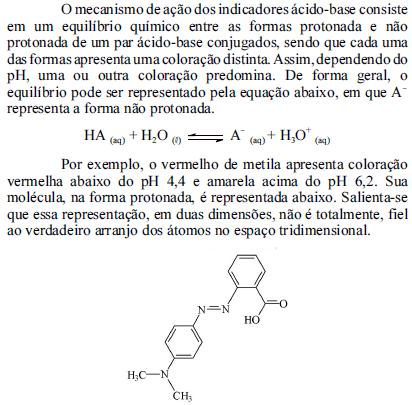
Tendo como referência as informações acima, julgue os itens conseguintes.
Na molécula do vermelho de metila, o átomo de nitrogênio que se encontra ligado a dois grupos metila apresenta geometria trigonal plana.
- C. Certo
- E. Errado
Em um sítio arqueológico, foram encontrados ossos de animais e um perito foi incumbido de fazer a datação das ossadas. Sabe-se que a quantidade de carbono 14, após a morte do animal, varia segundo a lei Q(t) = Q(0) e-0,00012t, em que e é a base do logaritmo natural, Q(0) é a quantidade de carbono 14 existente no corpo do animal no instante da morte e Q(t) é a quantidade de carbono 14 t anos depois da morte. Com base nessas informações e considerando -2,4 e 0,05 como valores aproximados de ln (0,09) e e-3, respectivamente, julgue os itens que se seguem.
Se, em uma ossada, o perito constatou que a quantidade de carbono 14 presente era 9% da quantidade no instante da morte do animal, então é correto afirmar que o animal morreu a menos de 19.000 anos.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
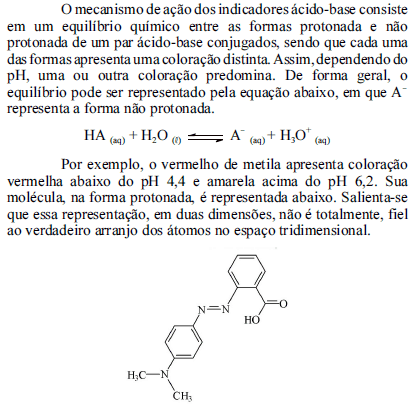
Tendo como referência as informações acima, julgue os itens conseguintes.
O vermelho de metila possui, em sua estrutura molecular, as funções amina e ácido carboxílico.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
Em um sítio arqueológico, foram encontrados ossos de animais e um perito foi incumbido de fazer a datação das ossadas. Sabe-se que a quantidade de carbono 14, após a morte do animal, varia segundo a lei Q(t) = Q(0) e-0,00012t, em que e é a base do logaritmo natural, Q(0) é a quantidade de carbono 14 existente no corpo do animal no instante da morte e Q(t) é a quantidade de carbono 14 t anos depois da morte. Com base nessas informações e considerando -2,4 e 0,05 como valores aproximados de ln (0,09) e e-3, respectivamente, julgue os itens que se seguem.
Suponha que, ao examinar uma ossada, o perito tenha verificado que o animal morreu há 25.000 anos. Nesse caso, a quantidade de carbono 14 existente nessa ossada, no instante do exame, era superior a 4% da quantidade no instante da morte.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011

Se os íons Ca 2+ forem precipitados, a partir de 2,0 L de uma solução com concentração de Ca2+ igual a 0,10 mol/L, pela adição de um grande excesso de CO32-, a quantidade de CaCO3 precipitada será superior a 18,0 g.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
Praticamente dois terços de nosso planeta são cobertos por água. Essa substância é também a mais abundante no organismo humano. Sendo a água tão comum, tem-se a tendência de considerar triviais suas propriedades químicas e físicas. Entretanto, ela possui muitas propriedades não usuais e essenciais à vida na Terra. Uma das propriedades mais importantes da água é a sua capacidade de dissolver uma grande variedade de substâncias. Por essa razão, a água é encontrada na natureza com um vasto número de substâncias nela dissolvidas. Como exemplo dessas substâncias, podem-se citar materiais radioativos, matérias orgânicas, coloides e metais pesados, entre outros.
Tendo o texto acima como referência inicial, julgue os itens a seguir, a respeito de aspectos diversos de química.
velocidade de decantação de uma suspensão aquosa será a mesma, independentemente de o sistema estar na superfície do planeta Terra ou na superfície da Lua.
- C. Certo
- E. Errado


