Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
Sabe-se que H2O2 / H2O, E0 = 1,77 V e que I2 / I-, E0 = 0,535 V. Então, atuará espontaneamente como agente oxidante a espécie
- A. I2
- B. H2O.
- C. I-
- D. H2O2.
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A extração líquido-líquido é um método de separação mais eficiente que a destilação,
I no caso de substâncias inorgânicas complexadas ou dissolvidas em soluções aquosas ou orgânicas.
II no caso da separação de mistura estar de acordo com o tipo químico e não com a volatilidade relativa.
III no caso de misturas que formam azeótropos.
- A.
Apenas um item está certo.
- B.
Apenas os itens I e II estão certos.
- C.
Apenas os itens I e III estão certos.
- D.
Apenas os itens II e III estão certos.
- E.
Todos os itens estão certos.
O processo de desenvolvimento de um fármaco inicia-se com a síntese e a determinação das características físico-químicas do princípio ativo. Essa análise inicial garante que a atividade observada nos ensaios in vivo é decorrente do princípio ativo no medicamento. A respeito dos parâmetros físico-químicos que podem ser utilizados durante o desenvolvimento de um xarope, julgue os itens a seguir.
Se duas preparações de xarope com concentrações diferentes do princípio ativo forem colocadas em contato por meio de uma membrana condutora, atingirão o equilíbrio térmico quando atingirem a mesma concentração do princípio ativo.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
Os vasos utilizados no craqueamento catalítico são normalmente de aço e passíveis de corrosão por substâncias presentes nas soluções envolvidas no processo. Uma dessas substâncias é o H 2 S, que pode causar corrosão localizada segundo a equação a seguir.
Fe + H 2 S →FeS + H 2
Considerando as informações acima, julgue os itens a seguir.
Considere que uma barra de zinco seja ligada a um duto de aço por meio de um condutor elétrico. Nesse caso, a partir das reações a seguir, é correto afirmar que essa barra poderá promover uma proteção anticorrosiva para o duto de aço, uma vez que o zinco irá oxidar-se preferencialmente em detrimento do ferro. 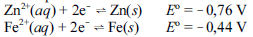
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
Uma solução de CrCl2 é empregada num processo de cromação de um objeto metálico cuja massa antes era 1000 g e depois de transcorridos 40 minutos do processo passou a ser 1010 g. Sabendo-se que 1 Faraday = 96.500 Coulomb, pode-se afirmar que a corrente i), em ampère, utilizada nesse processo foi de aproximadamente
- A. 7,7.
- B. 15,5.
- C. 464.
- D. 928.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
O solvente (absorvente) ideal em uma coluna de absorção é aquele que
I tem uma alta volatilidade para minimizar os custos de sua recuperação.
II tem uma alta solubilidade para o soluto, o que minimiza a sua quantidade na alimentação.
III deve ser estável para minimizar sua reposição.
- A.
Apenas um item está certo.
- B.
Apenas os itens I e II estão certos.
- C.
Apenas os itens e III estão certos.
- D.
Apenas os itens II e III estão certos.
- E.
Todos os itens estão certos.
O processo de desenvolvimento de um fármaco inicia-se com a síntese e a determinação das características físico-químicas do princípio ativo. Essa análise inicial garante que a atividade observada nos ensaios in vivo é decorrente do princípio ativo no medicamento. A respeito dos parâmetros físico-químicos que podem ser utilizados durante o desenvolvimento de um xarope, julgue os itens a seguir.
O volume molar do xarope é muito maior quando comparado ao de um gás.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
Os vasos utilizados no craqueamento catalítico são normalmente de aço e passíveis de corrosão por substâncias presentes nas soluções envolvidas no processo. Uma dessas substâncias é o H 2 S, que pode causar corrosão localizada segundo a equação a seguir.
Fe + H 2 S →FeS + H 2
Considerando as informações acima, julgue os itens a seguir.
De acordo com a equação de corrosão apresentada, o ferro foi oxidado e o hidrogênio, reduzido.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
Dado que Kw = 1,0 × 10-14 e log 2,5 = 0,4, pode-se afirmar que uma solução aquosa 2 x10-3 M de Ba OH)2 apresenta
- A. concentração de íons hidroxila igual a 0,002 mol.L-1.
- B. pOH aproximadamente 11,6.
- C. pH aproximadamente 11,6.
- D. Kb aproximadamente 1,0 × 10-12.
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2008
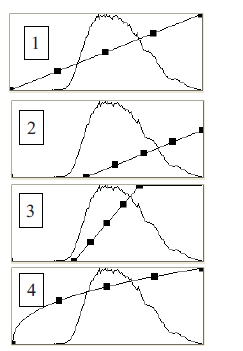
Considere os gráficos abaixo, numerados de 1 a 4, que mostram o histograma de intensidades de uma imagem em tons de cinza. Em cada gráfico, aparece também uma curva de controle de brilho e contraste (look-up table). A curva 1 corresponde à curva original. Logo, a curva 2 representa um (a)
- A.
aumento de brilho. A curva 3 representa um aumento de contraste sem saturação. A curva 4 representa a aplicação de um fator gama, que realça o contraste nas regiões escuras sem saturar as regiões claras.
- B.
redução de brilho e contraste. A curva 3 representa um aumento de contraste. A curva 4 representa a aplicação de um fator gama, que realça o contraste nas regiões claras sem saturar as regiões escuras.
- C.
aumento de brilho sem mudança de contraste. A curva 3 representa um aumento de contraste com saturação em tons altos. A curva 4 representa a aplicação de um fator gama, que realça o contraste nas regiões escuras sem saturar as regiões claras.
- D.
aumento de brilho e uma redução de contraste. A curva 3 representa um aumento de contraste com saturação. A curva 4 representa a aplicação de um fator gama, que realça o contraste nas regiões escuras sem saturar as regiões claras.
- E.
Aumento de brilho e uma redução de contraste. A curva 3 representa um aumento de contraste com saturação. A curva 4 representa a aplicação de um fator gama, que realça o contraste nas regiões escuras sem saturar as regiões claras.


