Questões sobre Eletroquímica
Lista completa de Questões sobre Eletroquímica para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
O princípio da espectroscopia fotoeletrônica se baseia no efeito fotoelétrico, descoberto no final do século XIX por Heinrich Hertz. Nesse princípio, a incidência de luz na superfície de um metal levava à indução de corrente elétrica. Se um experimento semelhante é realizado no estado gasoso, pode-se medir a energia de ionização de um elemento: o fóton da luz incidente transfere energia para o elétron, que é ejetado. A diferença de energia do fóton e do elétron ejetado é a energia de ionização do elemento. Considere as afirmativas abaixo sobre esses experimentos.
I A energia de cada fóton que incidirá na superfície metálica é independente da intensidade da luz.
II Para que o efeito fotoelétrico seja observado no sódio, necessita-se de um maior comprimento de onda que o utilizado para o potássio.
III O comprimento de onda necessário para que haja o efeito fotoelétrico aumentará com a dificuldade em ejetar os elétrons.
IV Para um mesmo elemento, quanto menor o comprimento de onda da luz incidente, maior será a energia cinética do primeiro elétron ejetado.
Estão corretas APENAS as afirmativas
- A.
I e III.
- B.
I e IV.
- C.
II e III.
- D.
II e IV.
- E.
I, II e IV.

- A.
primeiro nível energético.
- B.
terceiro nível energético.
- C.
quarto nível energético.
- D.
quinto nível energético.
- E.
sexto nível energético.
Para se obter exatidão nas medições potenciométricas, deve-se minimizar o potencial de junção líquida, que é causado
- A.
por diferenças na superfície interna e externa dos eletrodos de trabalho.
- B.
pela capacidade de variação na atividade das diferentes espécies de interesse da análise na superfície do eletrodo de trabalho.
- C.
pela diferença na mobilidade de diferentes íons que causa diversidade na distribuição de cargas em regiões distintas do sistema.
- D.
pela saturação da solução do sistema com o oxigênio atmosférico.
- E.
pelo uso de um terceiro eletrodo no sistema, que é o eletrodo auxiliar de platina.
Quando uma molécula absorve radiação eletromagnética na região do visível, provoca transições
- A.
vibracionais apenas.
- B.
rotacionais apenas.
- C.
vibracionais e rotacionais, mas não as eletrônicas.
- D.
que modificam no núcleo do átomo.
- E.
eletrônicas com promoção de elétrons de valência para orbitais de maior energia.
Considere o modelo no qual a luz pode ser tratada como uma onda eletromagnética para avaliar as afirmações a seguir.
I - O comprimento de onda da luz varia em função do índice de refração do meio em que se propaga.
II - A energia da luz é inversamente proporcional ao valor do seu comprimento de onda.
III - A constante de proporcionalidade que relaciona a frequência e o comprimento de onda da luz é a constante de Boltzmann.
Está correto APENAS o que se afirma em
- A.
I
- B.
II
- C.
III
- D.
I e II
- E.
II e III
Texto V, para responder às questões 28 e 29.
O ferro (Fe) é o elemento mais comum entre os metais de transição, compondo mais de 6% da massa das rochas da crosta terrestre. Além de ser o elemento mais abundante da Terra, também é o metal mais utilizado. Os principais minérios de ferro são os óxidos hematita (Fe2O3) e magnetita (Fe3O4). Sabe-se que o ferro é bastante reativo e é corroído em ar úmido. Além disso, do ponto de vista fisiológico, o corpo humano adulto saudável contém cerca de três gramas de ferro, principalmente como hemoglobina. A deficiência de ferro, ou anemia, resulta na redução do transporte de oxigênio para os músculos e para o cérebro e pode gerar vários problemas ao organismo humano.
O ferro, segundo o texto V, tem papel muito importante na composição do organismo humano, em grande parte devido à molécula de hemoglobina. Essa molécula é caracterizada pela possibilidade de carregamento de oxigênio, devido à característica específica do ferro de
- A.
ser caracterizado como um ligante e coordenar-se diretamente a um ácido de Lewis.
- B.
ser caracterizado como um ligante e coordenar-se diretamente a uma base de Lewis.
- C.
apresentar configuração eletrônica de ligante e formar o composto de coordenação.
- D.
ser um ácido de Lewis e formar ligações pelo compartilhamento de pares de elétrons.
- E.
ser uma base de Lewis e formar ligações pelo compartilhamento de pares de elétrons.
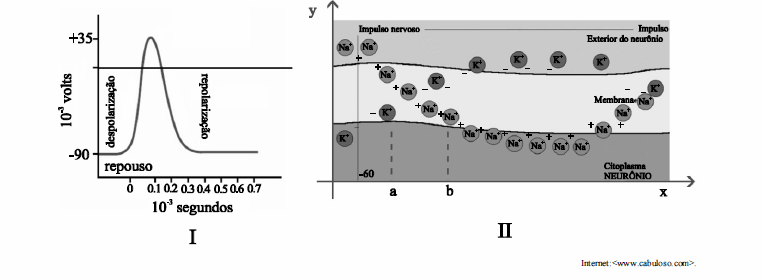
Considerando-se as figuras I e II apresentadas acima, que representam o potencial de ação (VM) de uma célula nervosa em função do tempo, em que a figura II ilustra, no eixo y, o processo da presença dos cátions Na+ e K+ nos meios interno e externo da célula, e, no eixo x, a direção de propagação do impulso elétrico, é correto concluir que
- A.
o potencial VM corresponde à diferença de potencial elétrico entre os pontos a e b representados no eixo x.
- B.
os lipídios não transportam correntes, o que explica a resistência elétrica das membranas.
- C.
o potencial repouso da membrana celular, quando não há perturbação externa, é nulo.
- D.
a concentração do íon Na+ é igual à concentração do íon K+.
Átomos de diferentes elementos químicos podem perder ou ganhar elétrons formando íons que, por sua vez, se ligam de diferentes maneiras, formando uma infinidade de substâncias. Essas ligações podem ocorrer entre diferentes quantidades de íons formando sais ou substâncias denominadas complexos. Acerca desse assunto, julgue os itens que se seguem.
A formação de cátions desocupa orbitais mais externos e diminui as repulsões totais elétron-elétron, fazendo com que a espécie fique menor do que o átomo que lhe deu origem.
- C. Certo
- E. Errado

Com referência à situação hipotética descrita acima, julgue os itens de 54 a 57.
A 1 atm, a fusão do gelo não ocorre espontaneamente em temperaturas inferiores a 273 K, porque o processo levaria a uma diminuição da entropia do sistema.
- C. Certo
- E. Errado
O diodo de junção possui duas regiões de materiais semicondutores dos tipos N e P. Esse dispositivo é amplamente aplicado em circuitos chaveados, como, por exemplo, fontes de alimentação, acionamentos para motores etc. A respeito das características terminais do diodo de junção, julgue os itens a seguir.
Em um diodo típico de silício, em estado de condução, não há queda de tensão entre seus terminais.
- C. Certo
- E. Errado


