Questões sobre Química Inorgânica
Lista completa de Questões sobre Química Inorgânica para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Acerca da produção, da aplicação e das propriedades do etanol, assinale a opção incorreta.
- A.
No Brasil, o etanol é obtido pela fermentação de monossacarídios. Se esse processo não for interrompido, o álcool pode se oxidar a ácido carboxílico.
- B.
O etanol pode ser usado como combustível, como solvente e na conservação de alimentos e bebidas.
- C.
O etanol é miscível em água; suas moléculas fazem ligação de hidrogênio com as moléculas de água.
- D.
A molécula de etanol é apolar, o que justifica que essa substância seja líquida.
Considerando o gráfico e a tabela de indicadores acima, assinale a opção correta.
- A.
Com base no gráfico, é correto concluir que, em pH = 4,76, uma solução de ácido acético contém concentrações iguais do ácido fraco e da base conjugada.
- B.
A curva apresenta o resultado de uma centrifugação, procedimento experimental em que se adiciona volumes conhecidos de uma solução de concentração conhecida a um volume conhecido de uma solução de concentração desconhecida.
- C.
No ponto de equivalência, destacado no gráfico, inexiste ácido acético.
- D.
Entre os indicadores citados, apenas a fenolftaleína não é apropriada para indicar o ponto final da reação.
A Era dos Descobrimentos foi impulsionada, em grande parte, pela demanda da pimenta-do-reino. A pimenta pode ter sido, no início, uma novidade, um luxo que poucos podiam comprar, mas seu poder de disfarçar o ranço, de dar sabor a uma comida seca e insossa, e, ao que parece, de reduzir o gosto da comida conservada em sal a tornou indispensável. O ingrediente ativo da pimenta é a piperina, cuja fórmula estrutural é apresentada a seguir.
Acerca desse assunto e da conservação de alimentos, assinale a opção incorreta.
- A.
A fórmula molecular da piperina é C18H20O3N.
- B.
Pimenta e outros temperos ajudam a retardar as reações de deterioração de alimentos.
- C.
Considerando a fórmula estrutural da capsaicina, mostrada a seguir, e sabendo que essa substância é responsável pela ardência da espécie de pimenta chile, então, se o efeito picante resulta da forma da molécula, comparativamente à molécula de piperina, é correto associar esse efeito ao que há de comum em ambas estruturas: um único anel aromático e átomo de nitrogênio vizinho a átomo de carbono duplamente ligado a oxigênio.
- D.
Na atualidade, a conservação de alimentos industrializados por refrigeração ou por substâncias químicas — umectantes, aromatizantes, corantes etc. — tornou dispensável o uso de especiarias, como pimenta, cravo e canela, como meio de conservar ou mascarar o sabor de alimentos.
Texto para as questões 38 e 39
O dióxido de enxofre e o dióxido de nitrogênio estão entre os poluentes comumente encontrados na atmosfera. O dióxido de enxofre pode originar-se de atividades naturais, como erupções vulcânicas, ou de atividades antropogênicas, como queima de combustíveis ou processos metalúrgicos usados para a obtenção de metais a partir de sulfetos, a exemplo da ustulação da calcopirita, cuja equação de reação é mostrada a seguir.
Ainda considerando o texto, assinale a opção correta.
- A.
A ustulação é um processo exotérmico, daí a tendência dos metais em oxidar.
- B.
O2 e O3 são formas alotrópicas de um mesmo elemento químico e diferem na maneira como os átomos estão ligados.
- C.
Para cada mol de cobre obtido na ustulação da calcopirita, são produzidos 113 L de SO2 nas CNTP.
- D.
NO e NO2 são moléculas que apresentam todos os elétrons emparelhados.
A tabela acima apresenta a composição do ar limpo e seco da homosfera.
Ainda considerando o texto, assinale a opção correta, no que se refere a ligações químicas.
- A.
No ar limpo e seco da homosfera, estão presentes cinco substâncias monoatômicas.
- B.
O2 e N2 são exemplos de substâncias moleculares com tripla e dupla ligações covalentes, respectivamente.
- C.
A geometria da molécula de CO2 é angular.
- D.
Para o hidrocarboneto presente no ar, as ligações do átomo de carbono assumem uma estrutura tetraédrica, característica de hibridação sp2.
A análise físico-química faz uso de várias técnicas que empregam radiação, dos mais variados tipos. Acerca dessas radiações, suas propriedades, seus efeitos na matéria e dos instrumentos que as utilizam, julgue os itens seguintes.
Isótopos são nuclídeos que possuem o mesmo número de massa, mas número de nêutrons diferentes.
- C. Certo
- E. Errado
Alcoóis, sobretudo o metanol e o etanol, têm sido utilizados para substituir combustíveis líquidos. Eles podem ser diretamente queimados como combustíveis para gerar energia. No entanto, eles são usados também indiretamente. Por exemplo, o metanol é empregado para a formação de gasolina em uma reação catalisada por zeólitas, que são aluminossilicatos. As zeólitas são sólidos resultantes da substituição de alguns íons de Si +4 dos silicatos (óxidos de silício) por íons Al +3 . Sua função como catalisador está relacionada à sua capacidade em liberar íons H + . Considerando essas informações, julgue os itens seguintes.
As zeólitas são ácidos de Brønsted.
- C. Certo
- E. Errado
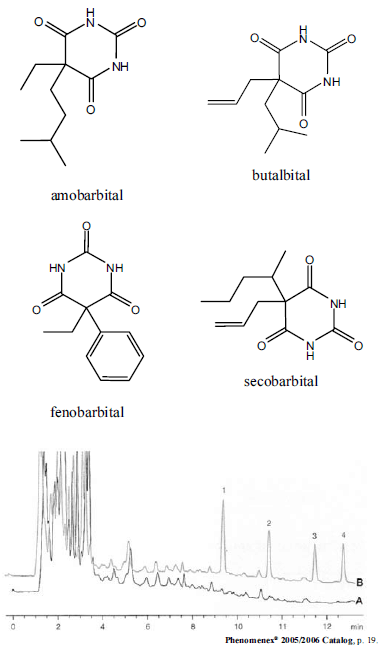
Uma das atividades mais rotineiras em um laboratório de perícia científica é a análise de drogas ilícitas. A figura acima mostra os cromatogramas do branco (A) e de uma amostra de urina humana (B), feitas por cromatografia de fase reversa com uma coluna Synergi ® Max-RP de 150 mm × 4,6 mm, 4 m de diâmetro de partícula, usando gradiente de KH 2 PO 4 20 mmol/L em água, pH 7,0 (solvente A), e acetonitrila (solvente B). Os picos 1, 2, 3 e 4 do cromatograma estão associados às drogas barbitúricas amobarbital, butalbital, fenobarbital e secobarbital, cujas estruturas são mostradas acima. Sabendo que a ordem de polaridade dessas moléculas é secobarbital < amobarbital < butalbital < fenobarbital, é correto concluir que os picos 1, 2, 3 e 4 do cromatograma correspondem, respectivamente, às drogas
- A.
secobarbital, amobarbital, butalbital e fenobarbital.
- B.
amobarbital, secobarbital, fenobarbital e butalbital.
- C.
butalbital, fenobarbital, secobarbital e amobarbital.
- D.
fenobarbital, butalbital, amobarbital, e secobarbital.
Combustíveis podem ser obtidos pela transesterificação de triglicerídeos. Essa reação ocorre entre um triglicerídio e um álcool. Uma reação desse tipo está representada a seguir. 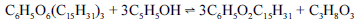
Com respeito a esse equilíbrio, julgue os itens a seguir.
A constante de equilíbrio dessa reação é
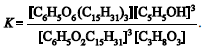 .
.
- C. Certo
- E. Errado
O uso da biomassa tem-se tornado uma alternativa viável e ambientalmente mais adequada que o petróleo. Nessa perspectiva, óleos e gorduras, genericamente denominados triglicerídeos (figura abaixo), têm sido estudados para a produção de materiais de interesse comercial e industrial.
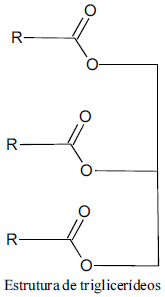
Por meio de craqueamento, é possível obter combustíveis. A pirólise de óleos e gorduras ocorre a temperaturas superiores a 300 ºC, em que se pode ainda fazer uso de catalisadores.
Com referência ao texto acima, julgue os itens seguintes.A presença da ligação B entre os átomos de carbono e oxigênio nas moléculas de triglicerídeos aumenta a estabilidade da ligação entre esses dois átomos, mas, ao mesmo tempo, torna essa ligação mais reativa.
- C. Certo
- E. Errado


