Questões de Química da Fundação CESGRANRIO (CESGRANRIO)
Lista completa de Questões de Química da Fundação CESGRANRIO (CESGRANRIO) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.

- A.

- B.

- C.

- D.

- E.

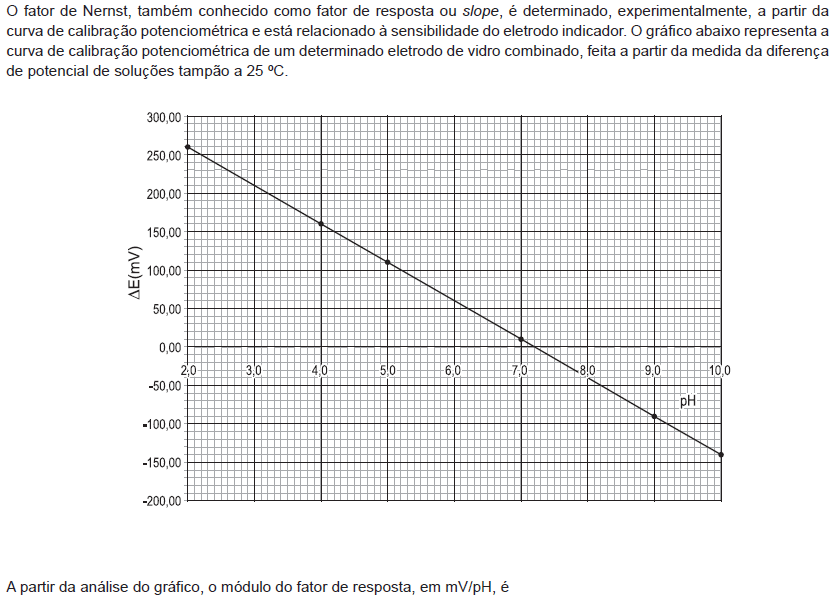
- A.
7
- B.
50
- C.
59
- D.
96
- E.
260
A gasolina é formada por cadeias carbônicas lineares ou ramificadas, com 6 a 12 átomos de carbono por cadeia. Qual das técnicas abaixo é indicada para identificar e quantificar os componentes presentes em uma amostra de gasolina?
- A.
Titulação potenciométrica
- B.
Espectrometria de absorção atômica
- C.
Espectrometria de difração de raios X
- D.
Cromatografia gasosa
- E.
Coulometria
Uma amostra de 500 mg de calcário (carbonato de cálcio) impuro foi introduzida em um tubo de ensaio com saída lateral. Para esse tubo foi transferida, em excesso, solução de ácido clorídrico, que reagiu completamente com o carbonato de cálcio presente na amostra. O gás liberado foi recolhido em um cilindro de vidro de 500,0 cm3 de volume interno e altura de 500,0 mm. O cilindro estava completamente cheio de líquido inerte e imiscível com o gás e, conforme o gás entrava no cilindro, o líquido era expulso, sendo possível medir o volume de gás liberado pela reação. Ao final do experimento, o líquido ocupava 400,0 mm da altura do cilindro. A percentagem de carbonato de cálcio, na amostra de calcário, considerando-se que, nas condições do experimento, o volume molar dos gases é de 25,0 L/mol e as impurezas presentes são inertes, é
- A.
25%
- B.
40%
- C.
60%
- D.
80%
- E.
95%
A cromatografia é um método físico-químico de separação fundamentado na migração diferencial dos componentes de uma mistura, que ocorre por diferentes interações entre duas fases, a fase móvel e a fase estacionária. Pertencem à classe de cromatografia em coluna as cromatografias
- A.
em camada delgada (CCD) e gasosa (CG)
- B.
líquida de alta eficiência (CLAE) e gasosa (CG)
- C.
líquida de alta eficiência (CLAE) e em camada delgada (CCD)
- D.
em papel (CP) e gasosa (CG)
- E.
em papel (CP) e em camada delgada (CCD)

- A.
I e II.
- B.
I e IV.
- C.
II e III.
- D.
I, III e IV.
- E.
II, III e IV.
Uma amostra de 20 mL de sulfato de ferro (II) e de amônio 0,1 M foi analisada por titulação potenciométrica com uma solução de sulfato de cério (IV) 0,1095 M, usando-se eletrodos de platina e de calomelano saturado. Observando essa análise potenciométrica, analise as afirmativas abaixo.
I - O eletrodo de calomelano é um eletrodo de referência e é composto de mercúrio e cloreto de mercúrio (I), cobertos com uma solução de cloreto de potássio saturada.
II - Nessa análise potenciométrica, o cério se oxida a Ce3+, e o ferro se reduz a Fe3+.
III - Trata-se de uma potenciometria direta, e o eletrodo indicador é a platina.
Está correto o que se afirma em
- A.
I, apenas.
- B.
II, apenas.
- C.
I e III, apenas.
- D.
II e III, apenas.
- E.
I, II e III.
Considere que, no início do experimento, em vez de 56 g de but-1-eno, foram utilizados 56 g de monóxido de carbono. Os gases nitrogênio e monóxido de carbono não reagem entre si e apresentam comportamento ideal. Na câmara P, antes da Válv. 2 ser aberta, a temperatura do sistema era, também, de 300 K, e a pressão medida do sistema foi de P2. A relação entre as pressões, utilizando o but-1-eno, P1, e o monóxido de carbono, P2, é
- A.
P1 = P2
- B.
P1 = 2P2
- C.
2P1 = P2
- D.
2P1 = 3P2
- E.
3P1 = 2P2
Analise as afirmativas abaixo sobre as determinações analíticas quantitativas com base na Espectroscopia por Adsorção Molecular.
I - O método utilizado para a determinação quantitativa da concentração de uma substância através da absorção da radiação é baseada na Lei de Beer-Lambert.
II - A Lei de Beer é limitada a soluções diluídas porque considera que há interações dos centros absorventes com outras espécies presentes nestas soluções.
III - A Lei de Beer se aplica a soluções concentradas porque a interação entre as moléculas não afeta a distribuição de cargas na espécie absorvente, o que alteraria o coefi ciente de absortividade molar.
IV - Desvios químicos da Lei de Beer ocorrem quando um analito se dissocia, se associa ou reage com um solvente gerando um produto cujo espectro de absorção é diferente do analito.
Está correto APENAS o que se afirma em
- A.
I
- B.
I e II
- C.
I e IV
- D.
II e III
- E.
III e IV
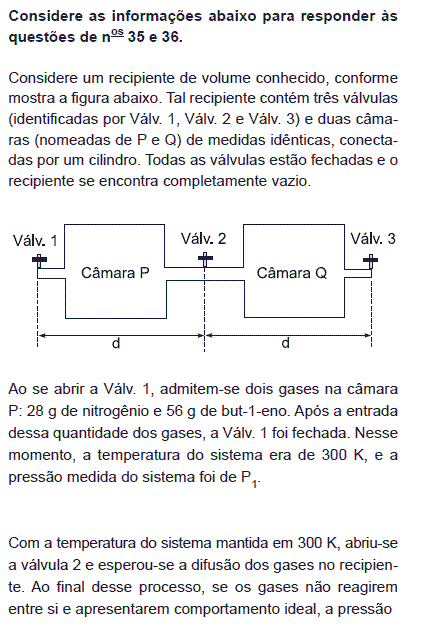
- A.
final do sistema será igual a P1.
- B.
final do sistema será igual ao dobro de P1.
- C.
parcial dos dois gases permanecerá constante.
- D.
parcial do gás nitrogênio será quatro vezes menor que P1.
- E.
parcial do but-1-eno será o dobro da do nitrogênio.


