Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE)
Lista completa de Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
Com relação à química analítica quantitativa instrumental, julgue os itens de 114 a 120. A fotometria de chama é uma técnica de absorção atômica amplamente utilizada na química analítica para detecção de elementos de massa atômica reduzida como sódio, potássio, cálcio, nitrogênio, oxigênio e hidrogênio.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
Considere as situações I e II a seguir.

Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
Em uma titulação de neutralização, caso a adição do indicador gere uma solução de coloração muito escura, aconselha-se adicionar água ao titulado para que a coloração fique mais clara, o que torna mais precisa e exata a detecção do ponto final da titulação.- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
Considere as situações I e II a seguir.

Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
Uma maneira de eliminar os erros aleatórios relativos às medidas de volume durante a titulação na situação II é a utilização de uma bureta eletrônica no lugar da vidraria convencional.- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
Considere as situações I e II a seguir.

Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
Diferentemente da volumetria de neutralização, a volumetria de oxirredução é limitada pela impossibilidade de se utilizar indicadores que acusem o final da titulação por meio da mudança de cor do sistema.- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
Considere as situações I e II a seguir.
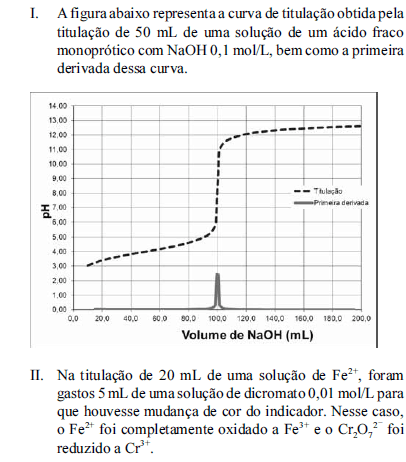
Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
Na situação II, a concentração de Fe2+ na amostra é superior a 0,010 mol/L.- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
Considere as situações I e II a seguir.
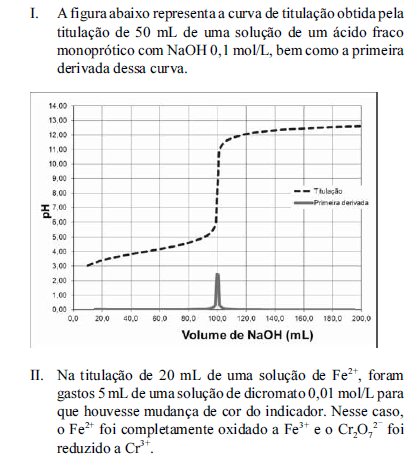
Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
O ácido titulado na situação I é mais forte que o ácido propiônico, que tem pKa = 4,9.- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
Considere as situações I e II a seguir.

Com base nas situações apresentadas acima, julgue os itens a seguir, relativos à química analítica clássica.
Na situação I, a concentração do ácido titulado é o dobro da concentração da base utilizada nessa titulação.- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
Acerca dos aspectos estatísticos da representatividade de análises laboratoriais, julgue o item abaixo. O valor de pureza anotado nos rótulos de reagentes comerciais é aproximado e representa a média de uma população imensurável. Para que o valor fosse real, cada amostra, que é uma réplica da população, deveria ser dosada individualmente.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
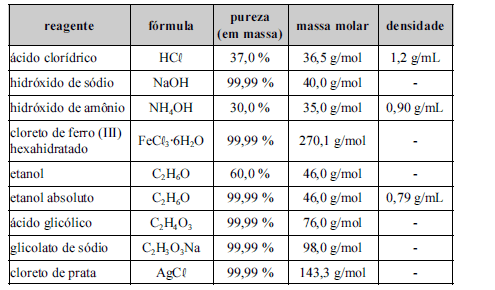
A tabela acima apresenta reagentes utilizados para o preparo de algumas soluções. Com base nessas informações, julgue os itens a seguir.
A mistura de 100 mL de etanol a 60,0 % com 100 mL de etanol absoluto produz uma solução final de concentração superior a 75,0 % em massa.- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015

A tabela acima apresenta reagentes utilizados para o preparo de algumas soluções. Com base nessas informações, julgue os itens a seguir.
Em 500 mL de uma solução de NaOH 0,2 mol/L, a massa de NaOH contida é maior que 5,0 g.- C. Certo
- E. Errado


