Questões de Química da Fundação Universa (FUNIVERSA)
Lista completa de Questões de Química da Fundação Universa (FUNIVERSA) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Uma solução tamponada resiste a uma mudança de pH quando pequenas quantidades de ácido ou base são adicionadas. Na bioquímica, soluções-tampão são muito importantes porque o funcionamento dos sistemas biológicos depende muito do pH. A propósito desse assunto, um tampão ácido é preparado utilizando-se uma solução aquosa que contenha
- A. NH3 e NH4 +.
- B. HCl e HNO3.
- C. HCl e NaOH.
- D. NaOH e NH3.
- E. CH3COOH e CH3CO2 −.
O pH de uma solução é medido eletroquimicamente com um aparelho denominado pHmetro. O medidor deve ser calibrado com pelo menos duas soluções-tampão padrões (pH conhecido) e o potencial medido é transformado no pH da solução, que é, então, visualizado. No processo de calibração desse equipamento para análise de uma amostra desconhecida, os valores de pH dos padrões para calibração devem
- A. se aproximar do valor do pH da amostra.
- B. apresentar valores de pH acima do valor do pH da amostra.
- C. apresentar valores de pH abaixo do valor do pH da amostra.
- D. ser selecionados de modo que o pH da amostra fique dentro da faixa definida pelos padrões.
- E. ser escolhidos de tal forma que a amostra apresente pH exatamente igual ao valor de um dos padrões.
O ácido oxálico (etanodioico) é usado em lavanderias comerciais e na remoção de ferrugem e de depósitos em radiadores de automóveis. Esses usos são consequência da capacidade do ácido oxálico de formar complexos solúveis com os íons ferro. Essa propriedade também o torna bastante venenoso. O nome deriva do grego oxalis, que significa ácido, e do gênero de algumas plantas herbáceas. Os cálculos renais, por exemplo, são formados por depósitos de oxalato de cálcio, na forma de pequenos cristais que não se dissolvem. As figuras seguintes representam, respectivamente, as fórmulas da molécula de ácido oxálico e do composto oxalato de cálcio.
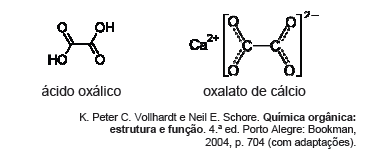
Os ácidos carboxílicos são caracterizados pela presença do grupo carbóxi (carboxila). Esses grupos ácidos são frequentemente escritos como COOH ou CO2H. Com base nessas afirmações e no texto VI, é correto afirmar que, em geral, nos ácidos carboxílicos, o grupo funcional carboxila é formado por uma unidade
- A.
idróxi ligada ao carbono eletrofílico de uma carbonila.
- B.
acética ligada ao carbono eletrofílico de uma carbonila.
- C.
fórmica ligada ao carbono eletrofílico de uma carbonila.
- D.
hidróxi ligada ao carbono nucleofílico de uma carbonila.
- E.
acética ligada ao carbono nucleofílico de uma carbonila.
Partindo da estrutura atômica da matéria, a fórmula química representa uma coleção de símbolos químicos e subscritos que indica a composição de uma substância. Assinale a alternativa que apresenta, nesta ordem, uma fórmula molecular e uma fórmula unitária.
- A.
NaCl e H2
- B.
NH3 e Fe2O3
- C.
H2O e CH3CH2OH
- D.
NaHCO3 e CaCO3
- E.
Mg3(PO4)2 e CH3COOH
Texto V, para responder às questões 28 e 29.
O ferro (Fe) é o elemento mais comum entre os metais de transição, compondo mais de 6% da massa das rochas da crosta terrestre. Além de ser o elemento mais abundante da Terra, também é o metal mais utilizado. Os principais minérios de ferro são os óxidos hematita (Fe2O3) e magnetita (Fe3O4). Sabe-se que o ferro é bastante reativo e é corroído em ar úmido. Além disso, do ponto de vista fisiológico, o corpo humano adulto saudável contém cerca de três gramas de ferro, principalmente como hemoglobina. A deficiência de ferro, ou anemia, resulta na redução do transporte de oxigênio para os músculos e para o cérebro e pode gerar vários problemas ao organismo humano.
O ferro, segundo o texto V, tem papel muito importante na composição do organismo humano, em grande parte devido à molécula de hemoglobina. Essa molécula é caracterizada pela possibilidade de carregamento de oxigênio, devido à característica específica do ferro de
- A.
ser caracterizado como um ligante e coordenar-se diretamente a um ácido de Lewis.
- B.
ser caracterizado como um ligante e coordenar-se diretamente a uma base de Lewis.
- C.
apresentar configuração eletrônica de ligante e formar o composto de coordenação.
- D.
ser um ácido de Lewis e formar ligações pelo compartilhamento de pares de elétrons.
- E.
ser uma base de Lewis e formar ligações pelo compartilhamento de pares de elétrons.
Texto V, para responder às questões 28 e 29.
O ferro (Fe) é o elemento mais comum entre os metais de transição, compondo mais de 6% da massa das rochas da crosta terrestre. Além de ser o elemento mais abundante da Terra, também é o metal mais utilizado. Os principais minérios de ferro são os óxidos hematita (Fe2O3) e magnetita (Fe3O4). Sabe-se que o ferro é bastante reativo e é corroído em ar úmido. Além disso, do ponto de vista fisiológico, o corpo humano adulto saudável contém cerca de três gramas de ferro, principalmente como hemoglobina. A deficiência de ferro, ou anemia, resulta na redução do transporte de oxigênio para os músculos e para o cérebro e pode gerar vários problemas ao organismo humano.
Conforme o texto V, o minério de ferro é um dos materiais mais empregados pela indústria metalúrgica no mundo. Acerca do processo metalúrgico de obtenção do ferro metálico, algumas reações ocorrem no alto forno; entre elas, a
- A.
oxidação dos minérios de ferro e a saída de escória e ferro fundido.
- B.
oxidação dos minérios de ferro e a saída de escória e ferro fundido.
- C.
redução dos minérios de ferro com dióxido de carbono produzido no forno.
- D.
oxidação dos minérios de ferro com monóxido de carbono e saída de ferro fundido.
- E.
redução dos minérios de ferro com monóxido de carbono e saída de escória e ferro fundido.
Grande parte das amostras encontradas na natureza é composta por misturas complexas. Por isso, na maioria dos trabalhos analíticos, é necessário o trabalho de separar os componentes dessas misturas. Essas etapas, muitas vezes, são seguidas pela identificação e pela quantificação de um ou mais componentes presentes na mistura. Com base nos fundamentos das separações analíticas, em especial no método de extração por solvente, a eficiência do processo de extração será maior quando forem
- A.
efetuadas poucas extrações com volumes grandes.
- B.
efetuadas poucas extrações com volumes pequenos.
- C.
utilizados líquidos miscíveis que permanecem em fases separadas quando misturados em qualquer proporção.
- D.
efetuadas muitas extrações com volumes pequenos do que se forem realizadas poucas extrações com volumes grandes.
- E.
efetuadas poucas extrações com volumes grandes do que se forem feitas muitas extrações com volumes pequenos.

Sabe-se que, do ponto de vista ambiental, os avanços alcançados pela química moderna não estão apenas ligados a aspectos negativos. Com base nessa afirmação, no texto acima e na importância social da química, é correto afirmar que devem ser buscadas
- A.
novas técnicas para o tratamento de efluentes tóxicos, sem a necessidade de uso de fontes de energia sustentáveis.
- B.
novas tecnologias que visem ao desenvolvimento de processos químicos mais eficientes e menos agressivos ao meio ambiente.
- C.
novas tecnologias de redução, mas não de eliminação, do uso de substâncias tóxicas perigosas em processos químicos.
- D.
reduções de custos, mas não a redução da poluição, necessária para o desenvolvimento de processos químicos mais eficientes.
- E.
reduções de poluição, mas não a redução de custos, visando ao desenvolvimento de processos químicos menos agressivos ao meio ambiente.
Com relação à tabela periódica e às reações de oxidorredução, assinale a alternativa correta.
- A.
A energia de ionização (EI) cresce da esquerda para a direita; no entanto, a EI do alumínio é menor que a do magnésio.
- B.
Todos os halogênios formam hidrácidos fortes.
- C.
Os óxidos metálicos têm caráter ácido.
- D.
Os elementos metálicos não formam compostos hidrogenados.
- E.
O raio do íon Mg+2 é maior do que o raio do Mg metálico.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação Universa (FUNIVERSA) - 2010
Com relação à tabela periódica e às reações de oxidorredução, assinale a alternativa correta.
- A.
A energia de ionização (EI) cresce da esquerda para a direita; no entanto, a EI do alumínio é menor que a do magnésio.
- B.
Todos os halogênios formam hidrácidos fortes.
- C.
Os óxidos metálicos têm caráter ácido.
- D.
Os elementos metálicos não formam compostos hidrogenados.
- E.
O raio do íon Mg+2 é maior do que o raio do Mg metálico.


