Questões de Engenharia Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE)
Lista completa de Questões de Engenharia Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Um tanque é completamente preenchido com 16,0 kg de metano puro (CH4), componente majoritário do gás natural. A equação a seguir apresenta a reação de combustão do metano, cuja entalpia-padrão, a 25 ºC, é igual a !890 kJ/mol.
CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (R)
Com base na informações acima e considerando que a massa molar do metano seja 16,0 g/mol, que a constante universal dos gases valha 0,08 atm.L.mol-1 K-1 e que os gases envolvidos na reação se comportem de forma ideal, julgue os itens que se seguem.
Considerando que a uma temperatura de 270 K o metano tenha atingido uma pressão de 200 atm e que nessas condições o fator de compressibilidade do gás tenha sido igual a 0,80, é correto inferir que o tanque em questão possui volume maior que 100 L.
- C. Certo
- E. Errado
Um tanque é completamente preenchido com 16,0 kg de metano puro (CH4), componente majoritário do gás natural. A equação a seguir apresenta a reação de combustão do metano, cuja entalpia-padrão, a 25 ºC, é igual a !890 kJ/mol.
CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (R)
Com base na informações acima e considerando que a massa molar do metano seja 16,0 g/mol, que a constante universal dos gases valha 0,08 atm.L.mol-1 K-1 e que os gases envolvidos na reação se comportem de forma ideal, julgue os itens que se seguem.
O módulo do calor de combustão padrão do metano, a volume constante e a 25 ºC, é maior que 890 kJ/mol.
- C. Certo
- E. Errado
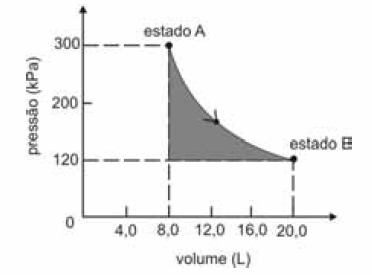
A figura seguinte ilustra, em um diagrama de pressão versus volume, a expansão isotérmica reversível de um mol de um gás ideal, desde um estado inicial A, correspondente a uma pressão de 300 kPa e um volume de 8,00 L, até um estado final B, com pressão e volume iguais a 100 kPa e 20,00 L, respectivamente.
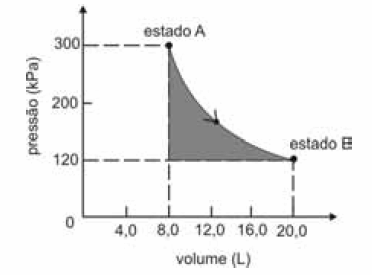
Com base nessas informações e considerando que a constante universal dos gases, R, seja igual a 8,3 .J.mol -1 K -1 e que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue os itens a seguir.
O calor, q, que entra para o sistema a partir das vizinhanças durante a transformação em questão é maior que o produto nRT, em que n e T representam, respectivamente, a quantidade de matéria e a temperatura do gás.
- C. Certo
- E. Errado
A figura seguinte ilustra, em um diagrama de pressão versus volume, a expansão isotérmica reversível de um mol de um gás ideal, desde um estado inicial A, correspondente a uma pressão de 300 kPa e um volume de 8,00 L, até um estado final B, com pressão e volume iguais a 100 kPa e 20,00 L, respectivamente.
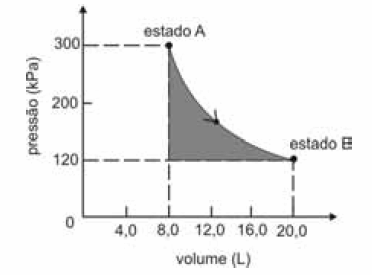
Com base nessas informações e considerando que a constante universal dos gases, R, seja igual a 8,3 .J.mol -1 K -1 e que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue os itens a seguir.
A variação de entropia durante a transformação descrita é maior que 5 J/K.
- C. Certo
- E. Errado
A figura seguinte ilustra, em um diagrama de pressão versus volume, a expansão isotérmica reversível de um mol de um gás ideal, desde um estado inicial A, correspondente a uma pressão de 300 kPa e um volume de 8,00 L, até um estado final B, com pressão e volume iguais a 100 kPa e 20,00 L, respectivamente.
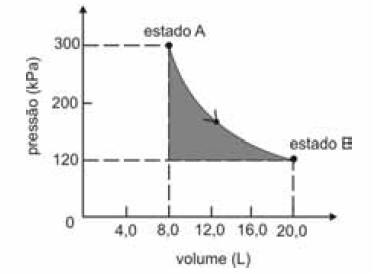
Com base nessas informações e considerando que a constante universal dos gases, R, seja igual a 8,3 .J.mol -1 K -1 e que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue os itens a seguir.
Considere que, após a referida transformação, o sistema tenha retornado ao estado A. Nessa situação, qualquer que seja o caminho de retorno, o calor trocado com as vizinhanças e o trabalho realizado pelo sistema durante o ciclo (estado A → estado B → estado A) são ambos iguais a zero, pois calor e trabalho são funções de estado termodinâmicas.
- C. Certo
- E. Errado
A figura seguinte ilustra, em um diagrama de pressão versus volume, a expansão isotérmica reversível de um mol de um gás ideal, desde um estado inicial A, correspondente a uma pressão de 300 kPa e um volume de 8,00 L, até um estado final B, com pressão e volume iguais a 100 kPa e 20,00 L, respectivamente.
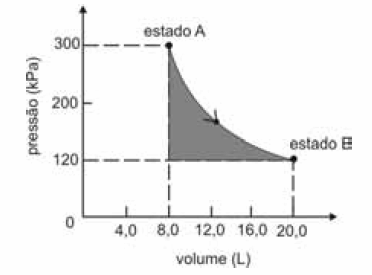
Com base nessas informações e considerando que a constante universal dos gases, R, seja igual a 8,3 .J.mol -1 K -1 e que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue os itens a seguir.
A temperatura do gás é maior que 300 K.
- C. Certo
- E. Errado
A figura seguinte ilustra, em um diagrama de pressão versus volume, a expansão isotérmica reversível de um mol de um gás ideal, desde um estado inicial A, correspondente a uma pressão de 300 kPa e um volume de 8,00 L, até um estado final B, com pressão e volume iguais a 100 kPa e 20,00 L, respectivamente.
Com base nessas informações e considerando que a constante universal dos gases, R, seja igual a 8,3 .J.mol -1 K -1 e que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue os itens a seguir.
A área sombreada do gráfico corresponde ao trabalho realizado pelo gás durante a referida expansão.
- C. Certo
- E. Errado
Para a seguinte reação, a constante de equilíbrio a uma temperatura T é igual a 400.
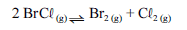
Com base nessa informação e considerando que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue os itens seguintes.
Para a reação em questão, o volume da câmara não influencia a velocidade com que o equilíbrio é atingido.
- C. Certo
- E. Errado
Para a seguinte reação, a constante de equilíbrio a uma temperatura T é igual a 400.
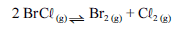
Com base nessa informação e considerando que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue os itens seguintes.
Considerando que a reação seja endotérmica em toda a faixa compreendida entre as temperaturas T e T e que T seja maior que T, é correto concluir que a constante de equilíbrio da reação na temperatura T é superior a 400.
- C. Certo
- E. Errado
Para a seguinte reação, a constante de equilíbrio a uma temperatura T é igual a 400.
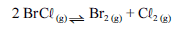
Com base nessa informação e considerando que os logaritmos naturais de 5 e 2 sejam iguais a 1,609 e 0,693, respectivamente, julgue os itens seguintes.
Se 10,0 mol de BrCR(g) forem colocados em uma câmara inicialmente evacuada, quando o equilíbrio químico for atingido, à temperatura T, a quantidade de matéria de Br2 será inferior a 6,0 mol.
- C. Certo
- E. Errado


