Questões de Engenharia Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE)
Lista completa de Questões de Engenharia Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
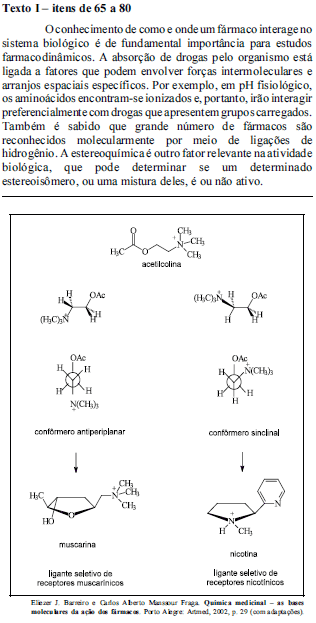
O esquema acima mostra a fórmula estrutural da acetilcolina e dois tipos de representação de seus isômeros conformacionais, cujo metabolismo conduz à formação de substâncias distintas, que são ligantes específicos de receptores muscarínicos e nicotínicos. Considerando as informações do texto I e o esquema acima, julgue os itens que se seguem.
O confôrmero antiperiplanar é mais estável que o sinclinal.
- C. Certo
- E. Errado
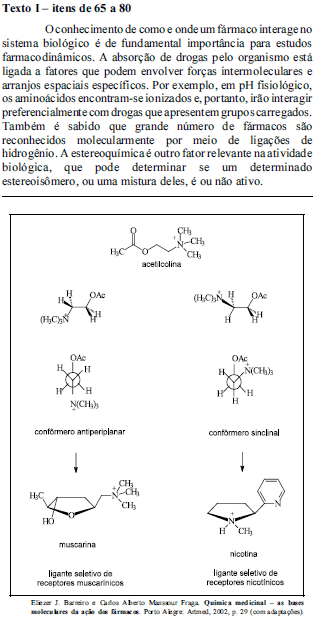
O esquema acima mostra a fórmula estrutural da acetilcolina e dois tipos de representação de seus isômeros conformacionais, cujo metabolismo conduz à formação de substâncias distintas, que são ligantes específicos de receptores muscarínicos e nicotínicos. Considerando as informações do texto I e o esquema acima, julgue os itens que se seguem.

- C. Certo
- E. Errado
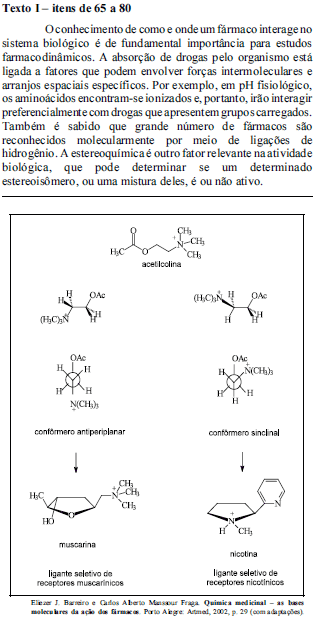
O esquema acima mostra a fórmula estrutural da acetilcolina e dois tipos de representação de seus isômeros conformacionais, cujo metabolismo conduz à formação de substâncias distintas, que são ligantes específicos de receptores muscarínicos e nicotínicos. Considerando as informações do texto I e o esquema acima, julgue os itens que se seguem.
Na estrutura da muscarina, existem somente três átomos de carbono quiral.
- C. Certo
- E. Errado
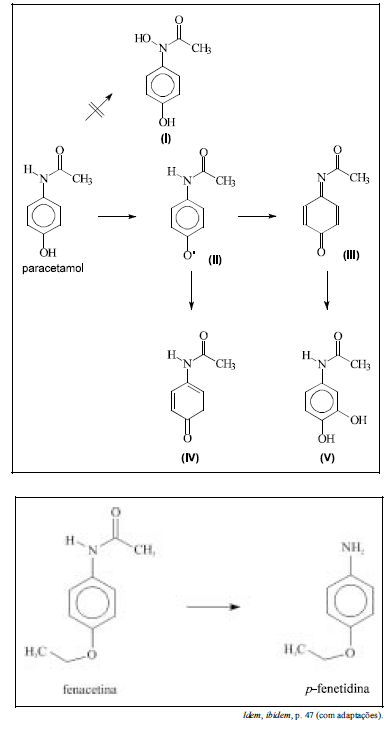
Os esquemas acima ilustram o metabolismo parcial de duas drogas: o paracetamol e a fenacetina. O estudo do metabolismo de um fármaco é importante, pois o conhecimento das possíveis substâncias formadas nas etapas de biotransformação fornece idéia dos possíveis efeitos colaterais e das substâncias a eles associadas, bem como dos virtuais marcadores moleculares da presença dessa droga no organismo.
No contexto do texto I, considerando as informações e os esquemas acima, julgue os itens a seguir.
Entre todos os compostos apresentados em ambos os esquemas, apenas o composto III não forma ligações de hidrogênio intermoleculares entre suas moléculas.
- C. Certo
- E. Errado
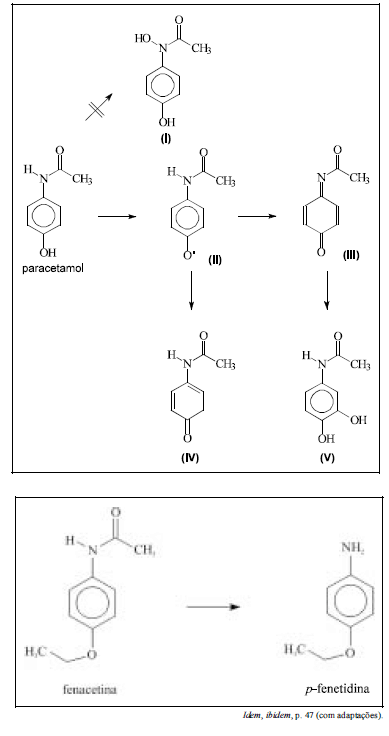
Os esquemas acima ilustram o metabolismo parcial de duas drogas: o paracetamol e a fenacetina. O estudo do metabolismo de um fármaco é importante, pois o conhecimento das possíveis substâncias formadas nas etapas de biotransformação fornece idéia dos possíveis efeitos colaterais e das substâncias a eles associadas, bem como dos virtuais marcadores moleculares da presença dessa droga no organismo.
No contexto do texto I, considerando as informações e os esquemas acima, julgue os itens a seguir.
O paracetamol é mais ácido que o composto V.
- C. Certo
- E. Errado
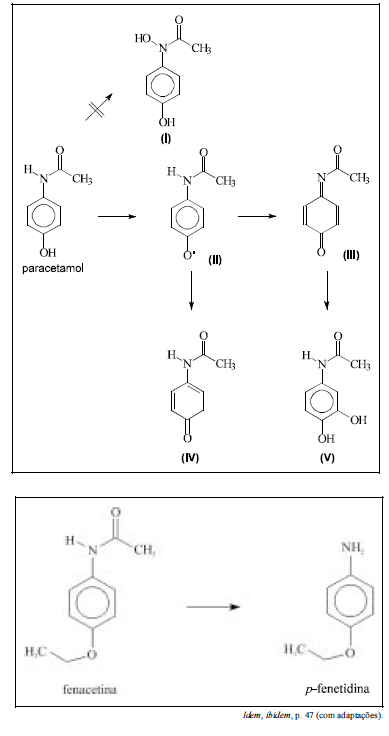
Os esquemas acima ilustram o metabolismo parcial de duas drogas: o paracetamol e a fenacetina. O estudo do metabolismo de um fármaco é importante, pois o conhecimento das possíveis substâncias formadas nas etapas de biotransformação fornece idéia dos possíveis efeitos colaterais e das substâncias a eles associadas, bem como dos virtuais marcadores moleculares da presença dessa droga no organismo.
No contexto do texto I, considerando as informações e os esquemas acima, julgue os itens a seguir.
Na rota metabólica do paracetamol, a aromaticidade do sistema inicial é mantida em todas as fases apresentadas.
- C. Certo
- E. Errado
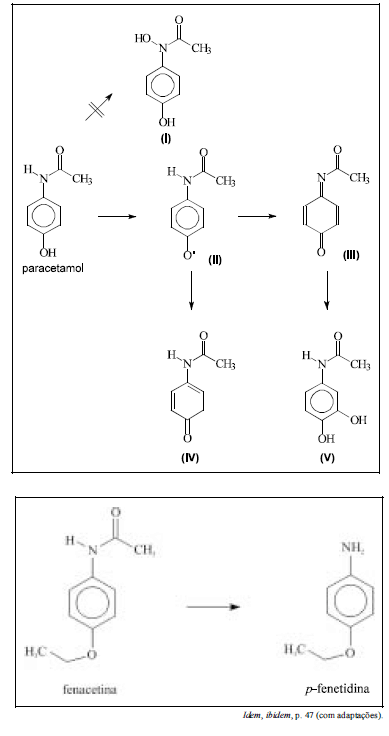
Os esquemas acima ilustram o metabolismo parcial de duas drogas: o paracetamol e a fenacetina. O estudo do metabolismo de um fármaco é importante, pois o conhecimento das possíveis substâncias formadas nas etapas de biotransformação fornece idéia dos possíveis efeitos colaterais e das substâncias a eles associadas, bem como dos virtuais marcadores moleculares da presença dessa droga no organismo.
No contexto do texto I, considerando as informações e os esquemas acima, julgue os itens a seguir.
A fenacetina é mais básica que a p-fenetidina.
- C. Certo
- E. Errado
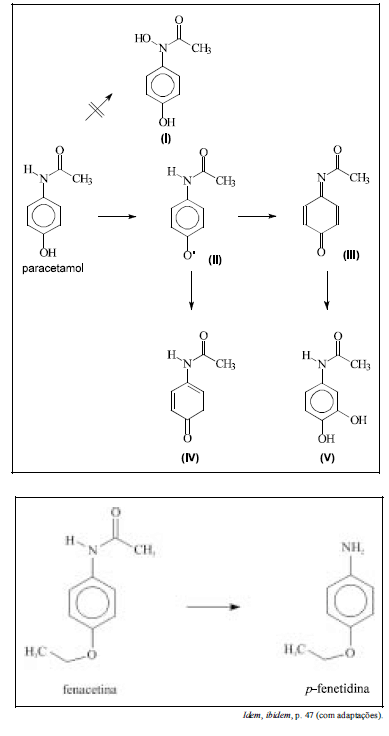
Os esquemas acima ilustram o metabolismo parcial de duas drogas: o paracetamol e a fenacetina. O estudo do metabolismo de um fármaco é importante, pois o conhecimento das possíveis substâncias formadas nas etapas de biotransformação fornece idéia dos possíveis efeitos colaterais e das substâncias a eles associadas, bem como dos virtuais marcadores moleculares da presença dessa droga no organismo.
No contexto do texto I, considerando as informações e os esquemas acima, julgue os itens a seguir.
Todos os substituintes ligados ao anel da fenacetina e da p-fenetidina são considerados orientadores orto/para em reações de substituição eletrofílica aromática.
- C. Certo
- E. Errado
O 1,2–dibromoetano, um líquido com odor levemente adocicado, já foi muito empregado como fumigante em produtos agrícolas e como aditivo de gasolina. Seu uso foi drasticamente reduzido por ser uma substância com potencial carcinogênico e possuir elevada toxicidade aguda por via oral, dérmica e inalatória, podendo acarretar em morte. Muitas substâncias utilizadas no controle de insetos em residências e na agricultura possuem alta toxicidade. Existem vários relatos de intoxicações de pessoas expostas a esses tipos de produtos. Muitos estudos visam à busca de novas substâncias com características toxicológicas e ecotoxicológicas mais amenas. O controle biológico de pragas, por utilização de feromônios e hormônios juvenis, tem sido visto como uma alternativa mais segura ao ser humano e menos danosa ao meio ambiente. A figura abaixo ilustra as formas anti, vici e eclipsadas para o 1,2–dibromoetano, e a estrutura do hormônio juvenil que atua no ciclo de desenvolvimento de muitas espécies de insetos, mantendo-os em seus estados larvais. Larvas tratadas com soluções diluídas desse hormônio morrem antes de se tornarem insetos adultos, controlando, portanto, o crescimento da população.
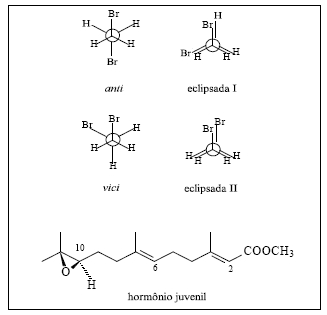
A conformação anti possui momento de dipolo maior que a conformação eclipsada II.
- C. Certo
- E. Errado
O 1,2–dibromoetano, um líquido com odor levemente adocicado, já foi muito empregado como fumigante em produtos agrícolas e como aditivo de gasolina. Seu uso foi drasticamente reduzido por ser uma substância com potencial carcinogênico e possuir elevada toxicidade aguda por via oral, dérmica e inalatória, podendo acarretar em morte. Muitas substâncias utilizadas no controle de insetos em residências e na agricultura possuem alta toxicidade. Existem vários relatos de intoxicações de pessoas expostas a esses tipos de produtos. Muitos estudos visam à busca de novas substâncias com características toxicológicas e ecotoxicológicas mais amenas. O controle biológico de pragas, por utilização de feromônios e hormônios juvenis, tem sido visto como uma alternativa mais segura ao ser humano e menos danosa ao meio ambiente. A figura abaixo ilustra as formas anti, vici e eclipsadas para o 1,2–dibromoetano, e a estrutura do hormônio juvenil que atua no ciclo de desenvolvimento de muitas espécies de insetos, mantendo-os em seus estados larvais. Larvas tratadas com soluções diluídas desse hormônio morrem antes de se tornarem insetos adultos, controlando, portanto, o crescimento da população.

Sabendo que o momento de dipolo observado experimentalmente para o 1,2–dibromoetano é igual a 1,0 D, conclui-se que a conformação preferencial da molécula em questão é a vici, pois as interações atrativas entre as nuvens eletrônicas dos átomos de bromo reduzem a energia total da molécula.
- C. Certo
- E. Errado


