Questões de Farmácia da Fundação de desenvolvimento da pesquisa (FUNDEP / UFMG)
Lista completa de Questões de Farmácia da Fundação de desenvolvimento da pesquisa (FUNDEP / UFMG) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Farmácia - Formulações farmacêuticas - Fundação de desenvolvimento da pesquisa (FUNDEP / UFMG) - 2013
Um medicamento na forma líquida foi submetido ao ensaio de Contagem microbiana por meio de diluição em placas contendo ágar, para verificação do número de micro-organismos totais no produto. As leituras das placas com as diluições são apresentadas na tabela abaixo.
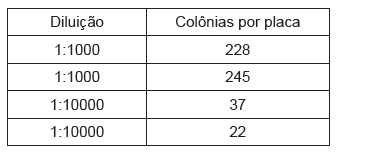
É correto afirmar que o número de unidades formadoras de colônia, por mL, no produto (UFC/mL) é:
- A. 1,06 x 105 UFC/mL.
- B. 2,66 x 105 UFC/mL.
- C. 2,66 x 106 UFC/mL.
- D. 1,06 x 106 UFC/mL.
Farmácia - Formulações farmacêuticas - Fundação de desenvolvimento da pesquisa (FUNDEP / UFMG) - 2013
Desintegração é um teste amplamente utilizado no controle de qualidade de formas farmacêuticas sólidas. Esse teste se aplica às formas farmacêuticas descritas abaixo, EXCETO:
- A. comprimidos revestidos com filme.
- B. comprimidos solúveis.
- C. comprimidos com liberação prolongada.
- D. comprimidos com liberação retardada.
Farmácia - Formulações farmacêuticas - Fundação de desenvolvimento da pesquisa (FUNDEP / UFMG) - 2013
Foi realizado o teste de determinação de água em um lote de comprimidos empregando o método volumétrico (Karl Fischer). Para a análise foram utilizados 0,1432 g do pó dos comprimidos e foram gastos 1,23 mL do reagente de Karl Fischer. Considerando que o título do reagente de Karl Fischer seja 4,9032 mg/mL, qual é a porcentagem de água encontrada nessa amostra?
- A. 6,03%.
- B. 3,55%.
- C. 5,50%.
- D. 4,21%.
Considere as seguintes afirmativas sobre o teste Determinação de Volume, e assinale V (VERDADEIRO) ou F (FALSO).
( ) O teste é requerido para produtos líquidos em recipientes para doses múltiplas e produtos líquidos em recipientes para dose única.
( ) O teste se aplica tanto a preparações líquidas quanto a preparações líquidas obtidas a partir de pós para reconstituição.
( ) O teste não se aplica a produtos líquidos injetáveis acondicionados em recipientes como ampolas e frascosampola.
A alternativa que contém a sequência CORRETA é:
- A. V, V, F.
- B. V, F, V.
- C. F, F, V.
- D. F, V, F.
Sobre o teste de dissolução, é INCORRETO afirmar:
- A. o aparelho deve ser isento de qualquer fonte de vibração que possa influir na hidrodinâmica do sistema.
- B. as amostras não devem flutuar no meio de dissolução.
- C. as alíquotas para análise podem ser retiradas de qualquer região da cuba contendo o meio de dissolução.
- D. as alíquotas devem ser imediatamente filtradas após sua coleta.
O teste de dissolução foi realizado para um lote de comprimidos contendo 20 mg do fármaco A. As condições do teste estão descritas abaixo:
- Meio de dissolução: ácido clorídrico 0,1 M, 900 mL
- Aparelhagem: pá, 50 rpm
- Tempo: 45 minutos
- Procedimento: após o teste, retirar alíquota do meio de dissolução, filtrar e medir as absorvâncias das soluções em 255 nm sem realizar diluição.
Considerando que a absortividade específica (A 1%, 1 cm) do fármaco A, nas condições do teste, seja 480 e a leitura de absorvância da amostra da primeira cuba seja 0,850, qual a porcentagem de cedência dessa primeira amostra?
- A. 88,5%.
- B. 85,0%.
- C. 76,5%.
- D. 79,8%.
Assinale a alternativa que contém a correlação INCORRETA entre o medicamento e os testes de controle de qualidade requeridos.
- A. Ampicilina cápsulas 500 mg dissolução, uniformidade de doses unitárias e friabilidade.
- B. Metronidazol solução injetável 500 mg/100 mL pH, esterilidade, endotoxinas bacterianas.
- C. Acetato de dexametasona creme 1 mg/g determinação de peso, contagem microbiana e pesquisa de patógenos.
- D. Glicose solução injetável 50 g/100ml determinação de volume, pH, contaminação por partículas.
Suponha que o laboratório de controle de qualidade coordenado por você tenha recebido uma amostra de Atenolol insumo farmacêutico ativo para a realização do teste Cinzas Sulfatadas. O procedimento realizado foi o seguinte: um cadinho de porcelana foi calcinado, esfriado em dessecador, pesado (10,4568 g) e tarado. A seguir, 1,2543 g da amostra foram pesados. Adicionou-se 1 mL de ácido sulfúrico e aqueceu-se brandamente até carbonização em temperatura não superior a 600 oC. Esfriou-se, sendo adicionado 1 mL de ácido sulfúrico para umedecer o resíduo. Procedeu-se à carbonização e incineração com aquecimento gradativo até 600 oC.O cadinho foi esfriado, pesado novamente e incinerado por mais 30 minutos. Esse procedimento foi repetido até que a diferença entre duas pesagens sucessivas não fosse maior que 0,5 mg. O peso final do cadinho foi 10,4595 g. Qual é a porcentagem de cinzas sulfatadas em relação à substância sob ensaio?
- A. 0,1%.
- B. 0,3%.
- C. 0,4%.
- D. 0,2%.
Analise as seguintes afirmativas sobre os parâmetros de validação.
I. Seletividade é a capacidade que o método possui de medir exatamente um composto em presença de outros componentes tais como impurezas, produtos de degradação e componentes da matriz.
II. Linearidade é a capacidade de um método analítico de demonstrar que os resultados obtidos são diretamente proporcionais à concentração do analito na amostra, dentro de um intervalo especificado.
III. Limite de detecção é a menor quantidade do analito em uma amostra que pode ser determinada com precisão e exatidão aceitáveis sob as condições experimentais estabelecidas.
IV. Precisão é a proximidade dos resultados obtidos pelo método em estudo em relação ao valor verdadeiro.
Com base nas afirmativas, conclui-se que- A. apenas as afirmativas I e II estão corretas.
- B. apenas as afirmativas II e III estão corretas.
- C. apenas as afirmativas I e III estão corretas.
- D. apenas as afirmativas I, II e IV estão corretas.
A robustez de um método analítico é a medida de sua capacidade em resistir a pequenas e deliberadas variações dos parâmetros analíticos. Os seguintes parâmetros devem ser avaliados em um método que emprega cromatografia líquida de alta eficiência, EXCETO:
- A. velocidade do gás de arraste.
- B. lotes ou fabricantes de colunas.
- C. pH da fase móvel.
- D. temperatura.


