Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
Em relação às soluções preparadas rotineiramente em laboratórios químicos e os respectivos procedimentos de preparo, julgue os itens a seguir.
Considere que, em um laboratório, existam dois frascos, A e B, contendo soluções de cloreto de sódio. Se as concentrações dessas soluções forem, respectivamente, iguais a 0,1 g/L e 0,1 % (p/v), as duas soluções possuirão a mesma concentração.
- C. Certo
- E. Errado
Com relação ao átomo de oxigênio, é correto afirmar que ele apresenta
- A.
eletronegatividade inferior à do carbono.
- B.
eletronegatividade inferior à do enxofre.
- C.
raio atômico inferior ao do carbono.
- D.
energia de ionização inferior à do carbono.
- E.
energia de ionização inferior à do enxofre.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
Em relação às soluções preparadas rotineiramente em laboratórios químicos e os respectivos procedimentos de preparo, julgue os itens a seguir.
Considere que em um laboratório haja 50 mL de solução aquosa de sulfato de amônio (NH4)2SO4 na concentração de 0,10 mol/L. Nessa situação, se forem adicionados 50 mL de água destilada a essa solução será produzida uma nova solução com concentração igual a 0,20 mol/L.- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
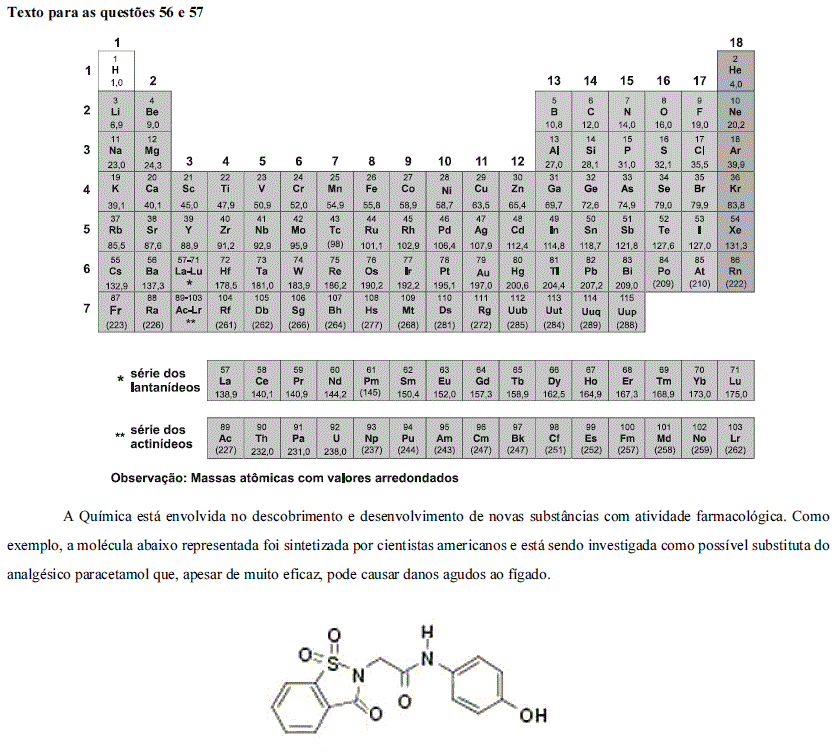
A respeito dos elementos que compõem a molécula apresentada, é correto afirmar que
- A.
pertencem a quatro diferentes períodos da tabela periódica.
- B.
três deles pertencem a um mesmo grupo da tabela periódica.
- C.
os elétrons de seus átomos neutros ocupam, no estado fundamental de energia, no máximo três níveis de energia.
- D.
há, pelo menos, um metal.
- E.
há, pelo menos, um halogênio.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
Em relação às soluções preparadas rotineiramente em laboratórios químicos e os respectivos procedimentos de preparo, julgue os itens a seguir.
Caso uma solução concentrada de ácido clorídrico apresente concentração de 38% (p/p), densidade igual a 1,2 g/mL, e considerando a massa molar do ácido clorídrico igual a 36,5 g/mol, então a concentração dessa solução em mol/L, será superior a 12 M.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
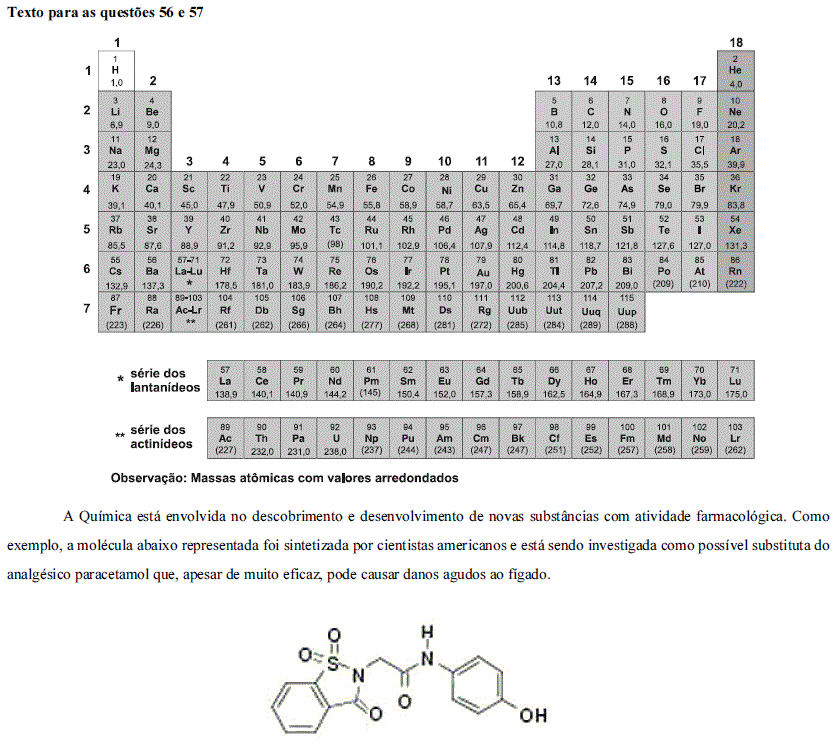
A julgar pela tabela periódica, é correto afirmar, com relação aos elementos que compõem a molécula apresentada, que os átomos neutros de carbono, enxofre, hidrogênio, nitrogênio e oxigênio apresentam, no estado fundamental de energia, respectivamente,
- A.
seis, oito, um, cinco e oito elétrons de valência.
- B.
quatro, seis, um, cinco e seis elétrons de valência.
- C.
cinco, sete, dois, seis e sete elétrons de valência.
- D.
quatro, oito, um, sete e oito elétrons de valência.
- E.
seis, dezesseis, um, sete e oito elétrons de valência.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
Em relação às soluções preparadas rotineiramente em laboratórios químicos e os respectivos procedimentos de preparo, julgue os itens a seguir.
A uma solução de 500 mL de ácido nítrico a 0,5 M, deve ser adicionado o volume de 750 mL de água para se obter solução com concentração final de ácido nítrico maior que 0,1 N.
- C. Certo
- E. Errado
A respeito das ligações químicas e dos estados de agregação da matéria, julgue os itens subsecutivos.
As ligações π são realizadas em orbitais hibridizados do átomo central.
- C. Certo
- E. Errado
A respeito das ligações químicas e dos estados de agregação da matéria, julgue os itens subsecutivos.
De acordo com a teoria de ligação de valência de Linus Pauling, a ligação covalente ocorre quando há a sobreposição dos orbitais atômicos, que devem possuir, além de energias semelhantes, orientação adequada.
- C. Certo
- E. Errado
A respeito das ligações químicas e dos estados de agregação da matéria, julgue os itens subsecutivos.
O rompimento de uma ligação química poderá ocorrer por meio de um processo endotérmico ou exotérmico.
- C. Certo
- E. Errado


