Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Em uma separação de duas substâncias por cromatografia de camada fina, utilizaram-se uma placa recoberta com uma camada de alumina e, como fase móvel, hexano. Após certo tempo na câmara de desenvolvimento, a linha frente do hexano atingiu 5,0 cm, com os centros das manchas das duas substâncias separadas percorrendo respectivamente 2,5 e 4,0 cm. O valor mais aproximado para o Rf da substância mais polar é
- A.
0,5
- B.
0,6
- C.
0,8
- D.
1,3
- E.
2,0
A pressão final de uma determinada massa de um gás ideal, se triplicado seu volume e reduzida sua temperatura a 1/4 da original, torna-se
- A. 3/4 da pressão original.
- B. 4/3 da pressão original.
- C. doze vezes maior que a original.
- D. doze vezes menor que a original.
- E. (E) sete vezes menor que a original.
A ureia, (NH2)2CO, pertence à função química
- A.
aldeído.
- B.
amida.
- C.
amina.
- D.
álcool.
- E.
cetona.
A cromatografia líquida com fase reversa faz uso de uma fase estacionária apolar e de uma fase móvel polar. Esse tipo de cromatografia pode ser usado para separar
- A.
grandes moléculas, como as proteínas, em função da diferença nos seus tamanhos.
- B.
cátions inorgânicos que são trocados por outros, característicos da estrutura da coluna.
- C.
substâncias orgânicas que formam diferentes coeficientes de partição entre fase móvel e fase estacionária.
- D.
substâncias com diferentes graus de solubilidade na fase móvel, que se precipitarão seletivamente na fase estacionária.
- E.
íons, em função de diferentes capacidades de migração na fase móvel onde se aplica uma diferença de potencial elétrico.
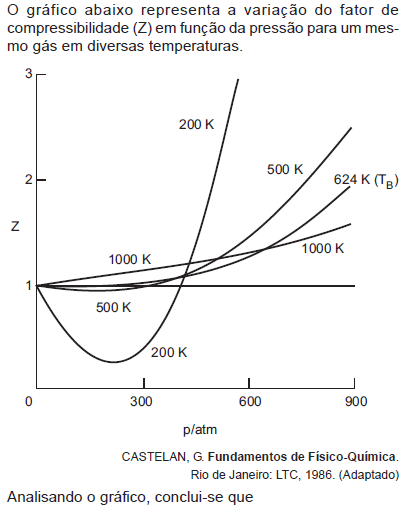
- A. à medida que se aumenta a temperatura, as forças atrativas são intensificadas.
- B. a 200 K, o gás se comporta como ideal numa faixa maior de pressões do que em qualquer outra temperatura.
- C. a 624 K, o gás se comporta como ideal numa faixa maior de pressões do que a 500K.
- D. a 1000 K, o gás se comporta como ideal para todas as pressões acima de 600 atm.
- E. a 600 atm, o gás se afasta mais da idealidade a 1000 K do que a 500 K.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação Carlos Chagas (FCC) - 2011
Considere:
I. bronze.
II. bromo.
III. ouro.
IV. gás carbônico.
V. ar.
VI. granito.
Pertencem ao grupo das substâncias puras
- A.
bromo, ouro e gás carbônico.
- B.
bronze, ouro e granito.
- C.
bromo, granito e gás carbônico.
- D.
ar, bronze e gás carbônico.
- E.
ar, ouro e gás carbônico.
Um técnico recebeu a incumbência de neutralizar uma solução de ácido sulfúrico com solução de hidróxido de sódio. Como não dispunha da solução de hidróxido de sódio, substituiu-a por outra da mesma função química. A solução utilizada pelo técnico foi
- A.
CO2
- B.
HCl
- C.
NH4Cl
- D.
HC2H3O2
- E.
Ca(OH)2
os cloretos atuam como ácido, enquanto as aminas atuam como base no composto conhecido como cisplatina, [Pt(NH3)2Cl2].
- A. Sim, sendo que o ácido nítrico atua como uma base recebendo um próton.
- B. Sim, sendo que o equilíbrio estará deslocado no sentido do ácido mais forte.
- C. Sim, sendo que o ácido sulfúrico atua como uma base recebendo um próton.
- D. Não, pois ambos os compostos são classificados como ácidos.
- E. Não, pois ambos os compostos são substâncias oxidantes.
Ao iniciar o ensino das transformações químicas, o professor deve considerar que
- A.
todas as transformações químicas são perceptíveis.
- B.
a utilização de experimentos dificulta o entendimento do conceito, pois o aluno não domina os modelos atômicos.
- C.
a representação das equações químicas deve ser o ponto de partida.
- D.
as transformações químicas só podem ser entendidas após o estudo dos modelos atômicos.
- E.
interações entre materiais e energia devem ser consideradas, além da formação de novas substâncias.

- A.
v = K.[A].[B]
- B.
v = K.[A]2.[B]
- C.
v = K.[A].[B]2
- D.
v = K.[A]2.[B]3
- E.
v = K.[A]3.[B]2


