Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação de Estudos e Pesquisas Sócio-Econômicos (FEPESE) - 2011
As substâncias orgânicas que apresentam coloração característica, de acordo com meio em que se encontram, são chamadas de:
- A.
Reatores.
- B.
Indicadores.
- C.
Credenciadores.
- D.
Aspersores.
- E.
Absolutos.

Tendo como base a reação acima e os gases nela envolvidos e considerando, ainda, que ln 0,7 = -0,357, julgue os itens seguintes.
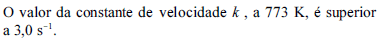
- C. Certo
- E. Errado
Atenção: Considere as seguintes reações de combustão do metano, para responder às questões de números 35 e 36.
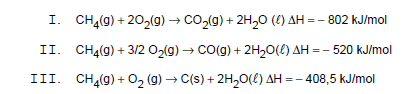
É produzido um gás estufa e um composto venenoso para os seres humanos, respectivamente, nas reações representadas em
- A.
I e II.
- B.
I e III.
- C.
II e III.
- D.
II e I.
- E.
III e II.
A leitura de parâmetros no espectrofotômetro está baseada na lei de:
- A.
Preti.
- B.
Tompson.
- C.
Beer-Lambert.
- D.
Lavoisier.
- E.
Pasteur.

Tendo como base a reação acima e os gases nela envolvidos e considerando, ainda, que ln 0,7 = -0,357, julgue os itens seguintes.

- C. Certo
- E. Errado
No controle da hiperacidez estomacal pode-se utilizar uma solução de comprimido antiácido contendo carbonato e bicarbonato. Nessa solução encontram-se os equilíbrios representados pelas seguintes equações:
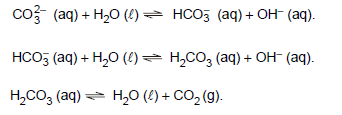
Quando ingerida, essa solução reage com o ácido estomacal e, como consequência, ocorre
- A.
aumento da concentração de íons CO32- (aq).
- B.
desidratação estomacal.
- C.
aumento da concentração de íons H+ (aq).
- D.
liberação de gás.
- E.
diminuição do pH dentro do estômago.
Química - Práticas Laboratoriais em química - Fundação de Estudos e Pesquisas Sócio-Econômicos (FEPESE) - 2011
É correto afirmar sobre o turbidímetro.
- A.
Funciona segundo o princípio Nefelométrico.
- B.
Resultado é expresso em miligramas por litro.
- C.
Leitura está baseada na intensidade de potência mecânica da amostra.
- D.
Imperfeições na cubeta de vidro facilitam a interpretação da correta leitura.
- E.
Presença de detritos e materiais grosseiros que decantam rápido, não interfere no resultado.

Tendo como base a reação acima e os gases nela envolvidos e considerando, ainda, que ln 0,7 = -0,357, julgue os itens seguintes.

- C. Certo
- E. Errado
A obtenção do sal da água do mar se dá pela retirada do sal sólido à medida que evapora a água do mar contida em grandes tanques. Nesse processo é obtido sal com teor de mais de 95% em NaCl. Esse alto teor de NaCl é possível porque
- A.
a água do mar tem esse teor de NaCl.
- B.
o NaCl é obtido por cristalização fracionada.
- C.
a temperatura de ebulição da água é maior que a do NaCl.
- D.
a densidade do NaCl é maior que a da água.
- E.
a temperatura de fusão da água é maior que a do NaCl.
Química - Práticas Laboratoriais em química - Fundação de Estudos e Pesquisas Sócio-Econômicos (FEPESE) - 2011
No laboratório o uso da capela é indicado na manipulação de:
- A.
Pipetas novas.
- B.
Água deionizada.
- C.
Areias e siltes inertes.
- D.
Frascos vazios limpos.
- E.
Solventes voláteis, tóxicos e reações perigosas.


