Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Deseja-se reaproveitar o enxofre sólido para um estudo, gerado através da seguinte reação:
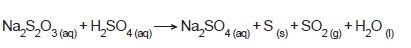
Qual é o método adequado para separar o enxofre sólido da mistura heterogênea do tipo sólido-líquido formada?
- A.
Filtração
- B.
Peneiração
- C.
Condensação
- D.
Destilação fracionada
- E.
Dissolução fracionada
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2009

Tendo como referência as informações apresentadas acima, julgue os itens de 57 a 61.
Suponha que, durante a determinação, em triplicata, da dureza de Mg 2+ e Ca 2+ em uma amostra de água por complexometria, ocorra interferência de íons Fe 2+ . Nessa situação, é correto afirmar que, desconsiderados outros erros, a citada interferência causará uma falta de exatidão do valor médio obtido.
- C. Certo
- E. Errado
O metano (CH4), um gás inodoro e incolor, é um dos principais constituintes do gás natural. A combustão completa do metano é representada por esta equação química:
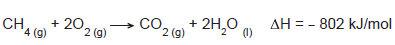
Tendo como base esses dados, assinale a afirmação correta.
- A.
O CH4 é um hidrocarboneto da família dos alcanos e sua molécula é apolar.
- B.
O gás natural é também conhecido e comercializado como Gás Liquefeito de Petróleo (GLP).
- C.
A emissão de CH4 para a atmosfera ajuda a combater o efeito estufa, em virtude da sua alta capacidade de absorção de radiação infravermelha (calor).
- D.
É necessário o fornecimento de 802 kJ/mol de energia para a reação ocorrer.
- E.
São produzidos 440 kg de CO2 a partir da queima de 22,4 L de CH4, nas CNTP.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2009

Tendo como referência as informações apresentadas acima, julgue os itens de 57 a 61.
Se a dureza de Mg 2+ e Ca 2+ em uma amostra de água foi determinada realizando-se a titulação complexométrica de 50,0 mL dessa amostra com uma solução de EDTA 0,0200 mol/L, se o ponto final da titulação foi detectado após a adição de 40,0 mL da solução titulante, e se forem desprezados eventuais erros experimentais, de titulação e devido à presença de interferentes, então é correto concluir que a concentração total de íons Mg 2+ e Ca 2+ na amostra de água em questão é maior do que 0,18 mol/L.
- C. Certo
- E. Errado
Um sistema de produção gera diariamente, como efluente, 5.000 litros de uma solução aquosa de amônia 0,5 M. A amônia é recuperada desse efluente por meio da reação com uma solução de ácido sulfúrico 1,25 M, formando sulfato de amônio como produto final, que é reutilizado como matéria-prima na planta de produção. A reação de recuperação da amônia é representada estequiometricamente pela equação a seguir.
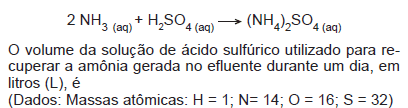
- A.
250
- B.
500
- C.
1000
- D.
1500
- E.
2000
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2009

Tendo como referência as informações apresentadas acima, julgue os itens de 57 a 61.
Os dados da tabela permitem concluir que a constante de equilíbrio para a formação do complexo do EDTA com o Ca 2+ é menor do que para o complexo desse mesmo ligante com o Mg 2+ .
- C. Certo
- E. Errado
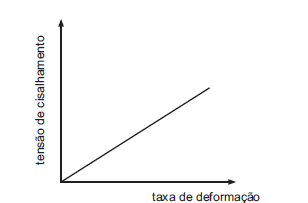
O gráfico acima descreve o comportamento reológico de um fluido
- A.
plástico.
- B.
pseudoplástico.
- C.
Plástico de Bingham.
- D.
newtoniano.
- E. dilatante.
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2009
Durante a realização de um procedimento analítico, um químico necessitou efetuar a transferência de determinada quantidade de um líquido L. Para isso, ele utilizou uma pipeta volumétrica previamente calibrada por meio da pesagem da massa de água destilada que por ela é transferida. Com relação à situação hipotética acima, julgue os itens que se seguem.
Considere que o químico tenha utilizado, nos cálculos do volume da pipeta, a densidade da água correspondente a uma temperatura diferente daquela do laboratório no momento da realização do procedimento. Nesse caso, o erro cometido pelo químico ao utilizar a pipeta para a transferência do líquido L consistirá em um erro aleatório.
- C. Certo
- E. Errado
Um técnico utilizou um método de análise química cuja principal operação consistiu em adicionar lentamente uma solução a outra, até a completa reação entre seus solutos, com a finalidade de determinar a concentração de uma das soluções, a partir da concentração já conhecida da outra solução. Trata-se do método denominado
- A.
Turbidimetria
- B.
Voltametria
- C.
Volumetria
- D.
Gravimetria.
- E.
Potenciometria.
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2009
Durante a realização de um procedimento analítico, um químico necessitou efetuar a transferência de determinada quantidade de um líquido L. Para isso, ele utilizou uma pipeta volumétrica previamente calibrada por meio da pesagem da massa de água destilada que por ela é transferida. Com relação à situação hipotética acima, julgue os itens que se seguem.
Se a calibração da balança analítica utilizada na pesagem da água transferida pela pipeta foi realizada com um peso padrão, cuja densidade é igual a 8,0 g/mL, e se não foi efetuada nenhuma correção relativa aos efeitos do empuxo do ar atmosférico, é correto concluir que a massa real de água transferida era menor do que o valor lido na balança.
- C. Certo
- E. Errado


