Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Eletrólitos são substâncias que dissolvidas em água produzem íons em solução, os quais possuem a capacidade de conduzir corrente elétrica. Entre essas substâncias, encontram-se as bases fortes e os sais solúveis originários dessas bases. Assinale a alternativa que apresenta somente tais substâncias.
- A.
H3CCOOH, H2S, NaCl
- B.
NaCl, C6H12O6, Fe(OH)3
- C.
NaOH, KCl, NaNO3
- D.
NaNO3, HCN, C6H12O6
- E.
BaSO4, H2S, NaCl
De modo a caracterizar o estado termodinâmico de uma substância pura deve-se conhecer o valor de duas propriedades termodinâmicas. Nessa perspectiva, está correto afirmar que as duas variáveis que são definidas como propriedades termodinâmicas são:
- A.
calor e trabalho.
- B.
calor e energia interna.
- C.
calor e entropia.
- D.
entalpia e entropia.
- E.
trabalho e entalpia.
O volume, em mL, de ácido clorídrico concentrado necessário para se preparar um litro de uma solução com concentração final de 0,6 mol.L−1 é:

- A. 0,05
- B. 0,50
- C. 5,00
- D. 5,50
- E. 50,0
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2006
Com relação a conceitos de química, julgue os itens seguintes.
Iguais quantidades de matéria de oxigênio, hidrogênio, nitrogênio e flúor apresentam diferentes valores de massa.
- C. Certo
- E. Errado
A medida de pH é freqüentemente realizada através do uso do eletrodo de vidro. Assinale a alternativa que corresponde a uma das possíveis fontes de erro nesse tipo de medida.
- A.
Efeito alcalino
- B.
Desvio padrão
- C.
Ponte salina
- D.
Membrana metálica
- E.
Intervalo de confiança
O cobre pode ser obtido a partir da reação da calcosita (Cu2
com a cuprita (Cu2 O), conforme a reação abaixo.
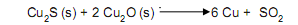
Ao reagir 260g de cuprita contendo 45% de impureza
com calcosita suficiente, foram obtidos 152,4g de cobre.
O rendimento da reação foi de:
(Dados - Massa molares: Cu = 63,5g/mol; S = 32 g/mol;
O = 16 g/mol)
- A.
100%
- B.
95%
- C.
90%
- D.
80%
- E.
75%
Numa estação de tratamento de esgoto, utiliza-se o processo de tratamento com lodo ativado visando
- A. a degradação da matéria orgânica oxidável.
- B. a floculação de partículas coloidais.
- C. a remoção dos sólidos suspensos.
- D. o aumento da demanda bioquímica de oxigênio.
- E. a eliminação dos microorganismos patogênicos.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2006
Com relação a conceitos de química, julgue os itens seguintes.
A presença de contaminantes, propositais ou não, em bebidas pode alterar suas propriedades físicas e químicas. Por exemplo, a temperatura de fusão de um refrigerante abaixa à medida que diminui a concentração de determinado soluto que o compõe, considerando que apenas o solvente muda de fase.
- C. Certo
- E. Errado
Espectrofotometria é a técnica que utiliza luz para medir concentrações de espécies químicas. Considerando esse assunto, numere a coluna da direita com base nas informações da coluna da esquerda.
- A.
5, 2, 3, 4, 1.
- B.
3, 1, 4, 5, 2.
- C.
2, 5, 4, 1, 3.
- D.
2, 4, 5, 3, 1.
- E.
1, 4, 5, 2, 3.
A mistura de pó de alumínio, perclorato de amônio e óxido de ferro III é utilizada como combustível sólido na impulsão dos foguetes de lançamento do ônibus espacial. Uma das reações que ocorrem quando essa mistura é inflamada está representada na equação não balanceada abaixo. A respeito dessa reação e das espécies envolvidas é correto afirmar que o(a):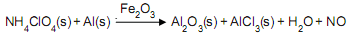
- A. Al sofre redução.
- B. NO é um óxido básico.
- C.
NH4
ClO4 é um sal oriundo de ácido forte e oxidante. - D.
Al2
O3 e o Fe2 O3 apresentam propriedades anfotéricas. - E.
soma dos coeficientes mínimos para essa equação é 15.


