Questões de Química do ano 2004
Lista completa de Questões de Química do ano 2004 para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.

Considerando as informações acima e sabendo que M(C) = 12 g/mol e M(H) = 1 g/mol, julgue os itens seguintes.
Considerando que o gás hidrogênio produzido na reação de síntese do tolueno tenha um comportamento distinto do previsto para gases ideais e que esse desvio possa ser medido pelo fator de compressão 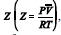 é correto afirmar que, caso esse gás tenha Z > 1, então as forças repulsivas não estarão atuando entre as moléculas desse gás.
é correto afirmar que, caso esse gás tenha Z > 1, então as forças repulsivas não estarão atuando entre as moléculas desse gás.
- C. Certo
- E. Errado

Considerando as informações acima e sabendo que M(C) = 12 g/mol e M(H) = 1 g/mol, julgue os itens seguintes.
A molécula indicada como molécula 2 é um peróxido.
- C. Certo
- E. Errado

Considerando as informações acima e sabendo que M(C) = 12 g/mol e M(H) = 1 g/mol, julgue os itens seguintes.
A estequiometria da reação de síntese do tolueno indica que para formar 1 mol de tolueno são necessários 1 mol de metil-ciclo-hexano e 1 mol do complexo Mo2O3 . Al2O3.
- C. Certo
- E. Errado

Considerando as informações acima e sabendo que M(C) = 12 g/mol e M(H) = 1 g/mol, julgue os itens seguintes.
Considerando que a velocidade média das moléculas do gás carbônico a 25 oC seja igual a 410 m/s, é correto afirmar que todas as moléculas do gás carbônico a 25 oC percorrem 410 metros em um segundo.
- C. Certo
- E. Errado

Considerando as informações acima e sabendo que M(C) = 12 g/mol e M(H) = 1 g/mol, julgue os itens seguintes.
Nas reações de combustão, o número de oxidação dos átomos que compõem as moléculas do gás oxigênio é reduzido, o que torna o gás oxigênio um agente redutor.
- C. Certo
- E. Errado

Considerando as informações acima e sabendo que M(C) = 12 g/mol e M(H) = 1 g/mol, julgue os itens seguintes.
A combustão de 16 g de metano transfere 8 elétrons para 4 mols de átomos de oxigênio.
- C. Certo
- E. Errado
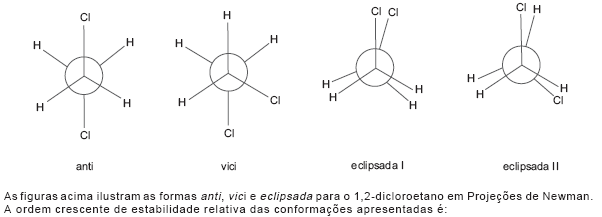
- A.
anti < vici < eclipsada I < eclipsada II.
- B.
anti < vici < eclipsada II < eclipsada I.
- C.
eclipsada I < eclipsada II < vici < anti.
- D.
eclipsada II < eclipsada I < anti < vici.
- E.
vici < anti < eclipsada I < eclipsada II.
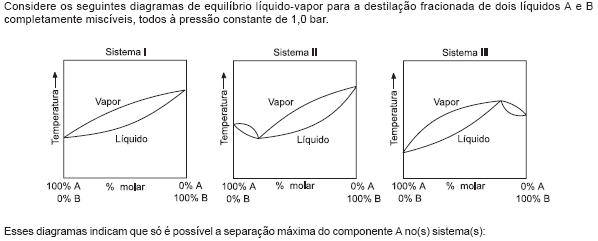
- A.
I, devido aos sucessivos ciclos de vaporização-condensação.
- B.
II, pois o ponto de ebulição de A é menor que o da mistura azeotrópica
- C.
III, pois o ponto de ebulição de B é maior que o da mistura azeotrópica.
- D.
I e II, pois o azeótropo formado é de mínima temperatura de ebulição.
- E.
I e III, pois o azeótropo formado é de máxima temperatura de ebulição.
Considere as espécies abaixo. 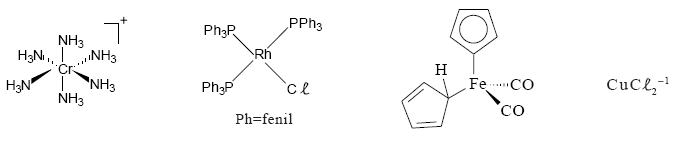 A geometria do composto organometálico é:
A geometria do composto organometálico é:
- A.
tetraédrica.
- B.
octaédrica.
- C.
linear.
- D.
tetragonal planar.
- E.
pirâmide de base quadrada.
Para avaliar o nível de poluição de um curso d'água, foram analisadas amostras coletadas em seis pontos distintos desse rio. Os resultados obtidos para oxigênio dissolvido (OD), demanda bioquímica de oxigênio (DBO) e demanda química de oxigênio (DQO) estão apresentados nos gráficos abaixo. 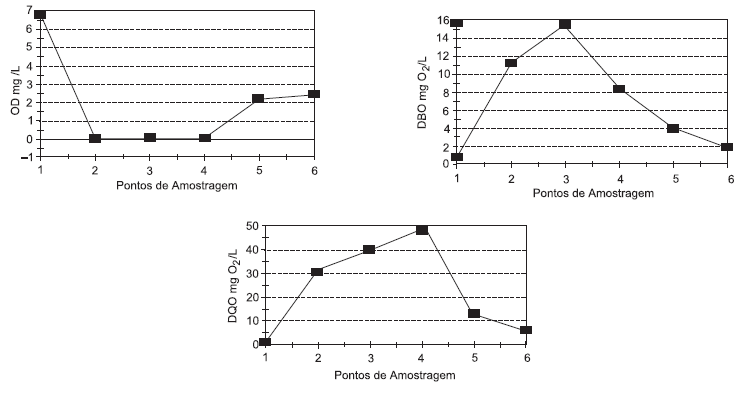 Os resultados dessas análises indicam que:
Os resultados dessas análises indicam que:
- A.
a amostra coletada no ponto 4 apresentou maior contribuição de poluição biodegradável e não biodegradável.
- B.
a contaminação sofrida pelo rio é causada apenas por material não biodegradável.
- C. a soma DBO + DQO expressa a demanda de O2 necessária para eliminar todo o material oxidável presente na água.
- D.
o ponto de amostragem correspondente à maior poluição biodegradável é o de número 3.
- E.
os pontos de amostragem de números 2, 3 e 4 são igualmente poluídos.


