Questões de Química do ano 2004
Lista completa de Questões de Química do ano 2004 para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Em áreas de baixo índice pluviométrico, os solos podem se tornar muito alcalinos devido à presença de sais com caráter básico como o Na2CO3. Nesses casos, o ajuste do pH do solo deve ser feito através de um processo de hidrólise, com a adição de:
- A.
Fe2(SO4)3
- B.

- C.

- D.
NaNO3
- E.


Esse texto fica correto quando as lacunas I, II e III são preenchidas, respectivamente, por
- A.
éteres − vinagres − hidrocarbonetos
- B.
ésteres − sabões − hidrocarbonetos
- C.
ésteres − vinagres − éteres
- D.
éteres − sabões − hidrocarbonetos
- E.
ésteres − sabões − éteres
Dentre os seguintes poluentes do ar, o que está mais diretamente relacionado à formação de chuva ácida é o
- A.
metano
- B.
monóxido de carbono.
- C.
diclorodiflúormetano.
- D.
isooctano.
- E.
dióxido de nitrogênio.
As questões de números 49 a 51 referem-se ao experimento descrito a seguir.

Supondo que a massa média do sólido resultante das massas obtidas por diferença (procedimento IV) por todos os grupos de alunos foi de 1,2 g e que o sólido formado seja totalmente insolúvel, conclui-se que essa média, em relação à massa prevista teoricamente, está portanto
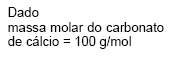
- A.
0,2 g acima.
- B.
0,4 g acima.
- C.
igual.
- D.
0,2 g abaixo.
- E.
0,4 g abaixo.
As questões de números 49 a 51 referem-se ao experimento descrito a seguir.

Considerando a temperatura de 25 graus Celsius, a solução de carbonato de sódio utilizada no experimento é
- A.
ácida e portanto tem pH maior do que 7,0.
- B.
ácida e portanto tem pH menor do que 7,0.
- C.
neutra e portanto tem pH igual a 7,0.
- D.
básica e portanto tem pH maior do que 7,0.
- E.
básica e portanto tem pH menor do que 7,0.
As questões de números 49 a 51 referem-se ao experimento descrito a seguir.

Considerando uma classe com 10 grupos de alunos, a massa de CaCl2.6H2O que o professor deve utilizar para preparar todo o volume necessário da solução de cloreto de cálcio é

- A.
2,19 g
- B.
11,1 g
- C.
21,9 g
- D.
111 g
- E.
219 g
Um professor propôs a seus alunos que confeccionassem um cartaz ilustrativo sobre os usos das frações da destilação do petróleo. Um grupo de alunos fez o seguinte: desenhou um esquema de torre de fracionamento e selecionou as fotografias indicadas a seguir para ilustrá-lo:
Foto I − um avião a jato sendo abastecido de combustível;
Foto II − asfalto e piche sendo utilizados para pavimentar uma estrada;
Foto III − um botijão de gás doméstico;
Foto IV − uma lata de óleo lubrificante.
A ordem em que essas fotos devem ser coladas no cartaz, da região de maior temperatura (parte inferior da torre) para a de menor temperatura é
- A.
I, II, III e IV.
- B.
I, III, IV e II.
- C.
II, III, IV e I.
- D.
II, IV, I e III.
- E.
II, I, IV e III.
Suponha que os alunos de determinada série estejam iniciando seus estudos sobre o átomo e que tenham conhecimento sobre a teoria atômica de Dalton. Com isso, já podem explicar, no nível microscópico, diversos fatos experimentais como, por exemplo:
- A.
Soluções aquosas iônicas são boas condutoras de eletricidade."
- B.
Quando sal de cozinha cai em um queimador de fogão aceso, a chama fica amarela."
- C.
A emulsão de um filme fotográfico sofre transformação quando atingido pela luz."
- D.
"Minérios de urânio emitem espontaneamente radiações."
- E.
Nas transformações químicas há conservação de massa."
O gráfico abaixo expressa a variação no nível médio da concentração de dióxido de carbono na atmosfera em umSão, respectivamente, causa e conseqüência dessa variação período de 30 anos.

São, respectivamente, causa e consequência dessa variação
- A.
decomposição anaeróbica de material orgânico e destruição da camada de ozônio.
- B.
demanda energética associada à queima de combustíveis fósseis e aquecimento global.
- C.
demanda bioquímica de oxigênio e inversão térmica.
- D.
decomposição aeróbica de material inorgânico e aquecimento global.
- E.
demanda energética associada ao desflorestamento e destruição da camada de ozônio.
Tendo o assunto abordado no texto acima por referência, julgue os itens subseqüentes.
O polysiloxane não reage com dióxido de titânio.
- C. Certo
- E. Errado


