Questões de Química do ano 2011
Lista completa de Questões de Química do ano 2011 para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Todos os elementos de um mesmo grupo da tabela periódica apresentam, na forma não ionizada, o mesmo número de elétrons de valência.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Nas primeiras versões da tabela periódica, antes da descoberta da massa atômica, o ordenamento dos elementos era feito com base nos números atômicos.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
De acordo com a teoria das ligações de valência, a maior parte dos gases nobres é capaz de formar compostos moleculares, uma vez que podem sofrer expansão da sua camada de valência.
- C. Certo
- E. Errado
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Dois átomos que apresentem o mesmo número atômico mas diferentes números de nêutrons são elementos químicos diferentes.
- C. Certo
- E. Errado
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Os elementos químicos pertencentes ao grupo dos halogênios caracterizam-se por serem os que apresentam as mais elevadas energia de ionização e eletronegatividade.
- C. Certo
- E. Errado
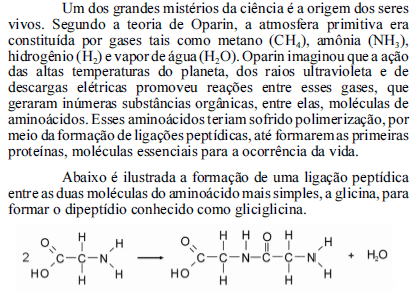
Considerando as massas atômicas do O, N, C e H como iguais a 16,0 g/mol; 14,0 g/mol; 12,0 g/mol e 1,0 g/mol, respectivamente, julgue os itens de 111 a 115, acerca dos fenômenos e substâncias envolvidos na teoria de Oparin para a origem da vida na Terra.
A separação dos gases acima citados como constituintes da atmosfera primitiva pode ser feita por meio da condensação fracionada.
- C. Certo
- E. Errado
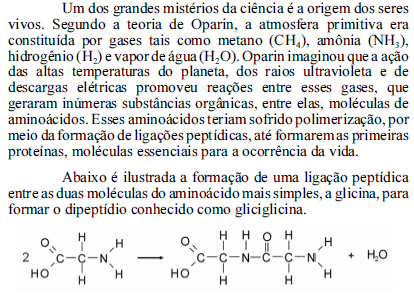
Considerando as massas atômicas do O, N, C e H como iguais a 16,0 g/mol; 14,0 g/mol; 12,0 g/mol e 1,0 g/mol, respectivamente, julgue os itens de 111 a 115, acerca dos fenômenos e substâncias envolvidos na teoria de Oparin para a origem da vida na Terra.
A atmosfera primitiva acima descrita pode ser considerada uma mistura heterogênea.
- C. Certo
- E. Errado
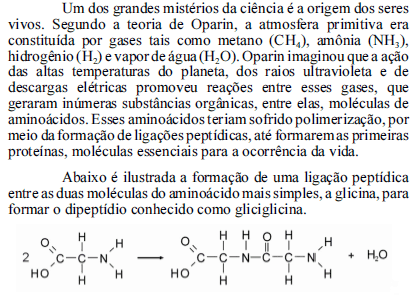
Considerando as massas atômicas do O, N, C e H como iguais a 16,0 g/mol; 14,0 g/mol; 12,0 g/mol e 1,0 g/mol, respectivamente, julgue os itens de 111 a 115, acerca dos fenômenos e substâncias envolvidos na teoria de Oparin para a origem da vida na Terra.
A reação de 300 g de glicina forma uma quantidade de gliciglicina inferior a 280 g.
- C. Certo
- E. Errado
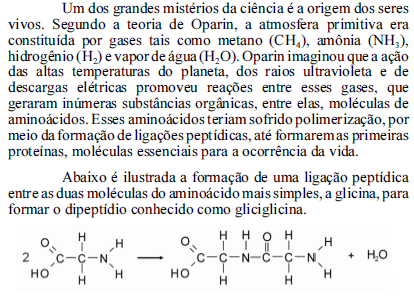
Considerando as massas atômicas do O, N, C e H como iguais a 16,0 g/mol; 14,0 g/mol; 12,0 g/mol e 1,0 g/mol, respectivamente, julgue os itens de 111 a 115, acerca dos fenômenos e substâncias envolvidos na teoria de Oparin para a origem da vida na Terra.
A condensação da água ocorre em temperaturas superiores às necessárias para a condensação do metano, da amônia e do hidrogênio, porque as ligações químicas O) H são mais fortes que as ligações N) H, C) H e H) H.
- C. Certo
- E. Errado
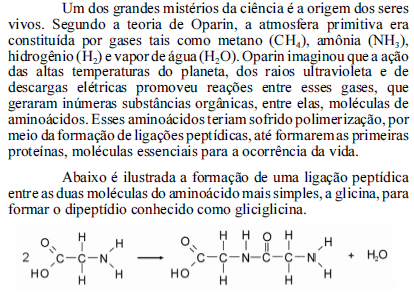
Considerando as massas atômicas do O, N, C e H como iguais a 16,0 g/mol; 14,0 g/mol; 12,0 g/mol e 1,0 g/mol, respectivamente, julgue os itens de 111 a 115, acerca dos fenômenos e substâncias envolvidos na teoria de Oparin para a origem da vida na Terra.
Entre as quatro substâncias químicas apresentadas no texto como constituintes da atmosfera primitiva, três delas são substâncias compostas.
- C. Certo
- E. Errado


