Questões de Química do ano 2012
Lista completa de Questões de Química do ano 2012 para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
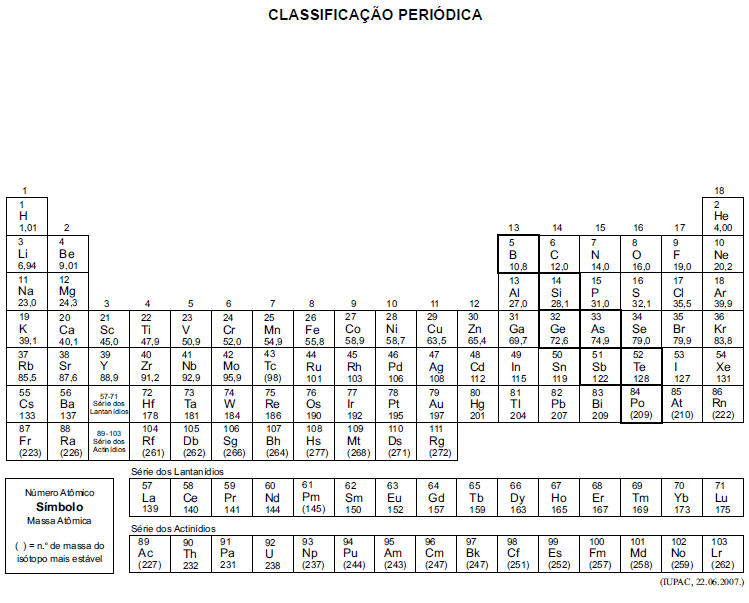
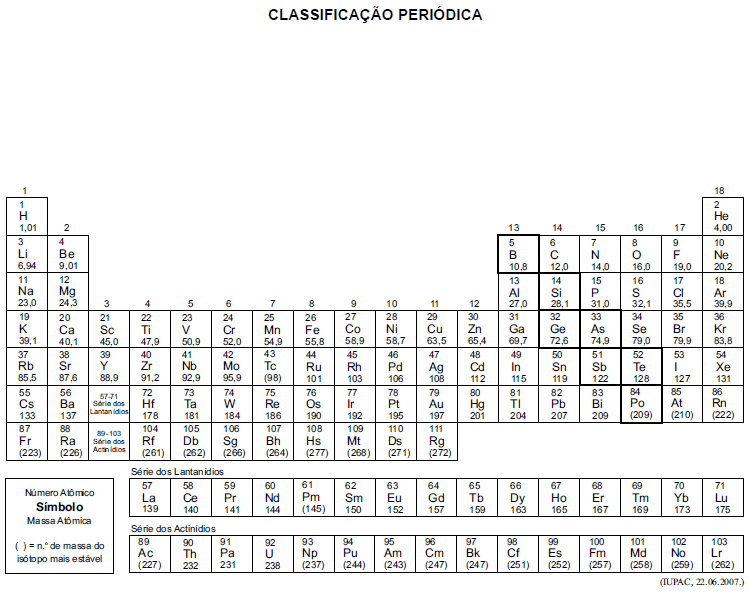
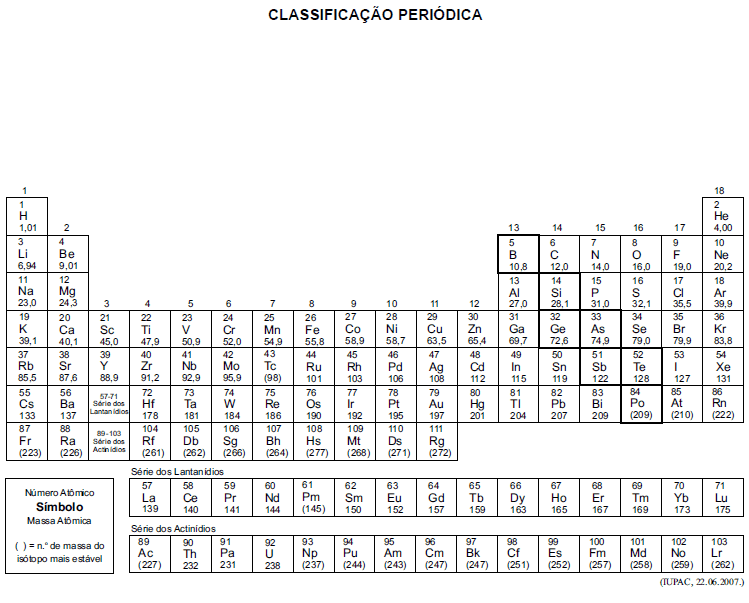
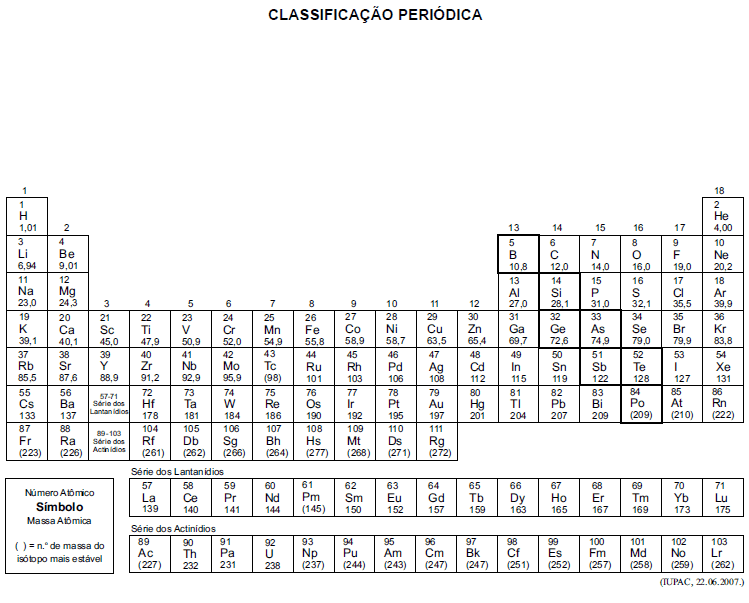
A tabela periódica encontra-se no final deste caderno.
Práticas agrícolas que envolvem desmatamento em larga escala, bem como o uso indiscriminado de praguicidas e fertilizantes, acarretam perturbações no ciclo natural
I. da água;
II. do nitrogênio;
III. do carbono.
Está correto o que se afirma em
- A.
I, apenas.
- B.
II, apenas.
- C.
I e II, apenas.
- D.
II e III, apenas.
- E.
I, II e III.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
No refino do petróleo, o aumento da quantidade de gasolina pode ser conseguido por processos que envolvem transformações como as exemplificadas a seguir:
1. C16H34 → C8H16 + C8H18
2. C4H10 + C4H8 → C8H18
As transformações 1 e 2 exemplificam, correta e respectivamente, os processos conhecidos como
- A.
craqueamento e alquilação.
- B.
craqueamento e hidrogenação.
- C.
hidrogenação e alquilação.
- D.
alquilação e hidrogenação.
- E.
alquilação e craqueamento.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
Dois açúcares presentes na alimentação humana são a glicose e a frutose, cuja fórmula molecular é a mesma: C6H12O6. Esses dois açúcares são:
I. hexoses;
II. isômeros entre si;
III. poliidroxialdeídos.
Está correto o que se afirma apenas em
- A.
I.
- B.
II.
- C.
III.
- D.
I e II.
- E.
II e III.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
A 25 ºC, o produto iônico da água, Kw , é igual a 1 x 1014. Nessa temperatura, o papel de tornassol azul torna-se vermelho em soluções aquosas cujo pH é inferior a 5 e o papel de tornassol vermelho torna-se azul em soluções aquosas cujo pH é superior a 8. Esses dois papéis manterão sua cor inalterada, caso sejam imersos em uma solução aquosa em que a concentração de íons OH , em mol, por litro, seja igual a
- A.
1 x 1011.
- B.
1 x 1010.
- C.
1 x 108.
- D.
1 x 105.
- E.
1 x 103.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
A água do mar é fonte natural para a obtenção industrial de várias substâncias, entre elas:
I. soda cáustica;
II. cloro;
III. magnésio;
IV. cloreto de sódio.
Processos químicos eletrolíticos são empregados para a obtenção do contido em
- A.
I e IV, apenas.
- B.
II e III, apenas.
- C.
II e IV, apenas.
- D.
I, II e III, apenas.
- E.
I, II, III e IV.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.

- A.
(CH3O2)+
- B.
H2O
- C.
(COH+
- D.
CO
- E.
H+
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
A primeira etapa do processo de obtenção industrial de nitrogênio e oxigênio, a partir do ar atmosférico ambiental, consiste em
- A.
resfriar o ar até a temperatura de zero kelvin.
- B.
aquecer o ar até a temperatura de 1 000 ºC.
- C.
remover do ar umidade, material particulado e CO2.
- D.
comprimir o ar até solidificá-lo completamente.
- E.
rarefazer o ar até pressões próximas do vácuo.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
Objetos de cobre expostos ao ar úmido adquirem uma coloração esverdeada devido à formação de carbonato básico de cobre, de acordo com a reação:
2 Cu (s) + H2O (l) + O2 (g) + CO2 (g) → Cu2(OH)2CO3 (s)
Nessa reação, as espécies redutora e oxidante são, correta e respectivamente,
- A.
a água e o cobre.
- B.
a água e o gás carbônico.
- C.
o oxigênio e o cobre.
- D.
o cobre e a água.
- E.
o cobre e o oxigênio.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
Considere as seguintes fontes de emissão de poluentes da água:
I. redes de efluentes domésticos;
II. deposições atmosféricas;
III. derramamentos acidentais;
IV. práticas agrícolas.
São consideradas fontes não pontuais apenas
- A.
I e II.
- B.
I e III.
- C.
II e III.
- D.
II e IV.
- E.
III e IV.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.

- A.
mole.
- B.
moderadamente mole.
- C.
levemente dura.
- D.
dura.
- E.
muito dura.


