Questões de Química do ano 2014
Lista completa de Questões de Química do ano 2014 para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Instituto de Estudos Superiores do Extremo Sul (IESES) - 2014
O número total de elétrons no ânion Y-2 é 19 e o seu número de massa é 34. O número de nêutrons do elemento Y vale:
- A. 15
- B. 16
- C. 17
- D. 20
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2014
A cromatografia é uma técnica de separação. Fundamentalmente, um fluido contendo um conjunto de substâncias dissolvidas (fase móvel) passa através de um solido ou um líquido adsorvido no sólido (fase estacionária). A cromatografia gasosa é uma das técnicas analíticas mais utilizadas. Entretanto, a grande limitação deste método é:
- A. Baixa resolução.
- B. Utiliza predominantemente fase estacionária sólida.
- C. Necessidade de que a amostra seja volátil ou estável termicamente.
- D. Não permite o acoplamento de espectrômetros de massa, limitando a identificação das substâncias.
- E. A CG de alta resolução só aceita fase estacionária polar polietileno glicol puro.
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2014
A informação gravimétrica reveste-se de primordial importância em diversas áreas das ciências da Terra, como por exemplo na Geodésia (estudo da forma -geóide- e dimensões da Terra), na Geologia (investigação de estruturas geológicas) e na Geofísica (prospecção mineral). A técnica gravimétrica onde o analito é separado de uma solução da amostra como um precipitado e é convertido a uma espécie de composição conhecida que pode ser pesada é chamada de:
- A. Gravimetria por precipitação.
- B. Gravimetria de volatilização.
- C. Eletrogravimetria.
- D. Titulação gravimétrica.
- E. Espectrometria de massas atômicas.
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2014
Dois métodos básicos são empregados para estabelecer a concentração de soluções padrão: o método direto (utiliza padrão primário) e o método da padronização (utiliza solução padrão secundário). A concentração de uma solução padrão secundário está sujeita a incertezas maiores que a da solução padrão primário. Então, se houver escolha, as soluções serão mais bem preparadas por meio do método direto. Supondo que se queira preparar 2,00 L de AgNO3 com concentração de 0,05 mol/L a partir de um sólido com grau padrão primário, a quantidade de AgNO3 a ser dissolvida será (Dados: Massa molar de AgNO3 = 169,87 g/mol)
- A. 1,698 g.
- B. 3,396 g.
- C. 169,8 g.
- D. 16,98 g.
- E. 33,96 g.
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2014
A recristalização é um método de purificação de compostos orgânicos que são sólidos à temperatura ambiente. O princípio deste método consiste em dissolver o sólido em um solvente quente e logo esfriar lentamente. Na baixa temperatura, o material dissolvido tem menor solubilidade, ocorrendo o crescimento de cristais. Se o processo for lento ocorre a formação de cristais, chamando-se, então, de cristalização, e, se for rápida, chamando-se de precipitação. O crescimento lento dos cristais, camada por camada, produz um produto puro, fazendo com que as impurezas fiquem na solução. Quando o esfriamento é rápido, as impurezas são arrastadas junto com o precipitado, produzindo um produto impuro. Assim, o fator crítico na recristalização é a escolha do solvente. Na técnica de recristalização, um solvente pode ser classificado como bom quando:
- A. Reage com o soluto.
- B. Solubiliza o soluto a temperatura elevada (em geral no ponto de ebulição).
- C. Solubiliza muito o soluto em baixas temperaturas (em geral entre 0 a 25º C).
- D. Não é volátil.
- E. Tem baixo poder de dissolução para as impurezas à baixa temperatura, ou solubiliza a temperaturas altas.
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2014
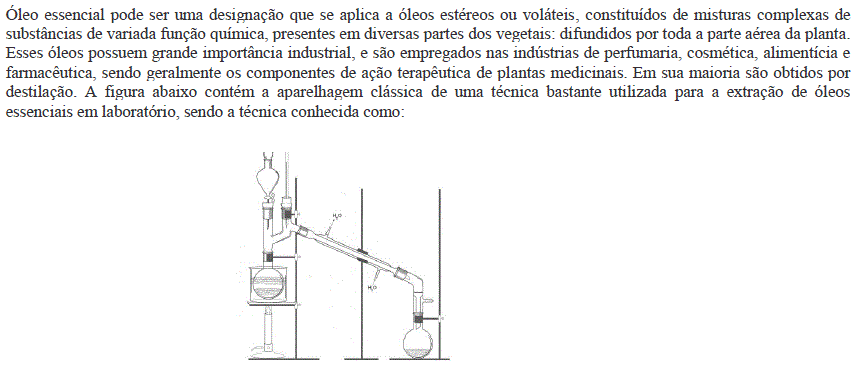
- A. Destilação simples.
- B. Destilação fracionada.
- C. Destilação por arraste de vapor.
- D. Destilação azeotrópica.
- E. Destilação a pressão reduzida.
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2014
Os resíduos químicos dos Institutos e Departamentos de Química das Universidades se diferenciam daqueles gerados em unidades industriais por apresentarem baixo volume, mas grande diversidade de composições, o que dificulta a tarefa de estabelecer um tratamento químico e/ou uma disposição final padrão para todos. No caso específico de Biossegurança em laboratórios biomédicos e microbiológicos, todas as culturas, colônias e outros resíduos deverão ser descontaminados antes de serem descartados. Dentre os métodos físicos de esterilização na área de Biossegurança, o mais utilizado para o nível de biossegurança 1 é a esterilização:
- A. Por calor úmido (autoclave).
- B. Com óxido de etileno (eto).
- C. Com solução sulfocrômica.
- D. Com solução de água sanitária.
- E. Com peróxido de hidrogênio (h2o2).
Química - Química, Tecnologia, Sociedade e Meio Ambiente - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2014
Química Verde é uma nova visão do problema ambiental e considera que, fundamentalmente, é preciso buscar uma alternativa que evite ou minimize a produção de resíduos, em detrimento do tratamento do resíduo no fim da linha de produção ("end of pipe"). Dentre os princípios da Química Verde, aquele que combate o uso de grupos bloqueadores, proteção/desproteção, modificação temporária por processos físicos e químicos, porque podem gerar resíduos é:
- A. A Economia de Átomos.
- B. A Busca pela Eficiência de Energia.
- C. O Uso de Fontes Renováveis de Matéria-Prima.
- D. Evitar a Formação de Derivados.
- E. Análise em Tempo Real para a Prevenção da Poluição.
Química - Química Inorgânica - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2014
O efeito estufa é um fenômeno natural e possibilita a vida humana na Terra. Quando existe um balanço entre a energia solar incidente e a energia refletida na forma de calor pela superfície terrestre, o clima se mantém praticamente inalterado. Entretanto, o balanço de energia pode ser alterado devido às mudanças na concentração de gases de efeito estufa na atmosfera, decorrente da poluição. Dentre os principais gases de efeito estufa regulados pelo Protocolo de Quioto, aquele que é utilizado como referência para classificar o poder de aquecimento global dos demais gases de efeito estufa é o:
- A. Gás metano CH4.
- B. Óxido nitroso - N2O.
- C. Hexafluoreto de enxofre - SF6.
- D. Perfluorcarbonos PFCs.
- E. Dióxido de carbono CO2.
Química - Química Inorgânica - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2014
O carbeto de cálcio apresenta fórmula química CaC2. É usado em alguns tipos de maçaricos oxi-acetilênicos, nos quais reage com a água produzindo acetileno (etino) que é usado na fabricação dos seguintes materiais: explosivos, solventes industriais e plásticos de borracha sintética. Este composto também é empregado na síntese de compostos orgânicos como ácido acético (oxidação) e álcool etílico (redução). O acetileno ao ser hidratado se converte em etanal, o qual pode sofrer oxidação (obtendo o composto X) ou redução (obtendo o composto Y).Se X e Y são compostos orgânicos oxigenados, a nomenclatura oficial da IUPAC do composto orgânico z, resultante da reação de X com Y é:
- A. Álcool etílico.
- B. Etoxi-etano.
- C. Etanoato de etila.
- D. Ácido etanoico.
- E. Eteno.


