Questões sobre Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica
Lista completa de Questões sobre Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
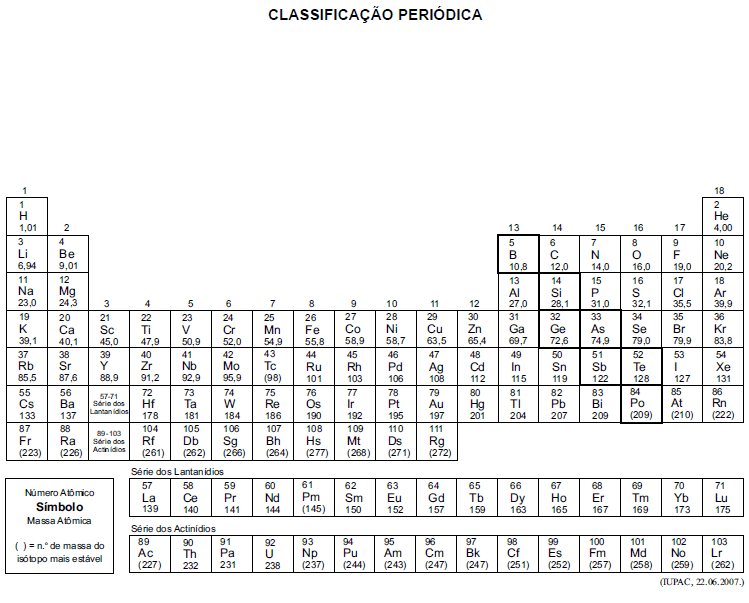
A tabela periódica encontra-se no final deste caderno.
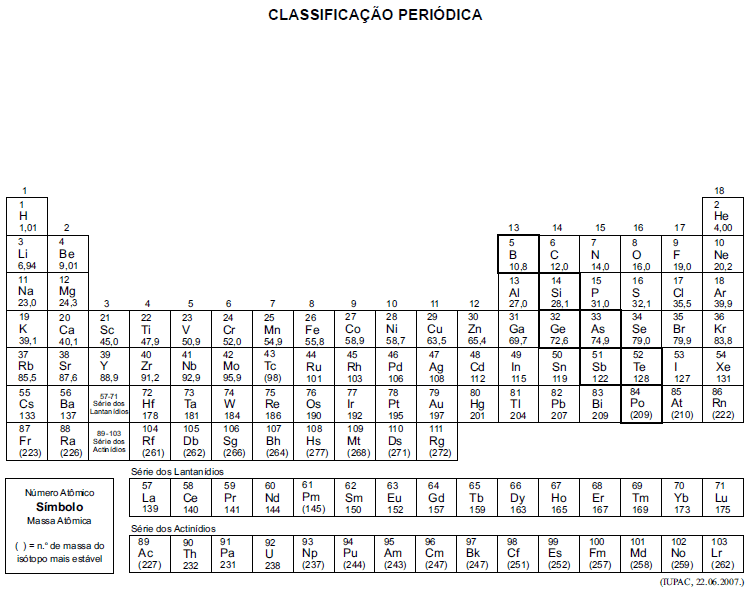
O enriquecimento do urânio pelo método da difusão em cascata é possível porque entre os isótopos desse elemento há diferença de
- A.
número atômico.
- B.
carga nuclear.
- C.
massa nuclear.
- D.
carga elétrica.
- E.
número de elétrons.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
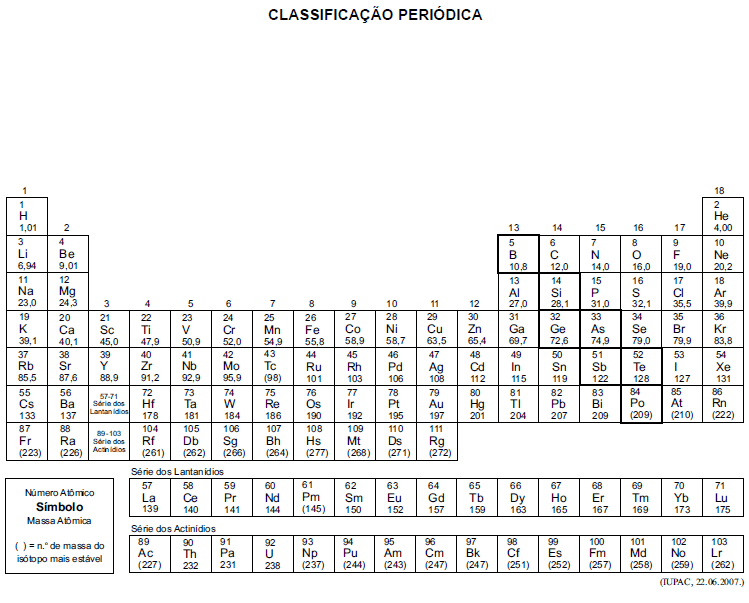
A tabela periódica encontra-se no final deste caderno.
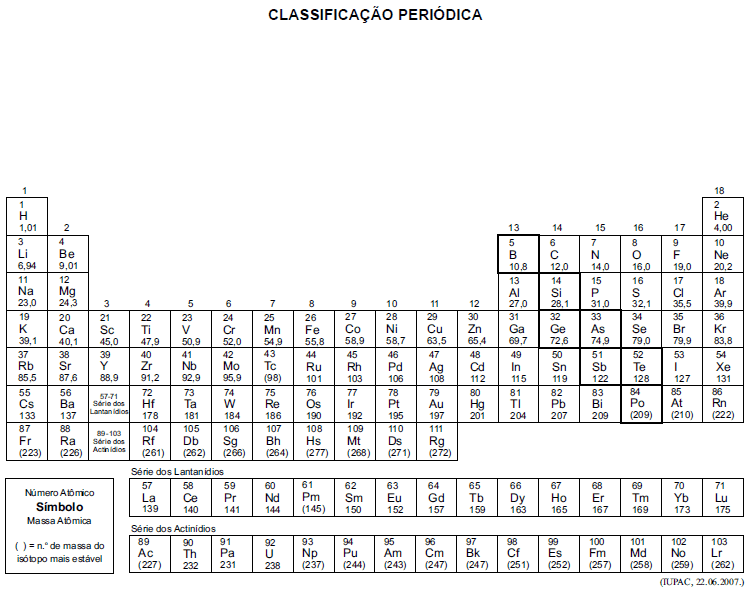

- A.

- B.

- C.

- D.

- E.

Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
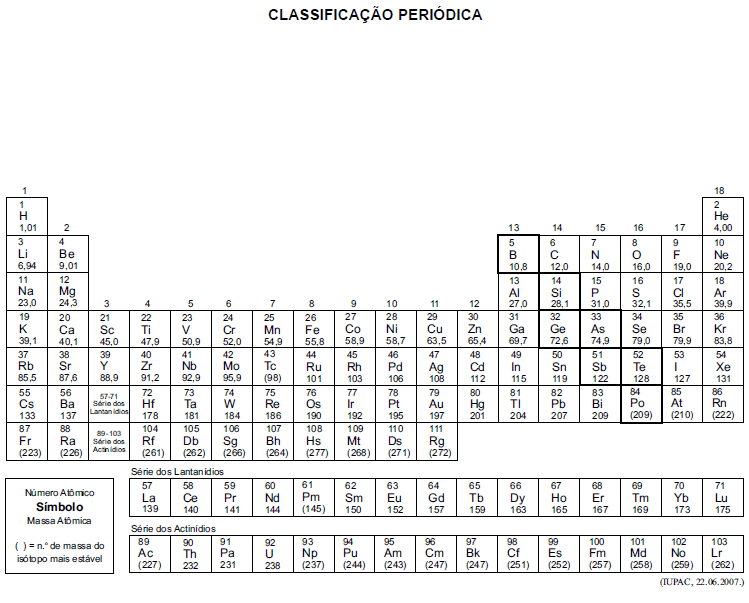
A tabela periódica encontra-se no final deste caderno.
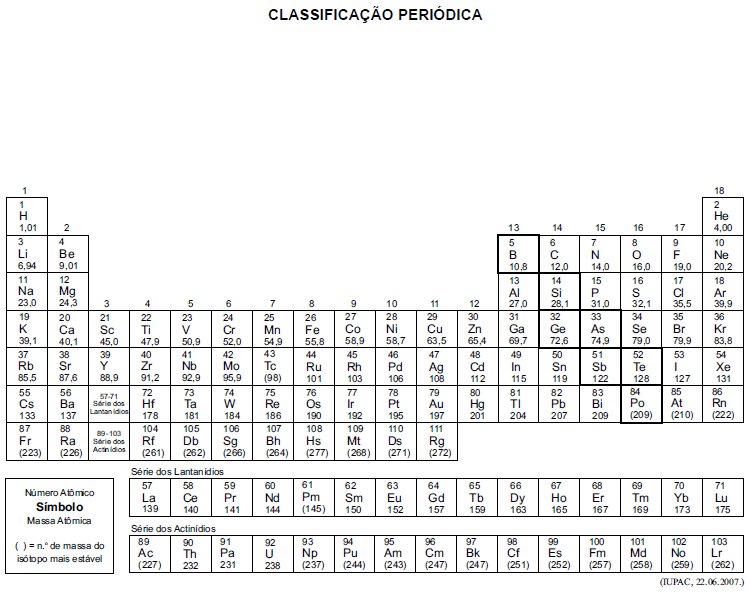
Considere as seguintes entalpias de combustão.
Etanol: 1 400 kJ/mol
Gasolina: 5 400 kJ/mol
A quantidade de CO2 (g), em mol, liberada quando se obtém a mesma quantidade de energia da combustão de 1 mol de gasolina (composição média C8H18), utilizando-se etanol, corresponde a, aproximadamente,
- A.
1,5.
- B.
4,4.
- C.
5,2.
- D.
6,5.
- E.
7,7.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
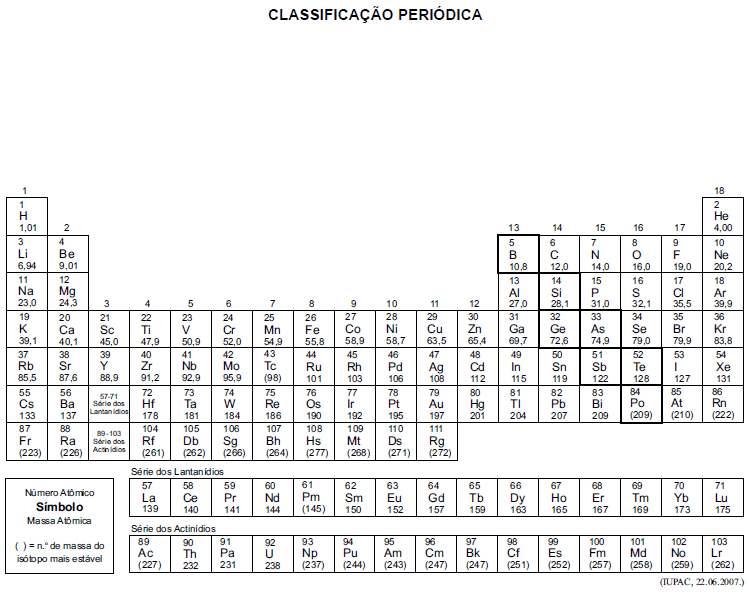
A tabela periódica encontra-se no final deste caderno.
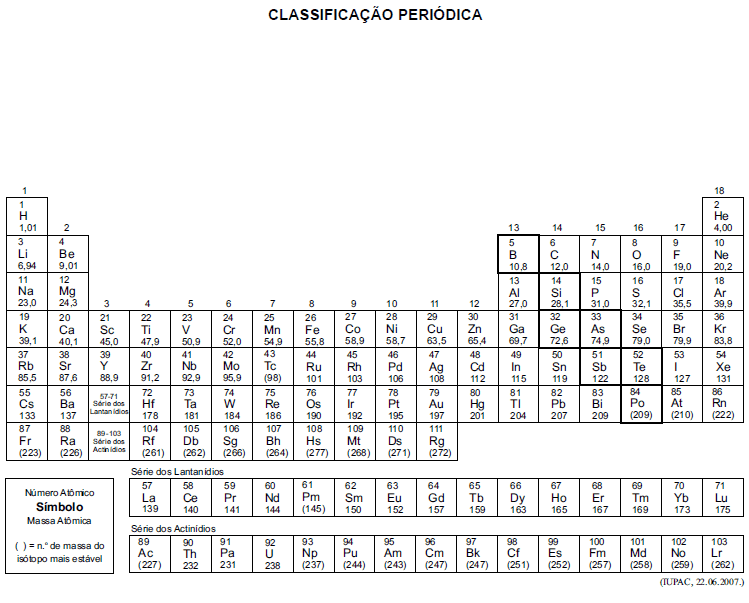
Para a obtenção do café solúvel, dois processos podem ser realizados na secagem do extrato do café: por ar seco e por liofilização (realizado em temperatura de 20 ºC e pressões perto do vácuo, em que não há presença de água no estado líquido). Em ambos os casos se retira a água, sendo que, o primeiro se dá por
- A.
evaporação e o segundo, por sublimação.
- B.
sublimação e o segundo, por liquefação.
- C.
liquefação e o segundo, por condensação.
- D.
condensação e o segundo, por fusão.
- E.
fusão e o segundo, por solidificação.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
As transformações químicas podem ser utilizadas para gerar energia e, assim, possibilitar a ocorrência de outras que consomem energia. Exemplos de transformações químicas que ocorrem, respectivamente, com liberação e absorção de energia são:
- A.
combustão do etanol e neutralização de ácidos.
- B.
fermentação biológica e combustão da gasolina.
- C.
queima de carvão e cozimento de um bolo.
- D.
cozimento de um ovo e fermentação biológica.
- E.
queima da madeira e combustão de metano.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
Práticas agrícolas que envolvem desmatamento em larga escala, bem como o uso indiscriminado de praguicidas e fertilizantes, acarretam perturbações no ciclo natural
I. da água;
II. do nitrogênio;
III. do carbono.
Está correto o que se afirma em
- A.
I, apenas.
- B.
II, apenas.
- C.
I e II, apenas.
- D.
II e III, apenas.
- E.
I, II e III.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
No refino do petróleo, o aumento da quantidade de gasolina pode ser conseguido por processos que envolvem transformações como as exemplificadas a seguir:
1. C16H34 → C8H16 + C8H18
2. C4H10 + C4H8 → C8H18
As transformações 1 e 2 exemplificam, correta e respectivamente, os processos conhecidos como
- A.
craqueamento e alquilação.
- B.
craqueamento e hidrogenação.
- C.
hidrogenação e alquilação.
- D.
alquilação e hidrogenação.
- E.
alquilação e craqueamento.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
Dois açúcares presentes na alimentação humana são a glicose e a frutose, cuja fórmula molecular é a mesma: C6H12O6. Esses dois açúcares são:
I. hexoses;
II. isômeros entre si;
III. poliidroxialdeídos.
Está correto o que se afirma apenas em
- A.
I.
- B.
II.
- C.
III.
- D.
I e II.
- E.
II e III.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
A 25 ºC, o produto iônico da água, Kw , é igual a 1 x 1014. Nessa temperatura, o papel de tornassol azul torna-se vermelho em soluções aquosas cujo pH é inferior a 5 e o papel de tornassol vermelho torna-se azul em soluções aquosas cujo pH é superior a 8. Esses dois papéis manterão sua cor inalterada, caso sejam imersos em uma solução aquosa em que a concentração de íons OH , em mol, por litro, seja igual a
- A.
1 x 1011.
- B.
1 x 1010.
- C.
1 x 108.
- D.
1 x 105.
- E.
1 x 103.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2012
A tabela periódica encontra-se no final deste caderno.
A água do mar é fonte natural para a obtenção industrial de várias substâncias, entre elas:
I. soda cáustica;
II. cloro;
III. magnésio;
IV. cloreto de sódio.
Processos químicos eletrolíticos são empregados para a obtenção do contido em
- A.
I e IV, apenas.
- B.
II e III, apenas.
- C.
II e IV, apenas.
- D.
I, II e III, apenas.
- E.
I, II, III e IV.


