Questões sobre Eletroquímica
Lista completa de Questões sobre Eletroquímica para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Eletroquímica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2013
Considere as distribuições eletrônicas dos elementos cálcio e flúor no estado fundamental e a sua localização na Tabela Periódica. É de se esperar que esses dois elementos formem, ao se unirem por ligação química, o composto
- A.
iônico, de fórmula CaF2.
- B.
iônico, de fórmula Ca2F.
- C.
molecular, de fórmula CaF2.
- D.
iônico, de fórmula CaF.
- E.
molecular, de fórmula CaF.
Se a uma dispersão coloidal aplicarmos uma diferença de potencial, através de eletrodos mergulhados nessa dispersão, observaremos que as partículas se moverão em direção a esses eletrodos. Aesse fenômeno denominamos:
- A. movimento browniano.
- B. eletroforese.
- C. potencial Zeta.
- D. eletrólise.
- E. dissociação iônica.
Considerando que na eletrogravimetria e na coulometria, a eletrólise é realizada por tempo suficiente para assegurar a oxidação ou redução completa do analito a um produto de composição conhecida, julgue os próximos itens.
Um requisito fundamental para a titulação coulométrica é que a eficiência da corrente seja igual a 100%.
- C. Certo
- E. Errado
Química - Eletroquímica - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2013
As células a combustível, dispositivos eletroquímicos que transformam energia química em energia elétrica, empregam como principal componente eletrocatalisadores, que são óxidos metálicos e metais de transição nanodispersos sobre a superfície de carbono na forma de negro de fumo. O sistema opera em meio aquoso.
Sobre os eletrocatalisadores da célula a combustível, é correto afirmar que a fase dispersa, o meio de dispersão e a sua classificação quanto à sua interação com a água do sistema são, respectivamente,- A.
sólido; sólido; hidrofóbico.
- B.
sólido; sólido; hidrofílico.
- C.
sólido; líquido, hidrofílico.
- D.
líquido, sólido, hidrofílico.
- E.
líquido, sólido; hidrofóbico.
As reações que ocorrem com transferência de elétrons são denominadas reações de oxirredução, ou, simplesmente, reações redox. Acerca desse assunto, julgue os seguintes itens.
Uma característica das reações de oxirredução é a presença de um agente oxidante e de um agente redutor. O agente oxidante recebe elétrons; o agente redutor, por sua vez, perde elétrons.
- C. Certo
- E. Errado
A respeito das ligações químicas e dos estados de agregação da matéria, julgue os itens subsecutivos.
De acordo com a teoria de ligação de valência de Linus Pauling, a ligação covalente ocorre quando há a sobreposição dos orbitais atômicos, que devem possuir, além de energias semelhantes, orientação adequada.
- C. Certo
- E. Errado
A respeito das ligações químicas e dos estados de agregação da matéria, julgue os itens subsecutivos.
O rompimento de uma ligação química poderá ocorrer por meio de um processo endotérmico ou exotérmico.
- C. Certo
- E. Errado
A respeito das ligações químicas e dos estados de agregação da matéria, julgue os itens subsecutivos.
Os sólidos metálicos são maleáveis, insolúveis em solventes orgânicos e apresentam alta condutividade elétrica. Além disso, muitos deles reagem com água.
- C. Certo
- E. Errado
Utilizando uma corrente de 100 mA, a eletrodeposição de 1,0 g de níquel a partir de Ni2+ (aq), sobre uma bijuteria de aço inox levaria o tempo, em minutos, de
Dados: Massa molar do níquel = 58,7 g/mol Constante de Faraday = 9,65 × 104 C/mol- A.
233.
- B.
354.
- C.
487.
- D.
487.
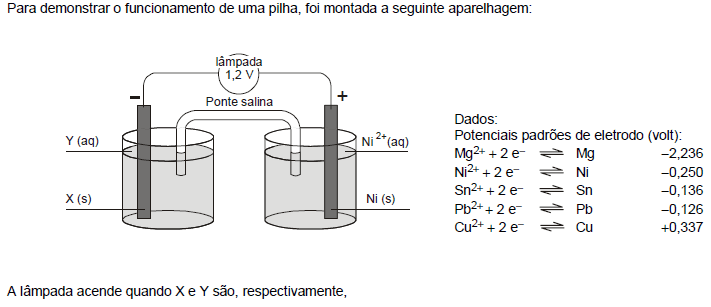
- A.
chumbo e nitrato de chumbo (II).
- B.
cobre e cloreto de cobre (II).
- C.
magnésio e sulfato de magnésio.
- D.
estanho e sulfato de estanho (II).


