Questões sobre Reações, Soluções e Transformações Químicas
Lista completa de Questões sobre Reações, Soluções e Transformações Químicas para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
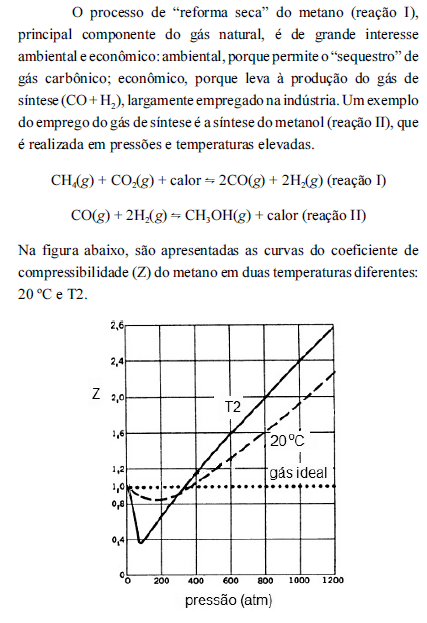
Com base nas informações acima, julgue os itens subsequentes, considerando que, para a reação II, a uma temperatura T, a constante de equilíbrio seja igual a K.
O valor da temperatura T2, representada no gráfico, é superior a 20 ºC.- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
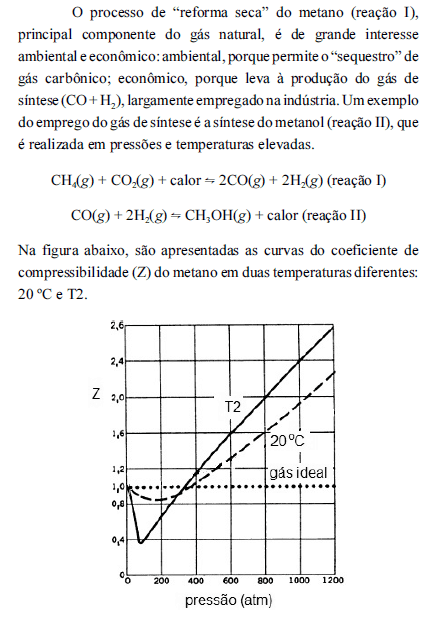
Com base nas informações acima, julgue os itens subsequentes, considerando que, para a reação II, a uma temperatura T, a constante de equilíbrio seja igual a K.
Um tanque contendo metano, a 20 ºC e a 200 atm, possui maior quantidade do gás do que a quantidade estimada com a equação dos gases ideais.- C. Certo
- E. Errado

- A. - 377
- B. - 722
- C. - 1.147
- D. - 2.566
- E. - 3.090
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
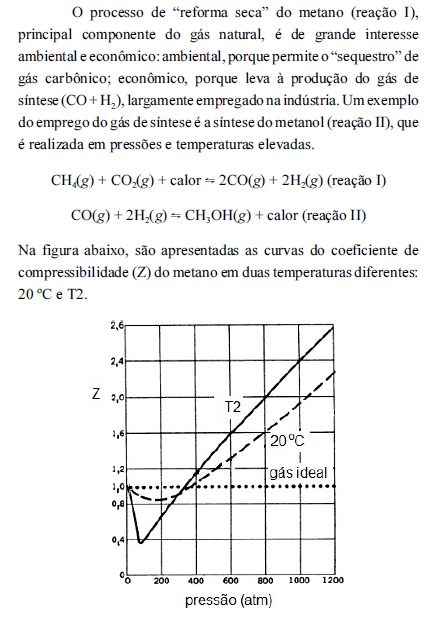
Com base nas informações acima, julgue os itens subsequentes, considerando que, para a reação II, a uma temperatura T, a constante de equilíbrio seja igual a K.
Para a reação II, o emprego de pressões elevadas favorece a formação dos produtos tanto do ponto de vista do equilíbrio químico, quanto da cinética. Entretanto, o emprego de temperaturas elevadas favorece a formação dos produtos do ponto de vista da cinética, mas desfavorece do ponto de vista do equilíbrio.- C. Certo
- E. Errado
Uma mistura gasosa, constituída por 112 g de nitrogênio e 16 g de metano, encontra-se em um recipiente de 30 L a uma pressão de 4 atm.
Considerando-se comportamento ideal para os gases, o valor de PCH4 / PN2 , isto é, a razão entre as pressões parciais de CH4 e N2 é
- A. 0,25
- B. 0,50
- C. 1,00
- D. 2,00
- E. 4,00
Química - Reações, Soluções e Transformações Químicas - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2014
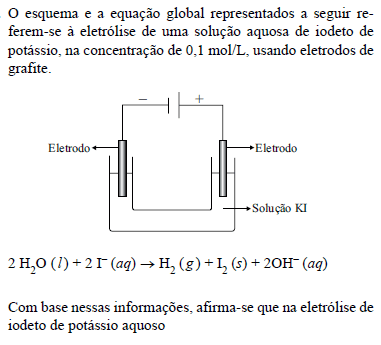
- A. há geração de gás hidrogênio no ânodo.
- B. íons iodeto são reduzidos no ânodo.
- C. ocorre redução da água no cátodo.
- D. forma-se iodo no cátodo.
- E. íons de potássio são reduzidos a átomos de potássio.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
A quantificação de ferro em uma amostra pode ocorrer por meio de análise gravimétrica. Por exemplo, na determinação do teor de ferro no solo, um dos procedimentos mais utilizados é o de, após solubilizar a amostra, adicionar NH4OH à solução, de forma a provocar a precipitação do ferro na forma de Fe2O3qxH2O. Em seguida, após a filtração, o precipitado é transformado em Fe2O3 e a pesagem é realizada.
Com base no texto acima, julgue os itens a seguir.
O NH4OH e o Fe2O3 são exemplos de compostos químicos correspondentes às funções base e óxido, respectivamente.- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2014
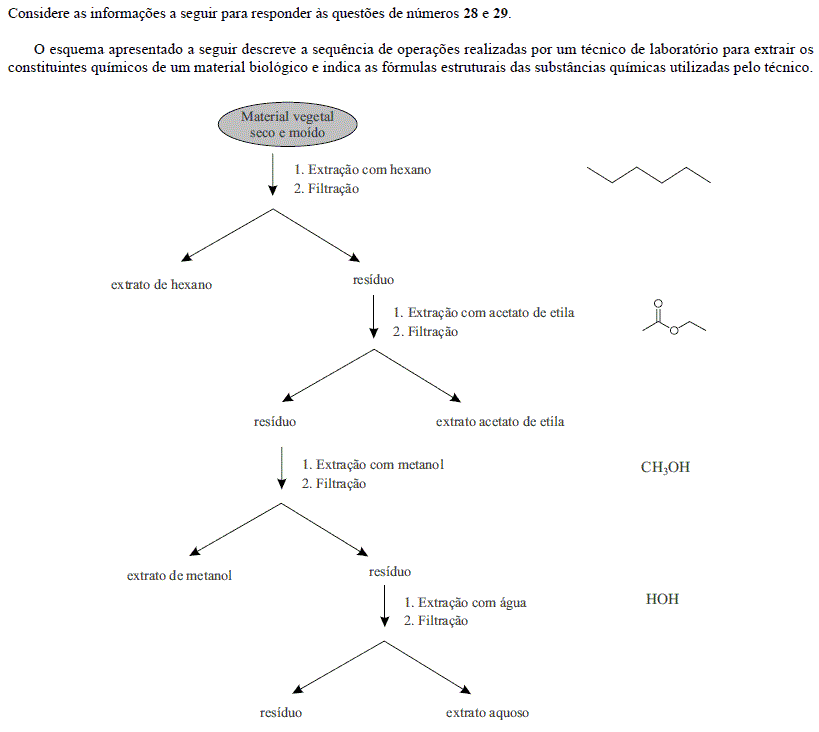 Sabendo que o material vegetal contém óleos, açúcares, polissacarídeos, vitamina C e sais minerais, afirma-se que o extrato em hexano e o resíduo após extração com água devem conter, respectivamente,
Sabendo que o material vegetal contém óleos, açúcares, polissacarídeos, vitamina C e sais minerais, afirma-se que o extrato em hexano e o resíduo após extração com água devem conter, respectivamente,
- A. açúcares e sais minerais.
- B. óleos e sais minerais.
- C. vitamina C e sais minerais.
- D. óleos e polissacarídeos.
- E. açúcares e polissacarídeos.

- A. alcino
- B. alcano
- C. polímero de condensação
- D. polímero de adição
- E. copolímero
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
A quantificação de ferro em uma amostra pode ocorrer por meio de análise gravimétrica. Por exemplo, na determinação do teor de ferro no solo, um dos procedimentos mais utilizados é o de, após solubilizar a amostra, adicionar NH4OH à solução, de forma a provocar a precipitação do ferro na forma de Fe2O3qxH2O. Em seguida, após a filtração, o precipitado é transformado em Fe2O3 e a pesagem é realizada.
Com base no texto acima, julgue os itens a seguir.
Considere que 1,00 g de amostra de solo seja analisado e que a massa de Fe2O3 formada após a calcinação tenha sido igual a 200 mg. Nessa situação, a porcentagem em massa de ferro na amostra de solo é superior a 20%.- C. Certo
- E. Errado


