Questões sobre Reações, Soluções e Transformações Químicas
Lista completa de Questões sobre Reações, Soluções e Transformações Químicas para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
A quantificação de ferro em uma amostra pode ocorrer por meio de análise gravimétrica. Por exemplo, na determinação do teor de ferro no solo, um dos procedimentos mais utilizados é o de, após solubilizar a amostra, adicionar NH4OH à solução, de forma a provocar a precipitação do ferro na forma de Fe2O3qxH2O. Em seguida, após a filtração, o precipitado é transformado em Fe2O3 e a pesagem é realizada.
Com base no texto acima, julgue os itens a seguir.
Para a determinação do teor de ferro em uma amostra de solo por meio do método gravimétrico, deve-se proceder, inicialmente, à dissolução da amostra por um ácido forte, como o ácido nítrico, de forma a garantir que o ferro seja todo oxidado a Fe 3+ e solubilizado.- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
A quantificação de ferro em uma amostra pode ocorrer por meio de análise gravimétrica. Por exemplo, na determinação do teor de ferro no solo, um dos procedimentos mais utilizados é o de, após solubilizar a amostra, adicionar NH4OH à solução, de forma a provocar a precipitação do ferro na forma de Fe2O3qxH2O. Em seguida, após a filtração, o precipitado é transformado em Fe2O3 e a pesagem é realizada.
Com base no texto acima, julgue os itens a seguir.
Na análise gravimétrica, o agente precipitante deve ser adicionado em excesso para reduzir a quantidade do analito que permanece dissolvida.- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2014
 A equação química correta, que descreve a transformação relatada na anotação 2 é escrita como
A equação química correta, que descreve a transformação relatada na anotação 2 é escrita como
- A.

- B.

- C.

- D.

- E.

Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
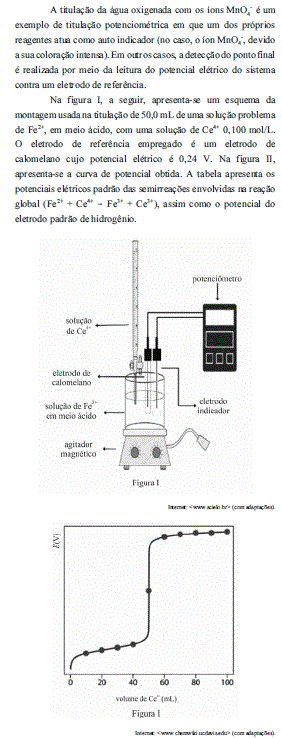
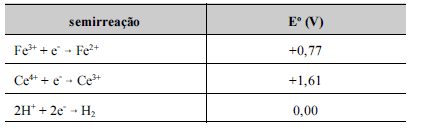
A partir das informações apresentadas, julgue os itens que se seguem, considerando que os potenciais elétricos padrão listados na tabela são válidos no meio ácido no qual foi realizada a titulação e desconsiderando a ocorrência de potenciais de junção.
Na reação de oxirredução apresentada, o Fe 2+ é o agente redutor, e o Ce 4+, o agente oxidante.- C. Certo
- E. Errado
Na combustão completa de 1 mol de butanol (C4H10O), a quantidade máxima, em mols, de dióxido de carbono produzido é igual a
- A. 1
- B. 2
- C. 3
- D. 4
- E. 5
Química - Reações, Soluções e Transformações Químicas - Fundação para o Vestibular da Universidade Estadual Paulista (VUNESP) - 2014
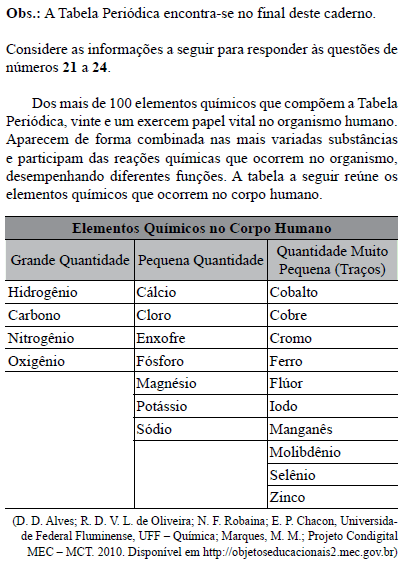 Considerando a massa molar do NaCl igual a 58,5 g/mol e sabendo que um organismo adulto contém em média 250 g de NaCl e que nele circulam 42 litros de água, a concentração de NaCl, em mol/L, no corpo de um adulto corresponde aproximadamente a
Considerando a massa molar do NaCl igual a 58,5 g/mol e sabendo que um organismo adulto contém em média 250 g de NaCl e que nele circulam 42 litros de água, a concentração de NaCl, em mol/L, no corpo de um adulto corresponde aproximadamente a
- A. 4,0.
- B. 0,1.
- C. 1,0.
- D. 0,4.
- E. 2,0.
Qual é, aproximadamente, a porcentagem da massa de cobre (Cu) no sulfato de cobre penta-hidratado (CuSO4.5H2O)?
- A. 12,7%
- B. 25,5%
- C. 31,8%
- D. 38,1%
- E. 44,4%
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
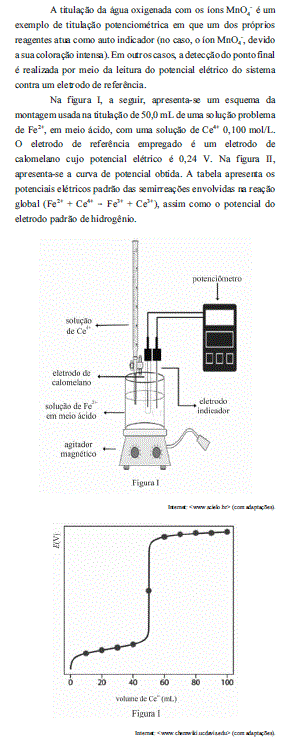
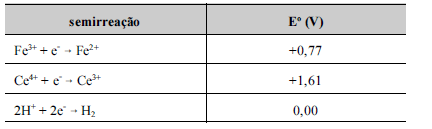
A partir das informações apresentadas, julgue os itens que se seguem, considerando que os potenciais elétricos padrão listados na tabela são válidos no meio ácido no qual foi realizada a titulação e desconsiderando a ocorrência de potenciais de junção.
Considere que tenha sido adicionado um volume da solução de Ce 4+ correspondente à metade do volume necessário para se atingir o ponto de equivalência. Nesse caso, o módulo do potencial elétrico lido no potenciômetro representado na figura I será superior a 0,70 V.- C. Certo
- E. Errado
Reações de oxirredução são aquelas em que há espécies que doam elétrons e espécies que recebem elétrons, ocasionando nesse processo variação do número de oxidação. Um exemplo de oxirredução é a seguinte reação
- A.

- B.

- C.

- D.

- E.

Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2014
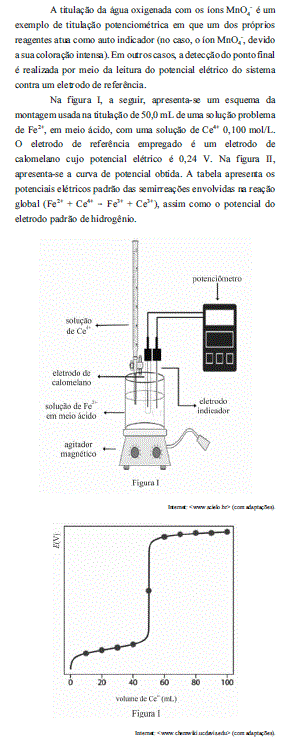
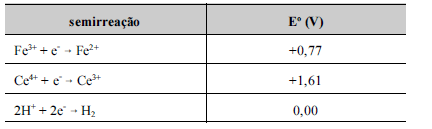
A partir das informações apresentadas, julgue os itens que se seguem, considerando que os potenciais elétricos padrão listados na tabela são válidos no meio ácido no qual foi realizada a titulação e desconsiderando a ocorrência de potenciais de junção.
A concentração de ferro na solução problema é superior a 0,090 mol/L.- C. Certo
- E. Errado


