Questões sobre Teorias Atômicas
Lista completa de Questões sobre Teorias Atômicas para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
John Dalton criou uma teoria sobre a estrutura da matéria que, mais tarde, ficou conhecida como Teoria Atômica de Dalton. Nela, Dalton propõe que
- A.
toda matéria é formada por átomos.
- B.
os átomos são divisíveis, daí, um número elevado na natureza desses elementos.
- C.
a formação da matéria não se dá por associações entre átomos iguais.
- D.
a matéria é feita, simplesmente, de substâncias compostas.
Considere as representações de John Dalton para os constituintes da matéria.
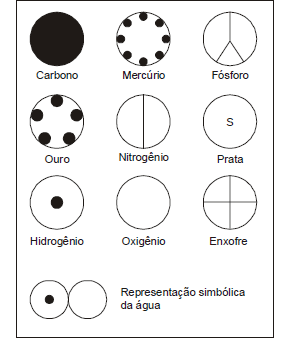
Representando, com os símbolos atuais, a combustão de hidrogênio, segundo as ideias de John Dalton para a constituição da matéria, tem-se
- A.
H + O
 HO
HO - B.
H−H + O
 H2O
H2O - C.
H + O−O
 HO2
HO2 - D.
H−H + O−O
 H2O2
H2O2 - E.
2 H−H + O−O
 2H2O
2H2O
Grande parte dos efeitos luminosos visualizados durante shows com fogos de artifício é produzida por luminescência. Nesse fenômeno, elétrons são excitados a estados de energia mais elevados e, ao retornarem para estados mais baixos, emitem luz característica de cada espécie química. Por exemplo, sais de Sr2+ emitem radiação vermelha, enquanto sais de Cu2+, radiação azul.
Tendo o fragmento de texto acima como referência inicial, julgue os itens seguintes, a respeito da luminescência e de sua relação com a estrutura eletrônica.
O experimento de bombardeamento de uma fina folha de platina com partículas 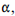 realizado no início do século XX pela equipe de Ernest Rutherford, permitiu explicar a razão de cada espécie química emitir radiação com uma coloração específica.
realizado no início do século XX pela equipe de Ernest Rutherford, permitiu explicar a razão de cada espécie química emitir radiação com uma coloração específica.
- C. Certo
- E. Errado
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Dois átomos que apresentem o mesmo número atômico mas diferentes números de nêutrons são elementos químicos diferentes.
- C. Certo
- E. Errado
Uma das grandes descobertas da ciência foi realizada por Ernest Rutherford, a partir de sua famosa experiência na qual bombardeou uma lâmina de ouro com partículas alfa, que possuem carga positiva. Observando o ângulo de desvio dessas partículas, percebeu que a maioria atravessava direto o ouro, algumas apresentavam desvio e outras sofriam uma violenta repulsão, que as mandava de volta. Com essas observações, constatou que
- A.
toda carga negativa do átomo estava concentrada no núcleo, e as cargas positivas dispostas ao redor na eletrosfera.
- B.
toda a massa, praticamente, do átomo está concentrada na eletrosfera, uma vez que os elétrons são muito mais pesados que os prótons.
- C.
o átomo é uma estrutura contínua, na qual, prótons e elétrons estariam misturados continuamente como num bolo recheado de passas.
- D.
o átomo constitui-se de um núcleo muito pequeno de carga positiva e os elétrons orbitam em torno dele, na chamada eletrosfera.
- E.
o átomo constitui-se de um núcleo muito pequeno de carga neutra, contendo prótons e elétrons, enquanto que os nêutrons orbitam em torno dele, na chamada eletrosfera.

- A.
I.
- B.
II.
- C.
III.
- D.
I e II.
- E.
II e III.
Com relação à mais importante ferramenta utilizada pelos químicos, assinale a opção correta.
- A.
Mendeleev e Meyer publicaram, no mesmo ano, esquemas de classificação periódica de elementos fundamentados na distribuição eletrônica dos respectivos átomos.
- B.
Data do século XIX a identificação dos primeiros elementos químicos.
- C.
Todos os elementos presentes na tabela de Mendeleev haviam sido identificados pelos pesquisadores da época.
- D.
Moseley demonstrou que átomos de cada tipo de elemento químico produzem raios X de frequência única, geralmente proporcional à massa atômica.
Apesar da pequena variedade de elementos químicos, cerca de 100 naturais, tem-se uma enorme diversidade de substâncias devido às diferentes possibilidades de ligação entre átomos de um mesmo elemento e entre átomos de diferentes elementos. Com relação a esse assunto, julgue os itens a seguir.
De acordo com o modelo da repulsão de pares de elétrons no nível de valência, o número de coordenação total de um átomo é igual à soma do número de átomos coordenados com o número de elétrons não ligantes.
- C. Certo
- E. Errado
Os métodos espectrométricos têm sido cada vez mais utilizados em química analítica em substituição aos métodos clássicos tradicionais, na determinação de elementos e compostos. Com relação a fundamentos, equipamentos e ferramentas envolvidos na aplicação desses métodos, julgue os itens seguintes.
Um porta-amostras de vidro de silicato é adequado para a realização de análises por espectrometria de absorção molecular nas regiões do ultravioleta e do visível.
- C. Certo
- E. Errado
Os métodos espectrométricos têm sido cada vez mais utilizados em química analítica em substituição aos métodos clássicos tradicionais, na determinação de elementos e compostos. Com relação a fundamentos, equipamentos e ferramentas envolvidos na aplicação desses métodos, julgue os itens seguintes.
Em espectrometria de absorção, o uso de feixe duplo em um equipamento tem o objetivo de minimizar a ocorrência de erros decorrentes de variações de intensidade do feixe incidente sobre a amostra devido a variações de voltagem na fonte de radiação.
- C. Certo
- E. Errado


