Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE)
Lista completa de Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
O flúor apresenta raio atômico menor que o do nitrogênio.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Todos os elementos de um mesmo grupo da tabela periódica apresentam, na forma não ionizada, o mesmo número de elétrons de valência.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Nas primeiras versões da tabela periódica, antes da descoberta da massa atômica, o ordenamento dos elementos era feito com base nos números atômicos.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
De acordo com a teoria das ligações de valência, a maior parte dos gases nobres é capaz de formar compostos moleculares, uma vez que podem sofrer expansão da sua camada de valência.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Dois átomos que apresentem o mesmo número atômico mas diferentes números de nêutrons são elementos químicos diferentes.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Os elementos químicos pertencentes ao grupo dos halogênios caracterizam-se por serem os que apresentam as mais elevadas energia de ionização e eletronegatividade.
- E. Errado
- C. Certo
No Brasil, as técnicas de tratamento de água para abastecimento público contemplam, em geral, as seguintes etapas: clarificação, desinfecção, fluoretação e estabilização química. A respeito dessas etapas, julgue os itens que se seguem.
A estabilização química visa à neutralização de todos os compostos químicos utilizados nas demais etapas do tratamento da água, a fim de garantir que ela não tenha cheiro nem sabor.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
No Brasil, as técnicas de tratamento de água para abastecimento público contemplam, em geral, as seguintes etapas: clarificação, desinfecção, fluoretação e estabilização química. A respeito dessas etapas, julgue os itens que se seguem.
A fluoretação propicia a eliminação de organismos patogênicos que possam estar presentes na água.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
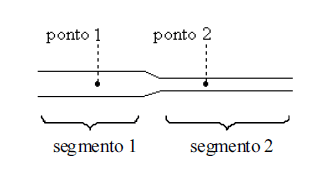
Considere que a tubulação acima representada é empregada para o transporte de um fluido. Para o segmento 1, o diâmetro do tubo é d; já para o segmento 2, o diâmetro é d/2.
Com relação a esse sistema, julgue o item subseqüente.
Para um fluido ideal, a velocidade v2 de escoamento no ponto 2 será duas vezes maior do que a velocidade de escoamento, v1, verificada no ponto 1.- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
Na espectroscopia de absorção atômica, a identificação e quantificação de determinado elemento é possível devido ao efeito da quantização da energia dos elétrons nos átomos, o qual faz com que os átomos apresentem linhas de absorção características de cada elemento. A figura a seguir apresenta a curva de calibração construída a partir de análises de espectroscopia de absorção atômica de soluções padrão de determinado metal. As absorbâncias correspondem a um comprimento de onda 8, sendo o caminho óptico percorrido pelo feixe de radiação através das soluções igual a 2,0 cm.
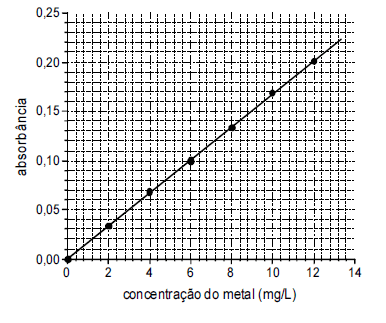
Considerando as informações fornecidas e a quantização de energia dos elétrons nos átomos, julgue os itens que se seguem.
A partir da lei de Beer, determina-se que o metal ao qual se refere a curva de calibração apresentada possui uma absortividade maior do que 10 L.g-1. cm-1 no comprimento de onda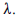
- C. Certo
- E. Errado


