Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE)
Lista completa de Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Alcoóis, sobretudo o metanol e o etanol, têm sido utilizados para substituir combustíveis líquidos. Eles podem ser diretamente queimados como combustíveis para gerar energia. No entanto, eles são usados também indiretamente. Por exemplo, o metanol é empregado para a formação de gasolina em uma reação catalisada por zeólitas, que são aluminossilicatos. As zeólitas são sólidos resultantes da substituição de alguns íons de Si +4 dos silicatos (óxidos de silício) por íons Al +3 . Sua função como catalisador está relacionada à sua capacidade em liberar íons H + . Considerando essas informações, julgue os itens seguintes.
As zeólitas são ácidos de Brønsted.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Alcoóis, sobretudo o metanol e o etanol, têm sido utilizados para substituir combustíveis líquidos. Eles podem ser diretamente queimados como combustíveis para gerar energia. No entanto, eles são usados também indiretamente. Por exemplo, o metanol é empregado para a formação de gasolina em uma reação catalisada por zeólitas, que são aluminossilicatos. As zeólitas são sólidos resultantes da substituição de alguns íons de Si +4 dos silicatos (óxidos de silício) por íons Al +3 . Sua função como catalisador está relacionada à sua capacidade em liberar íons H + . Considerando essas informações, julgue os itens seguintes.
A dispersão do metanol gasoso no interior das zeólitas forma uma emulsão.
- C. Certo
- E. Errado
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Alcoóis, sobretudo o metanol e o etanol, têm sido utilizados para substituir combustíveis líquidos. Eles podem ser diretamente queimados como combustíveis para gerar energia. No entanto, eles são usados também indiretamente. Por exemplo, o metanol é empregado para a formação de gasolina em uma reação catalisada por zeólitas, que são aluminossilicatos. As zeólitas são sólidos resultantes da substituição de alguns íons de Si +4 dos silicatos (óxidos de silício) por íons Al +3 . Sua função como catalisador está relacionada à sua capacidade em liberar íons H + . Considerando essas informações, julgue os itens seguintes.
Sabendo-se que os elementos químicos silício e oxigênio não são metálicos, então é correto afirmar que as ligações químicas existentes nos silicatos são iônicas.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Freqüentemente faz-se necessário diminuir o volume de uma solução que contenha um soluto não-volátil. Acerca desse assunto, assinale a opção correta.
- A.
As centrífugas a vácuo — chamadas também de concentradores a vácuo — são usadas para eliminação de solventes e purificação de solutos. Nesses equipamentos, a centrifugação é usada principalmente para criar uma força centrífuga que impede que o vácuo aspire a solução a ser secada.
- B.
Na evaporação de solventes em béqueres, não se deve cobrir o béquer com vidro de relógio porque isso impediria a evaporação dos solventes.
- C.
A evaporação por aquecimento deve ser conduzida sob chama intensa. Nesse caso, o uso de pérolas de vidro é desaconselhável, para evitar a contaminação da solução remanescente.
- D.
Não se deve adicionar ácido sulfúrico a soluções cujos constituintes orgânicos ainda não foram eliminados.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Alcoóis, sobretudo o metanol e o etanol, têm sido utilizados para substituir combustíveis líquidos. Eles podem ser diretamente queimados como combustíveis para gerar energia. No entanto, eles são usados também indiretamente. Por exemplo, o metanol é empregado para a formação de gasolina em uma reação catalisada por zeólitas, que são aluminossilicatos. As zeólitas são sólidos resultantes da substituição de alguns íons de Si +4 dos silicatos (óxidos de silício) por íons Al +3 . Sua função como catalisador está relacionada à sua capacidade em liberar íons H + . Considerando essas informações, julgue os itens seguintes.
Considerando-se que os íons citados no texto são obtidos quando os respectivos átomos cedem todos seus elétrons de orbitais da camada de valência, que são do tipo s e p, é correto afirmar que o alumínio é do grupo 3 (ou IIIB) e o silício, do grupo 4 (ou IVB).
- C. Certo
- E. Errado
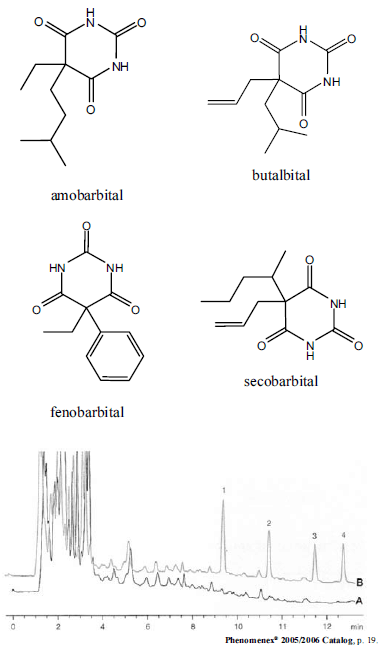
Uma das atividades mais rotineiras em um laboratório de perícia científica é a análise de drogas ilícitas. A figura acima mostra os cromatogramas do branco (A) e de uma amostra de urina humana (B), feitas por cromatografia de fase reversa com uma coluna Synergi ® Max-RP de 150 mm × 4,6 mm, 4 m de diâmetro de partícula, usando gradiente de KH 2 PO 4 20 mmol/L em água, pH 7,0 (solvente A), e acetonitrila (solvente B). Os picos 1, 2, 3 e 4 do cromatograma estão associados às drogas barbitúricas amobarbital, butalbital, fenobarbital e secobarbital, cujas estruturas são mostradas acima. Sabendo que a ordem de polaridade dessas moléculas é secobarbital < amobarbital < butalbital < fenobarbital, é correto concluir que os picos 1, 2, 3 e 4 do cromatograma correspondem, respectivamente, às drogas
- A.
secobarbital, amobarbital, butalbital e fenobarbital.
- B.
amobarbital, secobarbital, fenobarbital e butalbital.
- C.
butalbital, fenobarbital, secobarbital e amobarbital.
- D.
fenobarbital, butalbital, amobarbital, e secobarbital.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Alcoóis, sobretudo o metanol e o etanol, têm sido utilizados para substituir combustíveis líquidos. Eles podem ser diretamente queimados como combustíveis para gerar energia. No entanto, eles são usados também indiretamente. Por exemplo, o metanol é empregado para a formação de gasolina em uma reação catalisada por zeólitas, que são aluminossilicatos. As zeólitas são sólidos resultantes da substituição de alguns íons de Si +4 dos silicatos (óxidos de silício) por íons Al +3 . Sua função como catalisador está relacionada à sua capacidade em liberar íons H + . Considerando essas informações, julgue os itens seguintes.
Sabendo-se que o silício e o alumínio estão no 3. o período da tabela periódica, é correto afirmar que todos os orbitais que compõem a camada de valência desses elementos têm o número quântico principal igual a 3.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Texto para as questões de 24 a 31
A quantidade de proteína total no soro é um parâmetro clínico importante para o diagnóstico da disfunção hepática. O método de Kjeldahl é um dos métodos utilizados para essa determinação, que possibilita resultados de grande precisão e exatidão. Trata-se de um método para determinação de nitrogênio orgânico, com base em uma titulação de neutralização. No método de Kjeldahl, a amostra é decomposta a quente na presença de ácido sulfúrico concentrado, para converter todo o nitrogênio orgânico em íons amônio. A solução resultante é então resfriada, diluída e alcalinizada. A amônia liberada é destilada e coletada em uma solução que contém uma quantidade conhecida de um ácido padrão. O nitrogênio orgânico é determinado por titulação de retorno, ou seja, titulando-se o excesso de ácido nãoreagido no frasco de coleta. As reações são descritas a seguir.
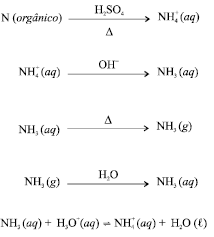
Um auxiliar técnico de perícia realizou o seguinte procedimento: pipetou 10,0 mL da solução contida em um frasco comercial de HCL cujo rótulo trazia as seguintes informações: 36,5% (fração em massa), M = 36,5 g/mol, d = 1,18 g/mL; transferiu o volume pipetado para um balão volumétrico de 250 mL; completou o volume do balão com água destilada; transferiu 25,0 mL dessa solução diluída para um frasco de coleta; acrescentou 50,0 mL de água destilada; realizou a destilação de Kjeldahl com 10,0 mL de uma amostra de sangue de um paciente humano, coletando a amônia no referido frasco de coleta. O ponto final da titulação do excesso de ácido não-reagido foi atingido com 17,0 mL de NaOH 0,500 mol/L.
No que se refere à situação hipotética descrita no texto, considerando que o sangue humano possui 6,25 g de proteína por grama de nitrogênio (M = 14,0 g/mol) e que todo o nitrogênio orgânico analisado é proveniente de proteínas, é correto concluir que a concentração de proteína total no sangue analisado é
- A.
inferior ou igual a 10 mg/mL.
- B.
superior a 10 mg/mL e inferior ou igual a 20 mg/mL.
- C.
superior a 20 mg/mL e inferior ou igual a 30 mg/mL.
- D.
superior a 30 mg/mL.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Alcoóis, sobretudo o metanol e o etanol, têm sido utilizados para substituir combustíveis líquidos. Eles podem ser diretamente queimados como combustíveis para gerar energia. No entanto, eles são usados também indiretamente. Por exemplo, o metanol é empregado para a formação de gasolina em uma reação catalisada por zeólitas, que são aluminossilicatos. As zeólitas são sólidos resultantes da substituição de alguns íons de Si +4 dos silicatos (óxidos de silício) por íons Al +3 . Sua função como catalisador está relacionada à sua capacidade em liberar íons H + . Considerando essas informações, julgue os itens seguintes.
A queima de etanol ou do metanol é uma reação de óxidoredução.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Texto para as questões de 24 a 31
A quantidade de proteína total no soro é um parâmetro clínico importante para o diagnóstico da disfunção hepática. O método de Kjeldahl é um dos métodos utilizados para essa determinação, que possibilita resultados de grande precisão e exatidão. Trata-se de um método para determinação de nitrogênio orgânico, com base em uma titulação de neutralização. No método de Kjeldahl, a amostra é decomposta a quente na presença de ácido sulfúrico concentrado, para converter todo o nitrogênio orgânico em íons amônio. A solução resultante é então resfriada, diluída e alcalinizada. A amônia liberada é destilada e coletada em uma solução que contém uma quantidade conhecida de um ácido padrão. O nitrogênio orgânico é determinado por titulação de retorno, ou seja, titulando-se o excesso de ácido nãoreagido no frasco de coleta. As reações são descritas a seguir.
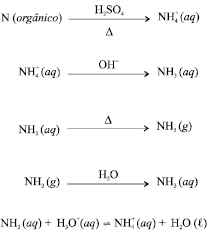
Um auxiliar técnico de perícia realizou o seguinte procedimento: pipetou 10,0 mL da solução contida em um frasco comercial de HCL cujo rótulo trazia as seguintes informações: 36,5% (fração em massa), M = 36,5 g/mol, d = 1,18 g/mL; transferiu o volume pipetado para um balão volumétrico de 250 mL; completou o volume do balão com água destilada; transferiu 25,0 mL dessa solução diluída para um frasco de coleta; acrescentou 50,0 mL de água destilada; realizou a destilação de Kjeldahl com 10,0 mL de uma amostra de sangue de um paciente humano, coletando a amônia no referido frasco de coleta. O ponto final da titulação do excesso de ácido não-reagido foi atingido com 17,0 mL de NaOH 0,500 mol/L.
Um método para determinação de proteína total em soro, alternativo ao método de Kjeldahl, é o método espectrofotométrico do biureto, no qual um reagente que contém íons Cu 2+ é utilizado para promover a formação de complexos de cor violeta entre os íons Cu 2+ e as ligações peptídicas das proteínas. Considerando ainda o texto, assinale a opção correta acerca desse assunto.
- A.
No método do biureto, é utilizado comprimento de onda na região do ultravioleta.
- B.
Entre as vantagens do método do biureto em relação ao método de Kjeldahl incluem-se ser mais rápido, prático, preciso e sensível, além de ser automatizável, ao contrário deste.
- C.
A medida da concentração dos complexos Cu-proteína pode ser feita também por colorimetria.
- D.
De acordo com a Lei de Beer, a absorvância da solução é proporcional ao quadrado da concentração dos complexos Cu-proteína na solução.


