Questões de Engenharia Química do ano 2011
Lista completa de Questões de Engenharia Química do ano 2011 para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
No armazenamento de substâncias de elavada pressão de vapor, existe o risco de ruptura do material dos tanques de armazenamento e da dispersão de tais substâncias em estado gasoso no ambiente. Em uma unidade, é necessário armazenar amônia condensada em um tanque. Uma forma de diminuir a pressão de vapor de amônia é
- A.
aumentar a altura do tanque de armazenamento.
- B.
injetar, dentro do tanque de armazenamento, um gás inerte e insolúvel na fase líquida.
- C.
instalar uma válvula para retirar amônia líquida do tanque, caso seja detectado um aumento de pressão no seu interior.
- D.
diminuir a área de contato entre as fases líquida e vapor no tanque de armazenamento.
- E.
diminuir a temperatura de armazenamento.
Um material sólido que contém umidade passa por um processo de secagem em batelada. A massa inicial do sólido úmido é de 50 kg, e a percentagem mássica de umidade nesse sólido é igual a 99% (em base úmida, ou seja, em relação à massa total do sólido úmido). Após o processo de secagem, verificou-se que a percentagem mássica de umidade no sólido em base úmida era de 98%. A massa total do sólido (incluindo a umidade restante) após o processo de secagem é, em quilogramas, igual a
- A.
49,5
- B.
49
- C.
45
- D.
25
- E.
24,5
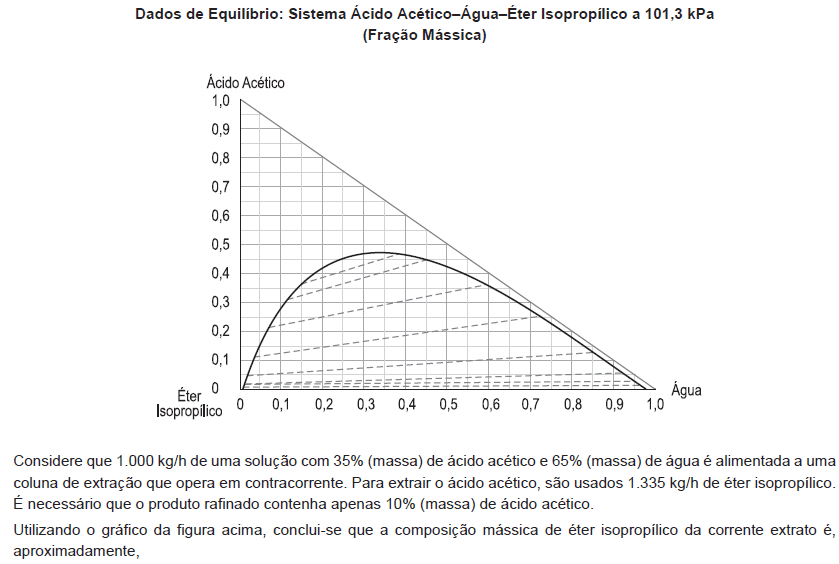
- A.
0,06
- B.
0,18
- C.
0,24
- D.
0,76
- E.
0,97
O campo de operação de uma coluna recheada é limitado por vazões da fase líquida e da fase vapor que podem acarretar problemas capazes de comprometer seriamente a operação da coluna. Entre essas anomalias de funcionamento, o gotejamento (weeping) causa uma diminuição significativa na eficiência do prato. O gotejamento é causado quando a fase
- A.
vapor tem uma velocidade muito baixa.
- B.
vapor tem uma velocidade muito alta.
- C.
líquida tem uma vazão muito baixa.
- D.
líquida tem uma velocidade muito alta.
- E.
líquida e a fase vapor têm a mesma velocidade.
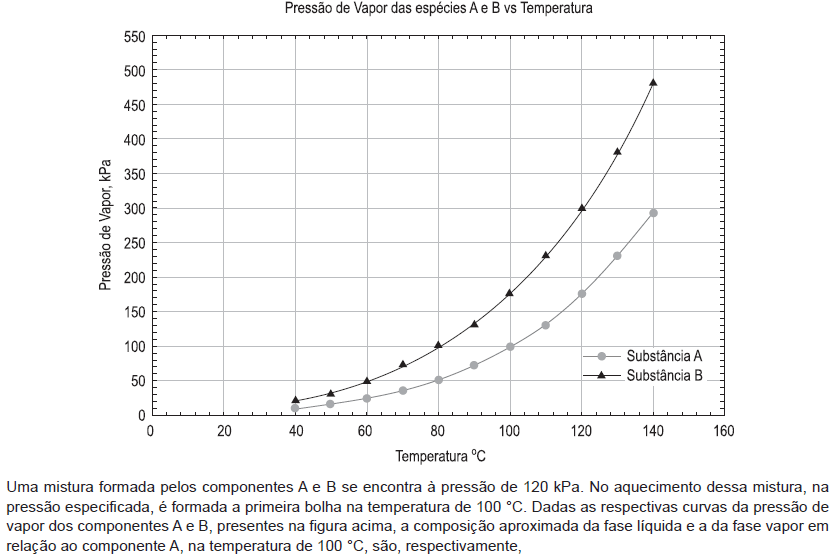
- A.
0,375 e 0,625
- B.
0,625 e 0,250
- C.
0,625 e 0,375
- D.
0,750 e 0,250
- E.
0,750 e 0,625
Para 1 mol de substância pura sofrendo uma transformação reversível de um estado inicial 1 a um estado final 2, dU = TdS − PdV, onde as variáveis U, S e V são, respectivamente, energia interna, entropia e volume molares, e as variáveis T e P são, respectivamente, temperatura e pressão. A relação de Maxwell obtida a partir da equação acima é
- A.

- B.

- C.

- D.

- E.

Os parâmetros a e b na equação de Van der Waals e outras equações cúbicas de estado representam, respectivamente,
- A.
atração molecular e polaridade molecular
- B.
atração molecular e tamanho molecular
- C.
peso molecular e polaridade molecular
- D.
tamanho molecular e peso molecular
- E.
tamanho molecular e velocidade molecular

- A.

- B.

- C.

- D.

- E.


- A.

- B.

- C.

- D.

- E.

Sabendo-se que as variáveis entalpia específica, entropia específica e pressão são representadas por H, S e P, respectivamente, em um diagrama de Mollier, a inclinação de uma linha isobárica é dada por
- A.

- B.

- C.

- D.
zero
- E.
infinito


