Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
A Lei de Avogadro foi decorrente da hipótese que sustentava que dois recipientes, de mesmo(a) _________, contendo _________ diferentes, à mesma temperatura e pressão, deveriam conter o mesmo número de _________.
Assinale a alternativa que completa correta e respectivamente as lacunas da sentença acima.
- A.
massa gases moléculas
- B.
massa líquidos partículas
- C.
massa gases partículas
- D.
volume líquidos partículas
- E.
volume gases moléculas
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
Ao ser submetida a condições adequadas, a função orgânica álcool reage com ácidos carboxílicos para a formação de ésteres. Um exemplo desse fenômeno é a esterificação de ácidos graxos para a síntese de biodiesel. Acerca desse sistema, assinale a opção correta.
- A.
Na reação de hidrólise de um éster, não é possível identificar os reagentes que originavam o éster (ácido carboxílico e álcoois correspondentes).
- B.
Compostos com função álcool são totalmente solúveis em água.
- C.
Triacilglicerídeos são exemplos de ácidos carboxílicos graxos.
- D.
Ácidos carboxílicos e alcoóis interagem entre si por forças intensas do tipo dipolo-induzido.
- E.
As reações de saponificação ocorrem, em meio básico, paralelamente às reações de esterificação.
Assinale a opção que apresenta a representação da conformação mais estável do trans- dimetilciclopropano na projeção de Newman.
- A.

- B.

- C.

- D.

- E.

Em condições adequadas, na reação de adição eletrofílica em que o bromo (Br2) reage com o but-2-eno,
- A.
formam-se alquinos por duas reações de eliminação consecutivas.
- B.
formam-se alcoóis, pois geralmente são mais reativos.
- C.
há apenas uma adição, pois questões estéreas impedem outras adições.
- D.
é mínima a taxa de reação, dada a imiscibilidade dos reagentes.
- E.
formam-se di-haletos vicinais com estereoquímica anti.
Assinale a opção que apresenta o produto majoritário de desidratação do 3,3-dimetil 2-butanol.
- A.
2,3-dimetil 2-buteno
- B.
2,2-dimetil 1-buteno
- C.
2,3-dimetil 1-buteno
- D.
2,2-bismetil 2-buteno
- E.
1,2-dimetil 3-buteno
Os compostos aromáticos
- A.
são mais reativos que os alquenos convencionais.
- B.
apresentam relativa estabilidade por deslocalizar elétrons pi em sua estrutura.
- C.
realizam reações de adição e substituição eletrofílicas.
- D.
possuem 3 elétrons pi deslocalizados em sua estrutura.
- E.
não obedecem a regra de Hückel, por serem aromáticos.
Em reações de substituição nucleofílica Sn2 entre um haleto de alquila e um nucleófilo,
- A.
apenas a concentração do nucleófilo influencia a cinética da reação.
- B.
entre as ligações químicas do haleto de alquila não há polarização.
- C.
a quebra da ligação do haleto de alquila é do tipo heterolítica.
- D.
a cinética da reação é unimolecular.
- E.
o haleto ligado à cadeia alquílica representa um centro eletrofílico.
Com relação aos alcanos, assinale a opção correta.
- A.
As forças intermoleculares que regem as propriedades desses compostos são do tipo dipolo-permanente.
- B.
Por serem muito polares, esses compostos são pouco solúveis em água.
- C.
São do tipo sp2 as ligações químicas carbono-carbono desses compostos.
- D.
Esses compostos promovem, de forma eficiente, reações de adição eletrofílica.
- E.
A introdução de ramificações em isomeros constitucionais diminuem o ponto de ebulição desses compostos.
Assinale a opção que apresenta a nomenclatura da IUPAC dos isômeros constitucionais dos álcoois com fórmula molecular C4H10O.
- A.
propan-2-ol, propan-1-ol e butan-2-ol
- B.
buten-2-ol, butan-1-ol e butan-2-ol
- C.
propan-2-ol, butan-1-ol e butan-2-ol
- D.
propen-2-ol, butan-1-ol e butan-2-ol
- E.
2-metil propan-2-ol, butan-1-ol e butan-2-ol
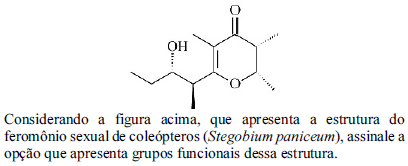
- A.
cetona e aldeído
- B.
cetona e álcool
- C.
ácido carboxílico cíclico e alquino
- D.
aromático e álcool
- E.
álcool e éster


