Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
A padronização de soluções de permanganato de potássio pode ser realizada a partir de uma solução de oxalato de sódio acidificada com ácido sulfúrico diluído, sob aquecimento:
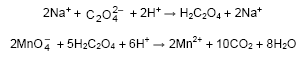
A padronização de 1,0 L de solução contendo 0,025 mol/L em permanganato de potássio necessitará, em massa de oxalato de sódio,
Dado: Massa molar do oxalato de sódio Na2C2O4 = 134 g/mol
- A.
8,4 g
- B.
7,2 g
- C.
3,1 g
- D.
2,5 g
- E.
1,0 g
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Todos os elementos de um mesmo grupo da tabela periódica apresentam, na forma não ionizada, o mesmo número de elétrons de valência.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2008
Na cromatografia de troca iônica, a principal função da coluna supressora é a de
- A.
aumentar a sensibilidade do detector.
- B.
diminuir o tempo de análise.
- C.
manter a pressão do sistema constante.
- D.
aumentar a velocidade de eluição.
- E.
diminuir a pressão total do sistema.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação Carlos Chagas (FCC) - 2008
Um padrão primário deve satisfazer os requisitos abaixo:
I. ser de fácil obtenção, purificação e secagem;
II. não deve se alterar no ar durante a pesagem;
III. ser facilmente solúvel nas condições de trabalho;
IV. ter baixa massa molecular para diminuir erros de pesagem.
É correto o que consta em
- A.
I e II, somente.
- B.
II e III, somente.
- C.
I, II e III, somente.
- D.
II, III e IV, somente.
- E.
I, II, III e IV.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Nas primeiras versões da tabela periódica, antes da descoberta da massa atômica, o ordenamento dos elementos era feito com base nos números atômicos.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2008
Em uma coluna de fase reversa, um soluto apresenta tempo de retenção de 31,3 min, enquanto uma espécie não retida requer 0,48 min para eluição. A fase móvel é constituída de 30%(v/v) de metanol e 70% de água. O fator de retenção é igual a
- A.
32
- B.
16
- C.
8
- D.
64
- E.
128
Considere a curva de titulação abaixo.
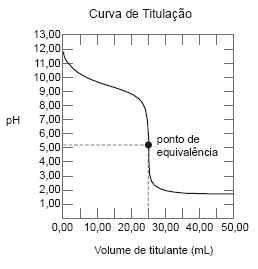
Entre os indicadores que apresentam as faixas de viragem de pH indicadas abaixo, aquele que causa menor erro nessa titulação é
- A.
0,2 – 1,8
- B.
4,2 – 6,3
- C.
8,0 – 9,6
- D.
9,3 – 10,5
- E.
11,1 – 12,7
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
De acordo com a teoria das ligações de valência, a maior parte dos gases nobres é capaz de formar compostos moleculares, uma vez que podem sofrer expansão da sua camada de valência.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2008
Os detectores de cromatografia líquida são de dois tipos básicos: universais ou de propriedades do soluto.
A alternativa que contém um detector de propriedade do soluto é:
- A.
Densidade.
- B.
Absorbância no UV.
- C.
Índice de refração.
- D.
Eletroquímico.
- E.
Condutividade Elétrica.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação Carlos Chagas (FCC) - 2008
A técnica da adição de padrão é aplicada nos métodos espectroscópicos e eletroquímicos quando se deseja
I. eliminar efeitos de matriz;
II. melhorar a resposta do instrumental analítico;
III. eliminar erros sistemáticos.
É correto o que consta em
- A.
I, somente.
- B.
II, somente.
- C.
I e II, somente.
- D.
II e III, somente.
- E.
I, II e III.


