Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Dois átomos que apresentem o mesmo número atômico mas diferentes números de nêutrons são elementos químicos diferentes.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2008
Na CLAE, a eluição por gradiente é usada
- A.
com um único solvente.
- B.
com água deionizada apenas.
- C.
quando se pretende determinar espécies polares.
- D.
para aumentar o processo de separação.
- E. quando um solvente não propicia uma eluição suficientemente rápida de todos os componentes.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação Carlos Chagas (FCC) - 2008
A amostragem de gases pode ser realizada a partir
I. do enchimento de um saco de amostragem com o gás;
II. da adsorção do gás por um líquido apropriado;
III. da adsorção do gás em um sólido apropriado.
É correto o que consta em
- A.
I, somente.
- B.
II, somente.
- C.
I e II, somente.
- D.
II e III, somente.
- E.
I, II e III.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Os elementos químicos pertencentes ao grupo dos halogênios caracterizam-se por serem os que apresentam as mais elevadas energia de ionização e eletronegatividade.
- E. Errado
- C. Certo
No Brasil, as técnicas de tratamento de água para abastecimento público contemplam, em geral, as seguintes etapas: clarificação, desinfecção, fluoretação e estabilização química. A respeito dessas etapas, julgue os itens que se seguem.
A estabilização química visa à neutralização de todos os compostos químicos utilizados nas demais etapas do tratamento da água, a fim de garantir que ela não tenha cheiro nem sabor.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2008
Na cromatografia líquida de alta eficiência não é possível a utilização de colunas capilares porque
- A.
o custo da análise aumentaria demasiadamente.
- B.
ainda não existe tecnologia para se produzir uma fase estacionária para este tipo de coluna.
- C.
a difusão em gases é 100 vezes mais lenta que a difusão em líquidos.
- D.
o diâmetro do canal do solvente é muito grande para ser percorrido por uma molécula de soluto em pequeno intervalo de tempo.
- E.
a sua utilização provocaria o aumento do número e pratos teóricos, diminuindo a eficiência, de acordo com a equação de Van Deemter.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação Carlos Chagas (FCC) - 2008
A meia-vida do radioisótopo 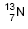 é 10,1 min. Assim, ao se passarem 40,4 min, de uma amostra de
é 10,1 min. Assim, ao se passarem 40,4 min, de uma amostra de 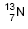 restará
restará
- A.
6,25%
- B.
12,5%
- C.
25,0%
- D.
50,0%
- E.
75,0%
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
No Brasil, as técnicas de tratamento de água para abastecimento público contemplam, em geral, as seguintes etapas: clarificação, desinfecção, fluoretação e estabilização química. A respeito dessas etapas, julgue os itens que se seguem.
A fluoretação propicia a eliminação de organismos patogênicos que possam estar presentes na água.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - FUNRIO Fundação de Apoio a Pesquisa, Ensino e Assistência (FUNRIO) - 2008
O detector de ionização de chama, na cromatografia a gás, não pode ser chamado de detector universal porque
- A.
é mais sensível com uma vazão menor.
- B.
é sensível apenas para halogênios.
- C. não apresenta sensibilidade a substâncias que não sejam hidrocarbonetos.
- D.
no apresenta sensibilidade para halogênios e aromáticos.
- E.
não é sensível para quantidades diminutas de amostra.
O carbeto de silício, SiC, é um abrasivo industrial que pode ser preparado pelo aquecimento de areia, SiO2, com grafita: SiO2 + 2C → SiC + CO2
Nessa reação, ocorre
- A.
redução do carbono, que perde elétrons.
- B.
oxidação do carbono, que perde elétrons.
- C.
redução do silício, que perde elétrons.
- D.
redução do silício, que ganha elétrons.
- E.
oxidação do silício, que perde elétrons.


