Questões de Química do ano 2008
Lista completa de Questões de Química do ano 2008 para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
Uma solução de CrCl2 é empregada num processo de cromação de um objeto metálico cuja massa antes era 1000 g e depois de transcorridos 40 minutos do processo passou a ser 1010 g. Sabendo-se que 1 Faraday = 96.500 Coulomb, pode-se afirmar que a corrente i), em ampère, utilizada nesse processo foi de aproximadamente
- A. 7,7.
- B. 15,5.
- C. 464.
- D. 928.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
Dado que Kw = 1,0 × 10-14 e log 2,5 = 0,4, pode-se afirmar que uma solução aquosa 2 x10-3 M de Ba OH)2 apresenta
- A. concentração de íons hidroxila igual a 0,002 mol.L-1.
- B. pOH aproximadamente 11,6.
- C. pH aproximadamente 11,6.
- D. Kb aproximadamente 1,0 × 10-12.
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
O grau de ionização percentual de um ácido fraco monoprótico Ka=1 x 10-10) em uma solução 0,01 molar será de aproximadamente
- A. 1 x 10-4.
- B. 3,2 x 10-3.
- C. 0,10.
- D. 0,32.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
Em um sistema com volume constante de 1,5 litros, estão presentes, no equilíbrio, 4,5 mols de N2, 7,0 mols de O2 e 0,15 mols de NO2, conforme representado na equação química:
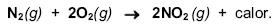
Nessas condições, o valor da constante de equilíbrio Kc) é aproximadamente
- A. 1,0 × 10-4.
- B. 1,5 × 10-4.
- C. 4,8 × 10-3.
- D. 7,1 × 10-3.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
O produto da reação do composto 2-propanol, em solução alcalina de KMnO4, tem fórmula molecular C3H6O. Esse composto é o a)
- A. propan-2-ona.
- B. 2-Propen-1-ol.
- C. propanal
- D. oxitano.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
Uma solução de bromo em benzeno é estável por muito tempo. Porém, ao se adicionar FeBr3 à solução, uma reação bastante rápida ocorre. Em relação a essa situação, constata-se que
- A. o único produto da reação de FeBr3 com benzeno é o bromobenzeno.
- B. o bromo atua como catalisador, facilitando o ataque nucleófilo do FeBr3 ao anel benzênico.
- C. é necessário adicionar uma quantidade estequiométrica de FeBr3 para que a reação se complete.
- D. o FeBr3 atua como catalisador, permitindo que um átomo de bromo promova um ataque eletrófílo ao anel benzênico.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
Observe a reação:
- A. oxidado.
- B. reduzido
- C. neutralizado.
- D. desintegrado.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
O TiO2 pode ser obtido pela reação do minério FeTiO3 com H2SO4, como representado a seguir:

O fato de o óxido de titânio IV ser opaco e não tóxico torna-o adequado para ser utilizado como pigmento em plásticos e tintas. No processamento de oito toneladas de FeTiO3, foram obtidos 3,68 x103 kg de TiO2. Então, o rendimento dessa reação química foi de aproximadamente
- A. 46%
- B. 58%
- C. 60%
- D. 87%.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
Entre as substâncias formadas pela união de átomos de boro e de flúor, encontra-se o trifluoreto de boro, BF3. Analisando-se as propriedades dessas espécies, chega-se à seguinte conclusão:
- A. sendo o flúor menos eletronegativo que o boro, as ligações B – F são polares.
- B.
como a geometria da molécula BF3 é triangular plana, as três ligações B – F são apolares.
- C.
dada a grande diferença de eletroafinidades, as ligações na espécie BF3 são iônicas.
- D.
a molécula BF3 é apolar porque seu momento dipolar é nulo.
Química - Reações, Soluções e Transformações Químicas - Fundação de Amparo e Desenvolvimento da Pesquisa (FADESP) - 2008
O espectro de emissão do hidrogênio cobre uma larga gama de comprimentos de onda λ). Desse modo, numa transição eletrônica do estado inicial de n=5 para o final de n=2 n= n.º quântico principal), haverá emissão de
- A. elétrons.
- B. fótons.
- C. prótons.
- D. nêutrons.


