Questões sobre Reações, Soluções e Transformações Químicas
Lista completa de Questões sobre Reações, Soluções e Transformações Químicas para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2012
A respeito da norma vigente que estabelece as especificações para álcool etílico anidro combustível (AEAC) e álcool etílico hidratado combustível (AEHC), julgue os itens subsequentes.
De acordo com a referida norma, o ensaio de acidez total deve ser realizado, uma vez que o resultado da oxidação do etanol é o ácido acético e este impacta na qualidade do combustível.
- C. Certo
- E. Errado
Uma solução diluída de ácido sulfúrico foi empregada no pré-tratamento de material lignocelulósico por via ácida. Tal solução foi preparada diluindo-se 200 vezes uma solução de ácido sulfúrico, com concentração igual a 196 g/L.
Após o pré-tratamento ácido, seguiu-se uma etapa de filtração, em que foram obtidos 200 m3 de hidrolisado ácido rico em pentoses. Com o intuito de aproveitar esse hidrolisado para a produção de etanol de segunda geração a partir da fermentação das pentoses, realizou-se um tratamento visando à neutralização, empregando-se óxido de cálcio, sendo formado um precipitado branco. Após outra etapa de filtração para a remoção do precipitado, obteve-se o hidrolisado neutralizado e clarificado.
A partir desses dados e assumindo que a acidez do hidrolisado decorreu exclusivamente da dissociação total do ácido sulfúrico, conclui-se que o pH e a massa de precipitado formado na reação de neutralização foram, respectivamente,
- A. 0,2 e 27,2 kg
- B. 0,2 e 272 kg
- C. 2,0 e 88 kg
- D. 2,0 e 136 kg
- E. 2,0 e 272 kg
 O reduzido teor de enxofre no gás natural NÃO contribui significativamente para a formação de
O reduzido teor de enxofre no gás natural NÃO contribui significativamente para a formação de
- A. gás sulfídrico na atmosfera, que é a principal substância responsável pela formação de chuva ácida.
- B. anidrido sulfúrico na atmosfera, que é a única substância responsável pela formação de chuva ácida.
- C. anidrido sulfuroso na atmosfera, que é a única substância responsável pela formação de chuva ácida.
- D. anidridos sulfúrico e sulfídrico na atmosfera, que são duas das principais substâncias responsáveis pela formação de chuva ácida.
- E. anidridos sulfúrico e sulfuroso na atmosfera, que são duas das principais substâncias responsáveis pela formação de chuva ácida.
Em um laboratório de análises químicas, um técnico misturou duas soluções de ácido sulfúrico, sendo uma sete vezes mais concentrada que a outra. O volume final obtido foi de 200 mL, e o volume da mais diluída foi três vezes maior que o da mais concentrada. Posteriormente, uma alíquota de 10,0 mL foi titulada com uma solução padronizada de hidróxido de sódio de concentração 0,100 mol/L. O volume de base gasto foi de 20,0 mL. Qual é a concentração das duas soluções iniciais?
- A. 0,14 mol/L e 0,02 mol/L
- B. 0,28 mol/L e 0,04 mol/L
- C. 0,56 mol/L e 0,08 mol/L
- D. 1,12 mol/L e 0,16 mol/L
- E. 2,24 mol/L e 0,32 mol/L

- A.
Pb
- B.
PbO2
- C.
PbSO4
- D.
H2O
- E.
H2SO4
A adsorção de moléculas sobre a superfície de um sólido pode ser classificada em dois tipos: adsorção física e a química. Na adsorção física, agem interações de Van der Waals. Na adsorção química, as interações são mais fortes, podendo levar à quebra de ligações atômicas nas moléculas adsorvidas. O processo de absorção
- A. física, com diversas camadas de moléculas adsorvidas, é adequadamente modelado pela isoterma de Langmuir.
- B. física, com diversas camadas de moléculas adsorvidas, é adequadamente modelado pelas isotermas de Langmuir e BET.
- C. física, com apenas uma camada de moléculas adsorvida, é inadequadamente modelado pelas isotermas de BET e Langmuir.
- D. química, com apenas uma camada de moléculas adsorvida, é adequadamente modelado pela isoterma de Langmuir.
- E. química, com diversas camadas de moléculas adsorvidas, é adequadamente modelado pelas isotermas de Langmuir e BET.

- A. P hexano; Q butanol; R Hg
- B. P Hg; Q butanol; R hexano
- C. P butanol; Q hexano; R Hg
- D. P Hg; Q hexano; R butanol
- E. P butanol; Q Hg; R hexano
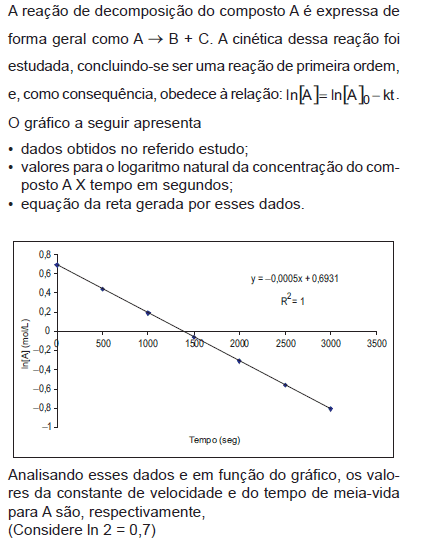
- A. 0,0005 s-1 e 1400 s
- B. 0,0005 s-1 e 0,693 s
- C. 0,693 s-1 e 0,0005 s
- D. 0,693 s-1 e 1,0 s
- E. 1,0 s-1 e 2,0 s
Três soluções, I, II e III, foram preparadas adicionando-se uma mesma quantidade de matéria dos seguintes solutos: solução I ureia ((NH2)2CO); solução II ácido sulfúrico (H2SO4); solução III ácido acético (CH3COOH). As três soluções foram preparadas com uma mesma massa de solvente, a saber, água. Considerando o comportamento ideal e definindo as temperaturas de início de congelamento das três soluções como: TI, TII e TIII, respectivamente, a relação entre estas temperaturas será
- A. TI = TIII< TII
- B. TI < TIII< TII
- C. TII = TIII< TI
- D. TI = TII = TIII
- E. TII < TIII< TI
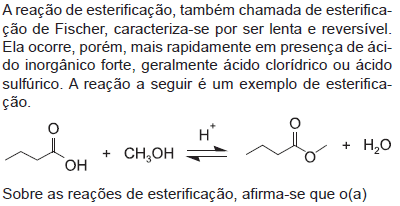
- A.
excesso de água não favorece a reação na direção do metanol.
- B.
ácido inorgânico deve ser usado em quantidade equimolecular, pois ele efetivamente participa como reagente.
- C.
álcool atua como uma espécie deficiente em elétrons que ataca o carbono do ácido.
- D.
álcool terciário, nesse tipo de reação, é mais reativo que o álcool primário.
- E.
reação na direção do metanol representa a hidrólise do éster.


