Questões sobre Reações, Soluções e Transformações Químicas
Lista completa de Questões sobre Reações, Soluções e Transformações Químicas para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Para demonstrar o efeito da superfície de contato e dos catalisadores em uma reação química, pode-se realizar alguns experimentos, como os descritos a seguir:
I. dissolução de um comprimido efervescente em água.
II. decomposição da água oxigenada com dióxido de manganês.
As condições para esses experimentos que demonstram maior rapidez nas reações são:
- A.
comprimido inteiro em I e decomposição na ausência de MnO2em II.
- B.
comprimido triturado em I e decomposição na ausência de MnO2 em II.
- C.
comprimido triturado em I e decomposição na presença de MnO2 em II.
- D.
comprimido inteiro em I e decomposição na presença de MnO2 em II.
- E.
comprimido inteiro em I e decomposição independente do MnO2 em II.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
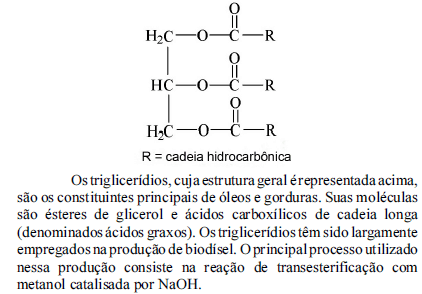
A respeito dos compostos e da reação de transesterificação mencionada, julgue os itens de 111 a 115.
Em uma reação de transesterificação, o emprego de um excesso de metanol contribui para aumentar o rendimento desta, porque desloca o equilíbrio na direção da formação dos produtos.
- C. Certo
- E. Errado
O uso de solução sulfocrômica para limpeza de vidrarias não é mais recomendado pela sua toxicidade e grau de poluição ao meio ambiente. Quando há necessidade, assinale a solução que a substitui:
- A.
Solução alcoólica de hidróxido de potássio.
- B.
Solução alcoólica de hidróxido de potássio.
- C.
Solução diluída de ácido acético.
- D.
Solução concentrada de cloreto de sódio.
- E.
Solução de permanganato de potássio dissolvido em qualquer composto orgânico insaturado.
O oxigênio utilizado em hospitais é obtido a partir do ar atmosférico. Nesse processo, o ar é liquefeito para se conseguir a separação de seus componentes, pela destilação fracionada. As condições de temperatura e pressão que permitem a liquefação do ar são
- A.
baixa temperatura e baixa pressão.
- B.
alta temperatura e alta pressão.
- C.
alta temperatura e baixa pressão.
- D.
alta temperatura e pressão atmosférica normal.
- E.
baixa temperatura e alta pressão.
Para demonstrar o processo de tratamento da água de abastecimento público para seus alunos, um professor deve utilizar experimentos que envolvam os seguintes procedimentos, nessa ordem:
- A.
filtração, coagulação e decantação.
- B.
decantação, filtração e coagulação.
- C.
decantação, coagulação e filtração.
- D.
filtração, decantação e coagulação.
- E.
coagulação, decantação e filtração.
Quando se prepara um suco a partir de uma mistura em pó, certamente pode-se desenvolver a articulação da experiência cotidiana com os seguintes conhecimentos químicos:
- A.
modelos atômicos.
- B.
diluição e equilíbrio químico.
- C.
hidrocarbonetos e álcoois.
- D.
dissolução e concentração de soluções.
- E.
partículas constituintes do átomo.
Atenção: Considere os dados abaixo para responder às questões de números 27 e 28.

A liquefação da água está corretamente representada pelo diagrama de energia
- A.

- B.

- C.

- D.

- E.

Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2011
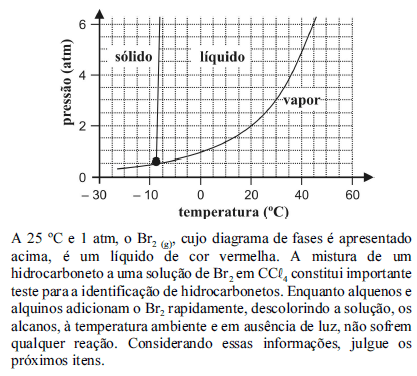
A 1 atm, as temperaturas de fusão e ebulição do Br2 são superiores a -5 ºC e 20 ºC, respectivamente.
- C. Certo
- E. Errado
O formaldeído (massa molecular = 30g/mol) é utilizado para esterilizar materiais de laboratório. Quando em concentrações superiores a 0,5mmol/L, polimeriza-se formando o paraformaldeído, um precipitado branco. Qual é a quantidade máxima de formaldeído que 100mL de uma solução pode conter, para que NÃO haja formação de precipitado?
- A.
15g
- B.
1,5g
- C.
150mg
- D.
15mg
- E.
1,5mg
Atenção: Considere os dados abaixo para responder às questões de números 27 e 28.
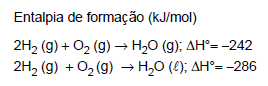
A combustão do GLP (gás liquefeito de petróleo) libera 4,5 × 104 kJ por quilograma de gás. Assim, para vaporizar 1 mol de água (cerca de 18 g) é necessário queimar uma massa, em gramas, desse gás correspondente a, aproximadamente,
- A.
3,29.
- B.
2,50.
- C.
1,58.
- D.
1,23.
- E.
0,98.


