Questões de Química da Fundação CESGRANRIO (CESGRANRIO)
Lista completa de Questões de Química da Fundação CESGRANRIO (CESGRANRIO) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
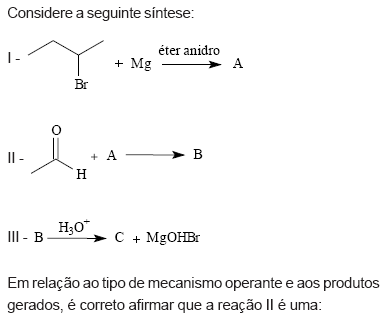
- A.
adição nucleofílica e C é o 2-hexanol.
- B.
adição eletrofílica e C é o 3-metil-2-pentanol.
- C.
adição nucleofílica e C é o 3-metil-2-pentanol.
- D.
adição eletrofílica e A é o brometo de butilmagnésio.
- E.
substituição nucleofílica e A é o brometo de 2- butilmagnésio.
A concentração de íons OH− presentes em uma solução de HCl 0,01M, assumindo como desprezível a contribuição dos íons H+ oriundos da dissociação da água, em mol/L, é:
- A.
10-16
- B.
10-14
- C.
10-12
- D.
10-10
- E.
10-2
O fenômeno da inversão térmica pode ser usado como um indicador natural do nível de poluição atmosférica nas grandes cidades. Neste fenômeno a camada de ar
- A.
quente encontra-se em movimento abaixo da camada de ar frio, facilitando a dispersão dos poluentes.
- B.
quente encontra-se estagnada abaixo da camada de ar frio, dificultando a dispersão dos poluentes.
- C.
quente encontra-se em movimento acima da camada de ar frio, facilitando a dispersão dos poluentes.
- D.
frio encontra-se em movimento acima da camada de ar quente, dificultando a dispersão dos poluentes.
- E.
frio encontra-se estagnada abaixo da camada de ar quente, dificultando a dispersão dos poluentes.
O uso de revestimentos metálicos é uma das formas de se efetuar a proteção contra a corrosão, sendo a eletrodeposição um dos processos comumente utilizados. Nesse processo o material a ser protegido é colocado como catodo em uma cuba eletrolítica, onde o eletrólito contém um sal do metal a ser usado no revestimento. Considerando o uso de anodo inerte, qual dos seguintes sais em solução NÃO produzirá um revestimento metálico quando utilizado como eletrólito?
- A.
AgNO3
- B.
Ni(NO3)2
- C.
Cr(NO3)3
- D.
Sn(NO3)2
- E.
Al(NO3)3


- A.
K2S possuem maior caráter iônico que as do Na2S, pois o K+1 apresenta maior poder polarizante que o Na+1.
- B.
MgI2 possuem maior caráter covalente que as do MgBr2, pois o I−1 apresenta maior polarizabilidade que o Br−1.
- C.
Na2S possuem maior caráter iônico que as do K2S, pois o Na+1 apresenta maior poder polarizante que o K+1.
- D.
MgBr2 possuem maior caráter covalente que as do MgI2< /sub>, pois o Br−1 apresenta maior polarizabilidade que o I−1.
- E.
MgBr2 e do Na2S possuem igual caráter covalente, pois o poder polarizante do Na+1 é maior do que o do Mg+2 e a polarizabilidade do Br−1 é maior que a do S−2.
Para tratar um despejo industrial que contém cromato (CrO4 -2), foram propostas as seguintes rotas:
I - redução com FeSO4 em meio ácido, seguida de precipitação com NaOH e filtração;
II - reação com sais de Pb+2, seguida de filtração;
III - percolação por resina aniônica.
É(São) adequada(s) ao tratamento a(s) rota(s):
- A.
I, apenas.
- B.
II, apenas.
- C.
III, apenas.
- D.
I e II, apenas.
- E.
I, II e III.
Necessita-se analisar o teor de manganês em um efluente aquoso. Para isso foi preparada uma solução padrão de manganês que, por tratamento adequado, foi oxidado a MnO4 −1. A partir da solução de íons MnO4 −1 foram preparadas cinco soluções com concentrações de 1ppm, 5 ppm, 10 ppm, 15 ppm e 20 ppm de manganês, respectivamente. Essas soluções foram analisadas por espectrofotometria de absorção em comprimento de onda adequado e forneceram o gráfico abaixo. 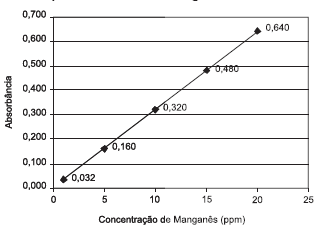 Em seguida, 10 mL do efluente aquoso foram tratados de modo a oxidar todo o manganês a MnO4 −1 e a solução resultante foi diluída até um volume final de 200 mL. Essa solução foi analisada por espectrofotometria de absorção, nas mesmas condições das soluções obtidas a partir da amostra padrão, fornecendo um valor de absorbância de 0,240. Considerando que não existem interferentes na amostra, a concentração de manganês, em ppm, no efluente aquoso é de:
Em seguida, 10 mL do efluente aquoso foram tratados de modo a oxidar todo o manganês a MnO4 −1 e a solução resultante foi diluída até um volume final de 200 mL. Essa solução foi analisada por espectrofotometria de absorção, nas mesmas condições das soluções obtidas a partir da amostra padrão, fornecendo um valor de absorbância de 0,240. Considerando que não existem interferentes na amostra, a concentração de manganês, em ppm, no efluente aquoso é de:
- A.
8
- B.
30
- C.
150
- D.
240
- E.
300

- A.
I e II.
- B.
I e III.
- C.
II e IV.
- D.
III e IV.
- E.
I, II e III.
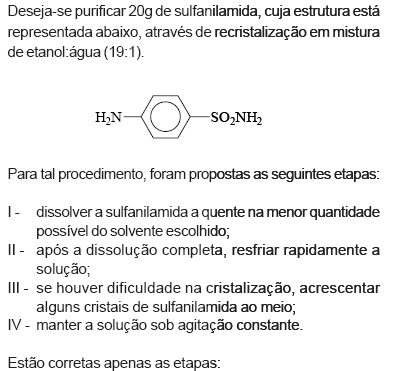
- A.
I e II.
- B.
I e III.
- C.
II e III.
- D.
II e IV.
- E.
III e IV.
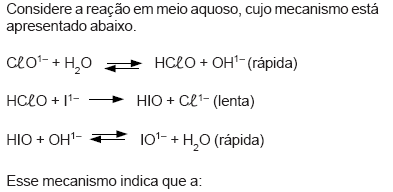
Considere a reação em meio aquoso, cujo mecanismo está apresentado abaixo.
- A.

- B.

- C.
molecularidade da reação correspondente à etapa lenta é 4.
- D.
água atua como uma Base de Lewis.
- E.
velocidade da reação independe do pH do meio.


