Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE)
Lista completa de Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
Considere a titulação de 20,0 mL de uma solução de HCR 0,080 mol/L com uma solução padrão de NaOH 0,10 mol/L. Com relação a esse sistema, é correto afirmar que
- A.
no ponto de equivalência, terá sido gasto um volume da solução de NaOH superior a 20 mL.
- B.
após a adição de 5,0 mL da solução de NaOH, a concentração de íons Na+ na mistura resultante será igual a 0,050 mol/L.
- C.
após a adição de 5,0 mL da solução de NaOH, a concentração de íons H+ na mistura resultante será igual a 0,050 mol/L.
- D.
após a adição de 5,0 mL da solução de NaOH, a concentração de íons Cl- na mistura resultante será igual a 0,064 mol/L.
- E.
no ponto de equivalência, a concentração de íons Na+ será superior à de íons Cl-.
Acerca de química orgânica, julgue os itens subsequentes.
O composto químico H3COC2H5 é uma cetona.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
Um técnico de laboratório realizou a padronização de 20,0 mL de uma solução de NaOH por meio da titulação com uma solução padrão de HCR 0,10 mol/L.
Considerando que foram gastos, no ponto de equivalência, 18,0 mL da solução ácida, assinale a opção que corresponde à concentração determinada pelo técnico para a solução de NaOH.- A.
0,18 mol/L
- B.
0,20 mol/L
- C.
0,90 mol/L
- D.
0,090 mol/L
- E.
0,10 mol/L
Acerca de química orgânica, julgue os itens subsequentes.
A nomenclatura química para a acetona é propanona.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
Considere que o ácido tereftálico seja um sólido à temperatura ambiente e que sua massa molar seja igual a 166 g/mol. Assinale a opção que apresenta a sequência correta de etapas a ser seguida na preparação de 100 mL de uma solução aquosa padrão 0,10 mol/L do referido ácido.
- A.
pesar 16,6 g do ácido; dissolver o sólido, em um béquer, em uma quantidade de água destilada inferior a 100 mL; transferir quantitativamente a mistura para um balão volumétrico de 100 mL e completar com água destilada
- B.
medir 100 mL de água destilada em um balão volumétrico; verter a água para um béquer; colocar o béquer contendo a água sobre uma balança analítica e adicionar, lentamente, o ácido até que a massa aumente em exatos 16,6 g
- C.
pesar 1,66 g do ácido; medir 100 mL de água destilada em um balão volumétrico; misturá-los em um béquer
- D.
pesar 16,6 g do ácido; medir 100 mL de água destilada em um balão volumétrico; misturá-los em um béquer
- E.
pesar 1,66 g do ácido; dissolver o sólido, em um béquer, em uma quantidade de água destilada inferior a 100 mL; transferir quantitativamente a mistura para um balão volumétrico de 100 mL e completar com água destilada
Acerca de química orgânica, julgue os itens subsequentes.
A reação entre um ácido carboxílico e um álcool, na presença de catalisador, formará um éter.
- C. Certo
- E. Errado
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
Um laboratorista deseja preparar uma série de padrões para construir uma curva de calibração para a determinação espectrométrica de um fármaco em solução e, para isso, ele dispõe de: a) uma solução padrão com concentração 1,00 × 10-2 mol/L do fármaco; b) pipetas volumétricas de 5,00 mL e de 10,00 mL; e c) balões volumétricos de 500 mL e de 1.000 mL.
Com relação a essa situação hipotética, assinale a opção correta, considerando a utilização exclusiva dos materiais disponíveis.- A.
A solução mais diluída que o laboratorista conseguirá preparar realizando apenas uma pipetagem terá concentração igual a 2,0 × 10-5 mol/L.
- B.
É possível a preparação de uma solução com concentração 1,0 × 10-5 mol/L.
- C.
Com duas pipetagens, a solução mais diluída que pode ser preparada terá concentração 1,0 × 10-7 mol/L.
- D.
Para preparar uma solução com concentração igual a 1,0 × 10-6mol/L, o laboratorista terá que realizar duas pipetagens.
- E.
Realizando apenas uma pipetagem, o laboratorista conseguirá preparar quatro soluções com diferentes concentrações para sua curva.
Acerca de química orgânica, julgue os itens subsequentes.
Considerando que a figura abaixo representa a molécula de vanilina, tradicionalmente conhecida como aroma de baunilha, é correto afirmar que a nomenclatura IUPAC para esse composto é 4-hidróxi-3-metoxi-benzaldeído.

- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2013
O volume Vm de um medicamento, que consiste em uma solução com concentração Cm de determinado princípio ativo, foi adicionado a um volume Vs de uma amostra de soro. A equação mais adequada para calcular a concentração Cf do princípio ativo na mistura obtida é
- A.
Cf = (Vm + Vs) / Vm· Cm
- B.
Cf = Vm· Cm/Vm
- C.
Cf = Vm· Cm/Vm
- D.
Cf = Vm· Cm/(Vm + Vs)
- E.
Cf = Vm· (Vm - Vs) /Cm
Acerca de química orgânica, julgue os itens subsequentes.
Considere que as estruturas 1 e 2 abaixo representam anestésicos locais com diferentes funções químicas em suas estruturas. Conforme essas representações, o composto 1 contém a função química éster, e o composto 2 a função química amida.
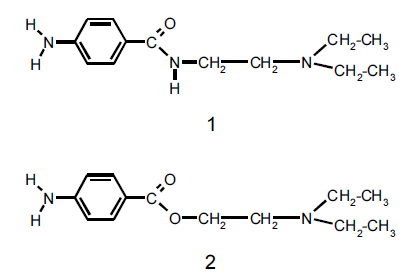
- C. Certo
- E. Errado


