Questões de Química da Fundação Getúlio Vargas (FGV)
Lista completa de Questões de Química da Fundação Getúlio Vargas (FGV) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Em 1923, o químico dinamarquês Johannes Brønsted (1879-1947) e o químico inglês Thomas Lowry (1874-1936) propuseram uma definição de ácidos e bases mais geral do que a proposta anteriormente por Arrhenius (1859-1927). O conceito de Brønsted- Lowry está baseado no fato de que a reação ácido-base envolve transferência de íons H+ de uma substância para outra.

- A.

- B.

- C.

- D.

- E.

A amônia atmosférica é de fundamental importância para a química ambiental, pois se trata de um composto capaz de neutralizar, em determinada extensão, gases ácidos e espécies ácidas adsorvidas em partículas.
Em uma determinada temperatura, a amônia apresenta pKb= 5. Nessas condições uma solução 0,1mol.L1 de amônia apresentará valor de pH igual a Dado: pKw = 14
- A. 3
- B. 8
- C. 10
- D. 11
- E. 13
Uma mistura gasosa de 10 mmol de CO e 10 mmol de H2O é colocada em um reator de 500 mL e aquecida até 500 °C, atingindo o equilíbrio:
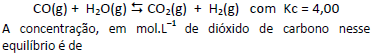
- A. 5,00 x 103.
- B. 1,33 x 102.
- C. 3,67 x 102.
- D. 4,00 x 102.
- E. 5,25 x 102.
A reação de cloro gasoso com uma base forte pode ser descrita pela equação

- A. 160 g.
- B. 60 g.
- C. 40 g.
- D. 10 g.
- E. 8 g.
Para uma determinada pratica em laboratório é necessário o preparo de 200 mL de solução 0,5 mol.L1 de ácido nítrico a partir de uma solução concentrada desse ácido. A solução concentrada é identificada por: 65%(m/m) e densidade 1,4g.cm3. O volume a ser utilizado dessa solução é de, aproximadamente,
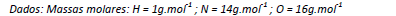
- A. 7 mL
- B. 12 mL
- C. 15 mL
- D. 22 mL
- E. 31 mL
A coleta de amostras de água é um dos elementos fundamentais no desenvolvimento de um Programa de Controle da Qualidade da Água. Embora considerada uma atividade simples alguns critérios técnicos como a exigência de pessoal treinado devem ser rigorosamente observados no processo de amostragem, a fim de que as amostras sejam representativas do nível de qualidade da água que se pretende determinar.
Assinale a opção que representa um requisito básico para a coleta deste tipo de amostras.
- A. Não há necessidade de planejamento prévio para definição dos pontos de coleta.
- B. A amostragem deve ser realizada diretamente de caixas, reservatórios, cisternas etc.
- C. As amostras coletadas para análises bacteriológicas devem ser feitas depois de qualquer coleta para outro tipo de análise.
- D. A coleta de água tratada deve ser realizada diretamente da torneira, fazendo-se a desinfecção com hipoclorito de sódio a 10%.
- E. As amostras coletadas para análise bacteriológica devem ser transportadas em caixas térmicas, em temperatura em torno de 30C.
Assinale a opção que indica a forma de nitrogênio que as plantas podem utilizar diretamente.
- A. Nitratos.
- B. Nitritos.
- C. Amônia.
- D. Gás N2.
- E. Metano.
Certo agente químico tem concentração de 10 ppm na água. Assinale a opção que descreve com mais precisão sua concentração.
- A. Existem 10 moléculas do agente químico em um milhão de moléculas de água
- B. Existem 10 moléculas do agente químico em um milhão de moléculas de água
- C. Existem 10 milhões de moléculas do agente químico em 1 litro de água
- D. Existem 10 moléculas de água em 1 milhão de moléculas do agente químico
- E. Existem 10 moléculas do agente químico em 10 milhões de moléculas de água.
O gás natural pode se originar de um reservatório de óleo ou de gás. O reservatório de gás é caracterizado como sendo o reservatório em que a jazida de petróleo, que contém a mistura de hidrocarbonetos encontra-se no estado gasoso em condições de reservatório. Esse tipo de reservatório se subdivide em:
I. reservatório de gás úmido;
II. reservatório de gás seco;
III reservatório de gás retrógrado.
A figura a seguir mostra um exemplo do diagrama de fase de um reservatório de gás úmido.

Em relação à figura acima, pode-se afirmar que:
- A.
o ponto crítico para uma mistura (gás-líquido) é o ponto na qual todos as propriedades do líquido e gás tornam-se idênticas.
- B.
a temperatura crítica da mistura é maior do que as temperaturas dos componentes da mistura.
- C.
no ponto 2 co-existem duas fases (gás + condensado).
- D.
no ponto 3 (condição de separador), a fração de líquido está entre 25% e 50%.
- E.
no ponto 3 (condição de separador), não existe nenhuma fração de condensado.
Uma canalização escoa gás natural do ponto A para o ponto B e para o ponto C, conforme mostrado na figura abaixo. No ponto B existe uma derivação que alimenta de gás o ponto D. Sabendo-se que a pressão inicial no ponto A é de 16 kgf/cm2, e as perdas de carga de cada trecho são AB = 2 kgf/cm2; BC = 3 kgf/cm2 e BD = 4 kgf/cm2, quais são as pressões finais nos pontos C e D?
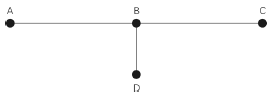
- A.
No ponto C, igual a 13 kgf/cm2, e, no ponto D, igual a 12 kgf/cm2
- B.
No ponto C, igual a 14 kgf/cm2, e, no ponto D, igual a 12 kgf/cm2
- C.
No ponto C, igual a 12 kgf/cm2, e, no ponto D, igual a 11 kgf/cm2
- D.
No ponto C, igual a 11 kgf/cm2, e, no ponto D, igual a 10 kgf/cm2
- E.
No ponto C, igual a 10 kgf/cm2, e, no ponto D, igual a 11 kgf/cm2


