Questões de Engenharia Química da Fundação Carlos Chagas (FCC)
Lista completa de Questões de Engenharia Química da Fundação Carlos Chagas (FCC) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
O dióxido de cloro ClO2 é um gás amarelo que pode ser condensado a um líquido vermelho de ponto de ebulição igual a 11 ºC. É um poderoso agente oxidante e de coloração, usado em grandes quantidades na purificação de água. É um bom alvejante, sendo empregado no branqueamento de celulose. É trinta vezes mais ativo que o cloro no branqueamento de cereais. É ainda empregado na fabricação de clorito de sódio NaClO2, que é também usado no branqueamento de tecidos e papel. Sua produção industrial pode ser representada pela seguinte equação:
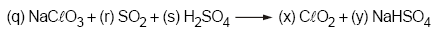
Os coeficientes mínimos (e inteiros) do balanceamento da equação correspondentes a q, r, s, x e y são, respectivamente,
- A.
2; 1; 2; 2 e 2.
- B.
2; 2; 1; 1 e 2.
- C.
2; 2; 1; 2 e 2.
- D.
2; 1; 1; 2 e 2.
- E.
2; 1; 1; 1 e 2.
Considere as figuras abaixo.
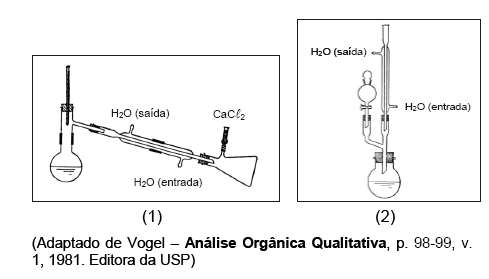
A figura
I. (1) mostra uma unidade de destilação quando se deseja proteger o destilado da umidade atmosférica com cloreto de cálcio anidro.
II. (2) mostra o uso de adaptador de duas bocas, disposto de modo a ter, simultaneamente, a adição de um reagente de um funil de separação e refluxo.
III. (1) e a figura (2) apresentam esquemas que podem ser utilizados para destilação.
Está correto o que se afirma APENAS em
- A.
I.
- B.
I e II.
- C.
II.
- D.
II e III.
- E.
III.
Considere a figura e as informações a seguir.

"A polimerização contínua do estireno pelo método a granel está representada na figura acima. Estireno purificado entra nos (2) com agitação e aquecimento/resfriamento para se manter a temperatura do processo entre 80 – 82 °C. Uma polimerização preliminar em até 32 – 35% do monômero ocorre nos (2). Então, a mistura líquida escoa abaixo através do (3). Lá a polimerização é completada. Este equipamento possui seis seções ao longo de seu comprimento, cada uma dotada de camisa de aquecimento (4) e serpentina para a reação da mistura. A temperatura sobe gradualmente de 100 ºC no topo para 200 ºC no fundo, que possui um aquecedor elétrico (5) para aquecimento adicional. O produto final, poliestireno fundido, sai continuamente do fundo do equipamento para um transportador de rosca (6), do qual sai em forma de bastão para um transportador de correias (7), onde o material resfria. O poliestireno resfriado é então, cortado em pedaços por uma faca rotatória (8) e moído em um moinho (9) e depois armazenado. Os vapores de estireno não reagido no (3) e nos (2) são enviados para o (1). Dali, o estireno líquido é então retificado e reciclado para os (2)."
Os equipamentos (1), (2) e (3) são, respectivamente,
- A.
condensador; reatores e reator tipo filme descendente.
- B.
aquecedor, tanques de armazenamento e coluna de destilação.
- C.
reator, tanques de armazenamento e coluna de destilação.
- D.
aquecedor, reatores e reator tipo filme descendente.
- E.
condensador, tanques de armazenamento e coluna de destilação.
Instruções: Considere as reações seqüenciais com radicais livres, abaixo, para responder às questões de números 55 e 56.
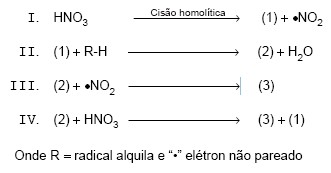
As espécies químicas (1), (2) e (3) são, respectivamente,
- A.
OH; R; R − NO2
- B.
H2O; R; NO2
- C.
OH; R; R − NO2
- D.
H2O; R; NO2
- E.
OH; R; NO2
Instruções: Considere as reações seqüenciais com radicais livres, abaixo, para responder às questões de números 55 e 56.
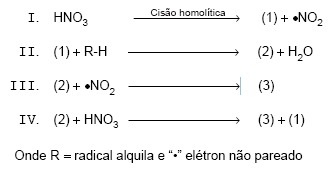
As reações III e IV representam, nas reações seqüenciais, respectivamente,
- A.
polimerização e redução.
- B.
propagação e terminação.
- C.
terminação e propagação.
- D.
polimerização e oxidação.
- E.
propagação e oxidação.
O calor de hidrogenação do propeno, a 25 °C e 1 atm,
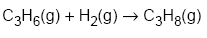
é, em kJ/mol,
Dados: calores de combustão a 25 °C e 1 atm
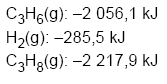
- A.
247,5
- B.
185,6
- C.
123,7
- D.
−247,5
- E.
–123,7
Considere as seguintes reações seqüenciais:
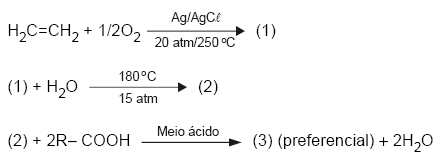
Onde : R = radical alquila de ácido graxo
Os compostos identificados por (1), (2) e (3) são, respectivamente,
- A.
óxido de etileno, etilenoglicol e diéster graxo do etilenoglicol.
- B.
gás carbônico, etilenoglicol e sal de ácido graxo.
- C.
etilenoglicol, óxido de etileno e sal de ácido graxo.
- D.
óxido de etileno, gás carbônico e sal de ácido graxo.
- E.
etileno, etilenoglicol e diéster graxo do etilenoglicol.
Considere as tabelas e o texto a seguir.
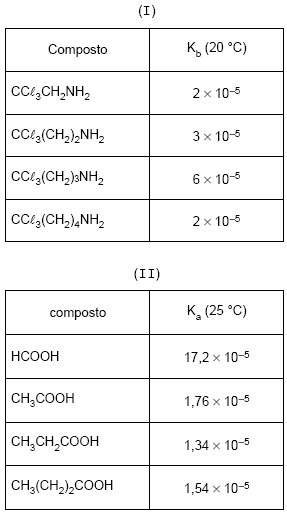

- A.
diminui, aumenta, efeito indutivo positivo e efeito indutivo negativo.
- B.
aumenta, diminui, efeito indutivo negativo e efeito indutivo positivo.
- C.
aumenta, diminui, efeito indutivo negativo e efeito indutivo negativo.
- D.
diminui, aumenta, efeito indutivo negativo e efeito indutivo positivo.
- E.
aumenta, diminui, efeito indutivo positivo e efeito indutivo negativo.
Com base nas entalpias padrão (ΔH°) para as reações abaixo, determine a entalpia padrão para a reação de formação do etano a partir do carbono sólido e do gás hidrogênio.

- A.
+276,9 kJ/mol
- B.
+776,7 kJ/mol
- C.
−276,9 kJ/mol
- D.
−83,7 kJ/mol
- E.
−3776,7 kJ/mol
Os alcanos halogenados C3H7Br, C3H7Cl, C3H7I, CH3Cl, C2H5Cl, em ordem crescente de ponto de ebulição são:
- A.
clorometano, cloroetano, 1-cloropropano, 1-bromopropano, 1-iodopropano.
- B.
clorometano, cloroetano, 1-cloropropano, 1-iodopropano, 1-bromopropano.
- C.
1-bromopropano, 1-iodopropano, 1-cloropropano, cloroetano, clorometano.
- D.
2-cloropropano, 2-bromobutano, 2-iodobutano, cloroetano, clorometano.
- E.
clorometano, cloroetano, 1-iodopropano, 1-bromopropano, 1-cloropropano.


