Questões de Engenharia Química da Fundação Carlos Chagas (FCC)
Lista completa de Questões de Engenharia Química da Fundação Carlos Chagas (FCC) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Utilize a tabela abaixo para responder às questões de números 31 e 32.

A análise da tabela permite afirmar que
I. se colocarmos em um gráfico os resultados de ΔH por mol de soluto em função da relação n1/n2, verificaremos que ΔH aumenta muito rapidamente a princípio, assumindo um valor limite assintótico à diluição infinita.
II. em uma pequena diluição é o solvente que sofre maior variação de entalpia.
III. em grandes diluições preponderá a variação de entalpia do soluto, pois este se encontra muito próximo ao seu estado puro.
Está correto o que se afirma APENAS em
- A.
I.
- B.
I e II.
- C.
I e III.
- D.
II.
- E.
II e III.
Utilize a tabela abaixo para responder às questões de números 31 e 32.
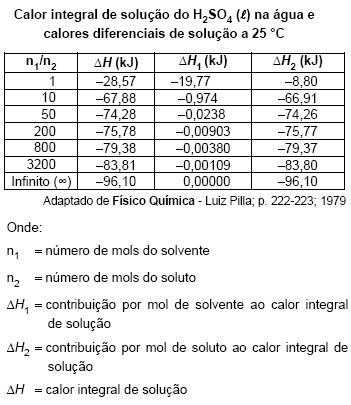
O calor de diluição de um mol de H2SO4 de 50 para 200 mols de água e de 50 para diluição infinita são respectivamente, em kJ,
- A.
−21,82; −1,50
- B.
1,50; 21,82
- C.
−1,50; 21,82
- D.
−1,50; −21,82
- E.
−21,82; 1,50
Instruções: Utilize o texto a seguir para responder às questões de números 34 e 35.
Um processo industrial de fabricação de 1,5-diaminonaftaleno fornece, num dado estágio de fabricação, uma solução aquosa de 1,5-diaminonaftaleno contendo 3% desta base em massa. A recuperação do produto é feita por extração da solução aquosa em contracorrente com éter etílico (éter isento) contendo 1% de água em massa. O extrato etéreo contém 15% da base e 4% de água em massa. A fase aquosa extraída (refinada) encerra quantidade desprezível da base, mas contém 3% de éter em massa.
A quantidade de éter isento de água por 1 000 kg de base extraída é aproximadamente, em kg:
- A.
4 500
- B.
5 000
- C.
6 400
- D.
7 700
- E.
9 100
Instruções: Utilize o texto a seguir para responder às questões de números 34 e 35.
Um processo industrial de fabricação de 1,5-diaminonaftaleno fornece, num dado estágio de fabricação, uma solução aquosa de 1,5-diaminonaftaleno contendo 3% desta base em massa. A recuperação do produto é feita por extração da solução aquosa em contracorrente com éter etílico (éter isento) contendo 1% de água em massa. O extrato etéreo contém 15% da base e 4% de água em massa. A fase aquosa extraída (refinada) encerra quantidade desprezível da base, mas contém 3% de éter em massa.
A porcentagem aproximada do éter utilizado contida na fase aquosa extraída (refinado) é, em %,
- A.
35
- B.
30
- C.
25
- D.
20
- E.
15
Considere a figura abaixo.
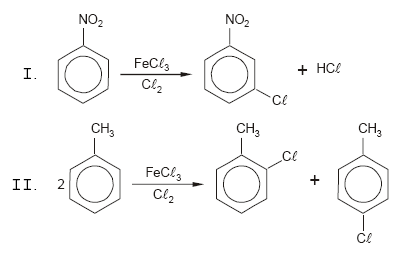
Os mecanismos de reação observados na obtenção dos produtos preferenciais são, em I e II, respectivamente, as substituições
- A.
por radical livre e nucleofílica.
- B.
por radical livre e eletrofílica.
- C.
nucleofílica e por radical livre.
- D.
nucleofílica e eletrofílica.
- E.
eletrofílica e nucleofílica.
Em virtude de restrições locais e dispondo apenas de fio de platina, bórax e chama de um bico de Bunsen, desejase determinar qualitativamente duas amostras contaminadas por metais desconhecidos. A primeira amostra forneceu uma pérola azul, tanto em chama redutora quanto em chama oxidante. A segunda amostra forneceu uma pérola azul esverdeada em chama oxidante e vermelha em chama redutora. Os possíveis metais contidos nas amostras I e II são, respectivamente,
- A.
cobalto e cobre.
- B.
silício e bismuto.
- C.
bismuto e silício.
- D.
tungstênio e cádmio.
- E.
cádmio e ferro.
Instruções: Utilize a figura e o enunciado a seguir para responder às questões de números 38 e 39.
A figura abaixo representa um tanque de estocagem de uma substância. A alimentação desse tanque é feita pelo topo através de uma linha de 2" que virá do ponto de alimentação e tem uma válvula de bloqueio e válvula de bloqueio de emergência (EBV) que deverá ser acionada quando o nível estiver muito alto. A malha apresenta um transmissor de nível eletrônico com registro e alarme de nível alto no painel. Possui, ainda, uma chave de nível muito alto com alarme na sala de controle que deverá acionar a válvula de bloqueio de emergência. A linha identificada por LP 4000 (3") é a sucção das bombas que mandam o material para o processo.
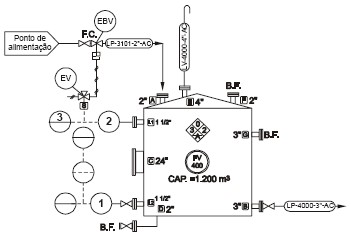
Os instrumentos representados por 1, 2 e 3 são, respectivamente,
- A.
transmissor de nível (campo); chave de nível muito alto (campo) e alarme de nível muito alto (painel).
- B.
transmissor de nível (painel); chave de nível baixo (painel); alarme de nível muito alto (campo).
- C.
registrador de nível (painel); chave de nível muito baixo (painel); alarme de nível muito alto (campo).
- D.
registrador de nível (campo); chave de nível muito alto (campo); alarme de nível muito alto (painel).
- E.
transmissor de nível (campo); chave de nível muito baixo (campo); alarme de nível muito alto (painel).
Instruções: Utilize a figura e o enunciado a seguir para responder às questões de números 38 e 39.
A figura abaixo representa um tanque de estocagem de uma substância. A alimentação desse tanque é feita pelo topo através de uma linha de 2" que virá do ponto de alimentação e tem uma válvula de bloqueio e válvula de bloqueio de emergência (EBV) que deverá ser acionada quando o nível estiver muito alto. A malha apresenta um transmissor de nível eletrônico com registro e alarme de nível alto no painel. Possui, ainda, uma chave de nível muito alto com alarme na sala de controle que deverá acionar a válvula de bloqueio de emergência. A linha identificada por LP 4000 (3") é a sucção das bombas que mandam o material para o processo.
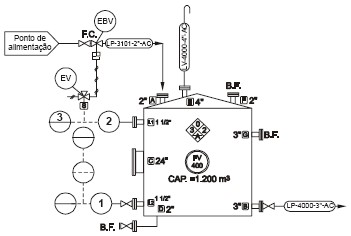
A substância contida no tanque FV 400 apresenta simbologia de identificação de risco recomendada pela NFPA (National Fire Protection Association). De acordo com esta representação, a substância armazenada no tanque apresenta as seguintes características:
- A.
risco de sérias lesões temporárias mesmo com tratamento médico imediato; não inflamável; material instável mas que não detona e que não reage violentamente com a água; permitido uso de água no combate ao fogo.
- B.
risco de irritação temporária mesmo com tratamento médico imediato; não inflamável; material instável mas que não detona e que reage violentamente com a água; proibido uso de água no combate ao fogo.
- C.
risco de sérias lesões temporárias mesmo com tratamento médico imediato; não inflamável; material instável mas que não detona e que reage violentamente com a água; proibido uso de água no combate ao fogo.
- D.
risco de sérias lesões temporárias mesmo com tratamento médico imediato; não inflamável; material instável mas que detona e que reage violentamente com a água; proibido uso de água no combate ao fogo.
- E.
risco de sérias lesões temporárias mesmo com tratamento médico imediato; inflamável; material instável mas que não detona e que reage violentamente com a água; proibido uso de água no combate ao fogo.
O pH estimado de uma solução de ácido acético (pKa = 4,74) 0,1 mol/L é:
- A.
5,24
- B.
2,37
- C.
4,24
- D.
2,87
- E.
1,87
Abaixo está representado o processo de transformação do SO2 em SO3
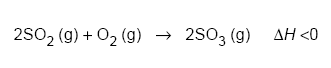
Dados experimentais de Kp em função da temperatura (no intervalo de 800 K a 1170 K) resultaram na seguinte equação:
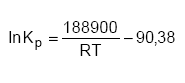
Com base nesta equação e no intervalo de temperatura indicado (onde Kp é a constante de equilíbrio como função de pressões parciais dos gases; R é a constante universal dos gases; T é a temperatura termodinâmica), é correto afirmar que:

Está correto o que se afirma APENAS em
- A.
I.
- B.
I, II e III.
- C.
II e III.
- D.
III e IV.
- E.
IV.


