Questões de Química do ano 2012
Lista completa de Questões de Química do ano 2012 para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Em 14 de agosto de 1996, Karen Wetterhahn, toxicologista e professora de Química do Darmouth College (New Hampshire, USA), derramou uma gotícula de dimetil-mercúrio na mão esquerda. Não se preocupou: estava usando luvas de látex. Mas um conhecimento que ela não tinha a matou. O dimetil-mercúrio era suficientemente volátil para penetrar na luva. Cinco meses depois, Karen começou a trombar com portas e dizer coisas ininteligíveis. Após três semanas hospitalizada, entrou em coma. Como uma toxicologista brilhante e minuciosa pôde ter um fim desses? Só domadores de leão são mortos por leões, justifi cou um dos pesquisadores que trabalhavam com ela. (adaptado de National Geographic, pág. 32, maio/2005). Sobre a toxicologia de produtos químicos, marque a opção incorreta.
- A.
Toxicologia é a ciência que estuda os efeitos nocivos decorrentes de interações de substâncias químicas com organismos vivos.
- B.
Sinergismo é o efeito combinado de duas ou mais substâncias que resulta em um efeito maior do que a soma dos efeitos de cada um administrado isoladamente.
- C.
Efeito teratogênico é causado por tóxicas que alteram o material genético da célula viva.
- D.
CL50 é a concentração letal de um gás suficiente para matar 50% da população a ele exposta.
- E.
A determinação da DL50 em espécies animais depende das variáveis: linhagem, idade, sexo, estado nutricional, e estado patológico.
Considerando a classificação adotada para os produtos considerados perigosos, feita com base no tipo de risco que apresentam e conforme as Recomendações para o Transporte de Produtos Perigosos das Nações Unidas, indique a opção incorreta.
- A.
A CLASSE 1 é constituída por substâncias explosivas e artigos explosivos.
- B.
A CLASSE 2 é constituída por substâncias que a 100 ºC tem pressão de vapor superior a 300 kPa ou que são completamente gasosas à temperatura de 50 ºC e pressão de 1013 kPa.
- C.
A CLASSE 3 é constituída por líquidos inflamáveis que tenham sido classificadas de forma diferente, em função de suas características perigosas.
- D.
A CLASSE 4 é constituída por sólidos inflamáveis ou substâncias que em contato com a água emitem gases inflamáveis.
- E.
A CLASSE 5 é constituída por substâncias oxidantes e peróxidos orgânicos.
O armazenamento de Produtos Perigosos requer cuidados especiais. Sobre esses cuidados, marque a opção incorreta.
- A.
Os produtos químicos devem ser acompanhados da identificação química, da ficha de Segurança e da ficha toxicológicas.
- B.
Produtos inflamáveis e corrosivos não devem ser armazenados em prateleiras elevadas.
- C.
No laboratório deve-se guardar somente quantidades mínimas de produtos químicos.
- D.
No armazenamento de produtos químicos, devese levar em consideração a incompatibilidade dos mesmos.
- E.
Se for utilizado armário fechado para armazenagem, este deve ser devidamente fechado para evitar troca de gases com o ambiente.
Química - Química, Tecnologia, Sociedade e Meio Ambiente - Escola de Administração Fazendária (ESAF) - 2012
O desenvolvimento econômico e tecnológico, associado ao aumento populacional, tem causado inúmeros problemas ao ambiente. Sobre esses problemas associados à Química, assinale a opção incorreta.
- A.
O efeito estufa é um fenômeno natural.
- B.
O buraco na camada de ozônio não indica ausência de ozônio na região.
- C.
É considerado lixo o material que não apresenta mais utilidade.
- D.
O tratamento de esgoto visa conferir às águas servidas condições mais próximas às águas utilizadas para abastecimento.
- E.
Uma chuva com pH igual a 6 é classifi cada como chuva ácida.
A Organização das Nações Unidas para a Educação, a Ciência e a Cultura UNESCO e a União Internacional de Química Pura e Aplicada IUPAC decidiram celebrar 2011 como o Ano Internacional da Química, com objetivo de destacar as conquistas e avanços da Química e o papel das mulheres nesta ciência. A Escolha deste ano é também uma homenagem à cientista Marie Curie, agraciada com o Prêmio Nobel de Física em 1903, pela descoberta da radioatividade, e agraciada com o Prêmio Nobel de Química de 1911, pela descoberta dos elementos químicos rádio e polônio. Sobre a radioatividade e seu amplo uso em nossa sociedade moderna, indique a opção incorreta.
- A.
A radiação α é igual ao núcleo dos átomos de 4He.
- B.
As emissões β são partículas como elétrons, emitidas por núcleos radioativos.
- C.
As emissões Ƴ' são constituídas por radiações eletromagnéticas como os raios X.
- D.
O pósitron é uma radiação semelhante ao próton, mas sem carga.
- E.
O neutrino é uma radiação semelhante ao elétron, mas sem carga.
A descoberta da radioatividade conferiu a Henri Becquerel, Pierre Curie e Marie Curie o Prêmio Nobel de Física em 1903. Esse fenômeno tem larga aplicação na sociedade moderna, das quais uma listada a seguir não está correta.
- A.
Determinação da idade de fósseis pela quantificação de átomos de 14C.
- B.
Determinação da idade da Terra pela quantificação de átomos de 206Pb.
- C.
Radioterapia utilizando 137Ce.
- D.
Irradiação de alimentos com 60Co.
- E.
Contador Geiger pelo uso de 239U.

- A.
4,0
- B.
4,4
- C.
4,7
- D.
5,0
- E.
6,0
Química - Reações, Soluções e Transformações Químicas - Escola de Administração Fazendária (ESAF) - 2012
O fluoreto de cálcio (CaF2) apresenta risco quando reage com ácido sulfúrico concentrado formando ácido fluorídrico, que provoca corrosão de frascos de vidro. Indique a opção que mostra a solubilidade do CaF2 , em mol/L, em uma solução de fluoreto de sódio (NaF) com concentração 0,010 mol/L.
Dado: Kps (CaF2) = 3,9 x 10-11- A.
2,1 x 10-4
- B.
4,4 x 10-6
- C.
3,9 x 10-7
- D.
2,1 x 10-8
- E.
3,9 x 10-9

- A.
I.
- B.
III.
- C.
II e III.
- D.
III e IV.
- E.
II, III e IV.
Química - Reações, Soluções e Transformações Químicas - Escola de Administração Fazendária (ESAF) - 2012
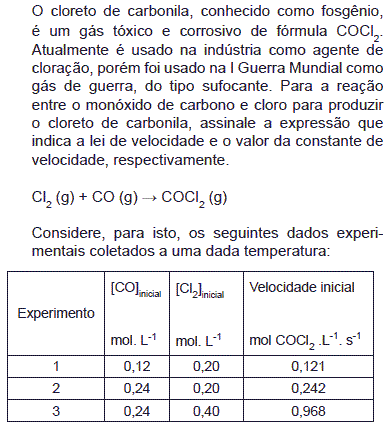
- A.
v = k [Cl2] k = 0,6 s-1
- B.
v = k [CO] k = 1,0 s-1
- C.
v = k [Cl2]2 k = 3,0 mol-1.L.s-1
- D.
v = k [CO][ Cl2] k = 5,0 mol-1.L.s-1
- E.
v = k [CO][ Cl2]2 k = 25 mol-2 .L2.s-1


