Questões sobre Reações, Soluções e Transformações Químicas
Lista completa de Questões sobre Reações, Soluções e Transformações Químicas para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Instituto de Planejamento e Apoio ao Desenvolvimento Tecnológico e Científico (IPAD) - 2006
O ácido salicílico é um composto oxigenado de grande potencialidade sintética. Quando tratado com excesso de metanol em meio ácido (ácido nítrico), sob refluxo, o ácido salicílico produz um composto odorífero. Sobre essa reação, é correto afirmar que:
- A.
a adição de salicilato de metila ao meio reacional aumentará a concentração do aldeído produzido.
- B.
o aumento da concentração de ácido nítrico resultará na diminuição da concentração do aldeído produzido.
- C.
será aumentada a quantidade de salicilato de metila, diminuindo-se a concentração do ácido salicílico.
- D.
é possível aumentar a produção do éster destilando a água obtida durante a reação.
- E.
a diminuição da concentração de ácido nítrico resultará na diminuição da concentração do aldeído produzido.
Química - Reações, Soluções e Transformações Químicas - Instituto de Planejamento e Apoio ao Desenvolvimento Tecnológico e Científico (IPAD) - 2006
Um papel indicador foi preparado através da imersão de tiras de papel de filtro em um extrato de azeitona-roxa (Syzygium cuminii). Quando testado em diferentes soluções, ele apresentou uma variação de cores, conforme mostrado no quadro abaixo.
Qual a cor será exibida por uma fita desse indicador ao entrar em contato com uma solução 0,1 M de acetato de sódio? (Ka do ácido acético = 2,0 10-5; log 7 = 0,84)
- A.
Lilás.
- B.
Azul.
- C.
Verde.
- D.
Amarelo.
- E.
Roxo.
Química - Reações, Soluções e Transformações Químicas - Núcleo de Computação Eletrônica UFRJ (NCE) - 2006
De modo geral, a temperatura utilizada na execução de um tratamento químico e a temperatura com que os documentos são conservados são parâmetros extremamente importantes, seja na restauração ou na conservação. Essa importância decorre do fato de que:
- A.
a velocidade de algumas reações aumenta com o aumento da temperatura;
- B.
a velocidade das reações químicas sempre diminui com o aumento da temperatura;
- C.
a velocidade das reações químicas sempre aumenta com o aumento da temperatura;
- D.
a velocidade de algumas reações diminui com o aumento da temperatura;
- E.
as reações que provocam a deterioração do acervo são exotérmicas.
Química - Reações, Soluções e Transformações Químicas - Núcleo de Computação Eletrônica UFRJ (NCE) - 2006
As mudanças das condições dos materiais são sempre muito importantes para o conservador. Essas mudanças podem ser classificadas como mudanças físicas ou químicas. Assinale a alternativa que mostra uma transformação física:
- A. evaporação da água existente no papel;
- B. oxidação dos materiais contendo ferro no acervo;
- C. fotodegradação do papel;
- D. deterioração do papel devido à acidez;
- E.
deterioração do acervo devido ao SO2, poluente atmosférico.
Química - Reações, Soluções e Transformações Químicas - Instituto de Planejamento e Apoio ao Desenvolvimento Tecnológico e Científico (IPAD) - 2006
A equação química a seguir, As4O6(s) + 6C(s) As4(g) + 6CO(g) mostra a reação de obtenção de arsênico, a partir da redução de As4O6 com carvão. O equilíbrio da reação será deslocado em direção aos produtos quando:
- A.
Adicionarmos monóxido de carbono.
- B.
Diminuirmos a concentração de arsênico.
- C.
Adicionarmos carvão.
- D.
Aumentarmos a concentração de arsênico.
- E.
Aumentarmos a concentração de As4O6 sólido.
O bicarbonato de sódio pode ser usado para combater a azia, diminuindo a acidez causada pelo excesso de ácido clorídrico existente no suco gástrico. Considerando a reação entre o bicarbonato de sódio e o ácido clorídrico representada abaixo, qual das alternativas é correta?
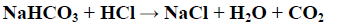
- A. NaHCO3 e HCl são produtos.
- B. NaHCO3 e H2O são reagentes.
- C. NaHCO3 e HCl são reagentes.
- D. HCl e H2O são produtos.
- E. NaCl, H2O e CO2 são reagentes.
Química - Reações, Soluções e Transformações Químicas - Instituto de Planejamento e Apoio ao Desenvolvimento Tecnológico e Científico (IPAD) - 2006
Do ponto de vista energético (ciclo de Haber-Born), a formação de um composto iônico envolve uma série de etapas. Os dados termodinâmicos são mostrados abaixo:
- A.
–437, sendo o processo favorável.
- B.
–315, sendo o processo favorável.
- C.
437, sendo o processo não favorável.
- D.
315, sendo o processo não favorável.
- E.
437, sendo o processo favorável.
Química - Reações, Soluções e Transformações Químicas - Instituto de Planejamento e Apoio ao Desenvolvimento Tecnológico e Científico (IPAD) - 2006
Quando o oxigênio dissolvido das águas é menor que o nível de saturação indica:
- A. presença de matéria orgânica.
- B. presença de algas.
- C. traços de metais.
- D. ausência de matéria orgânica.
- E. ausência de algas.
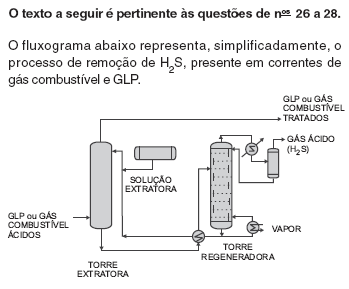
O gás ácido, separado no processo, apresenta um teor de H2S da ordem de 90% em volume e é enviado para Unidade de Recuperação de Enxofre. O aproveitamento do enxofre é feito pelo processo Clauss, cujas reações não balanceadas estão representadas abaixo.
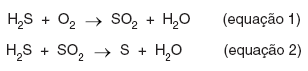
A respeito dessas reações, é correto afirmar que o(a):
- A.
H2S é o agente oxidante.
- B.
SO2 é o agente redutor.
- C.
enxofre é reduzido nas equações 1 e 2.
- D.
número de mols de elétrons transferidos na equação 2 balanceada é 6.
- E.
soma de todos os coeficientes mínimos das duas equações é 17.
Química - Reações, Soluções e Transformações Químicas - Instituto de Planejamento e Apoio ao Desenvolvimento Tecnológico e Científico (IPAD) - 2006
A determinação do teor de nitrogênio é importante para se fazer o balanço de nutrientes em um curso hídrico.
Analise as afirmativas abaixo em relação à presença de nitrogênio:
1. Quando na forma de nitratos está associado a doenças como metahemoglobinemia.
2. Em concentrações elevadas pode levar ao crescimento de algas chegando a eutroficação.
3. No processo bioquímico de conversão da amônia a nitrito e deste a nitrato libera muito oxigênio para o meio.
4. A forma de amônia é ideal para o crescimento dos peixes.
5. É indispensável ao crescimento de microorganismos dos esgotos
Está (ão) correta (as):
- A. 1 e 2, apenas.
- B. 1, 2 e 5, apenas.
- C. 2 e 5, apenas.
- D. 1, apenas
- E. 4 e 5, apenas.


