Questões sobre Reações, Soluções e Transformações Químicas
Lista completa de Questões sobre Reações, Soluções e Transformações Químicas para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Em um ambiente rico em oxigênio, dentro dos limites de explosividade, o fogo terá suas chamas
- A.
aumentadas, desprendendo mais luz e gerando maior quantidade de calor.
- B.
aumentadas, desprendendo mais luz e gerando menos quantidade de calor.
- C.
aumentadas, desprendendo menos luz e gerando menos quantidade de calor.
- D.
diminuídas, desprendendo mais luz e gerando maior quantidade de calor.
- E.
diminuídas, desprendendo menos luz e gerando menor quantidade de calor.
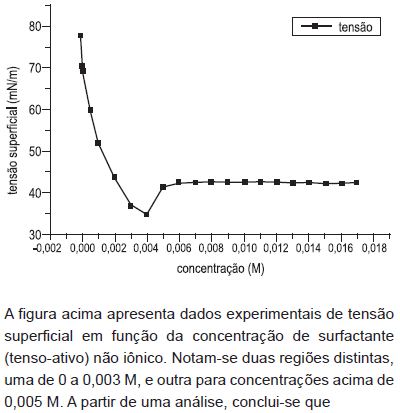
- A.
em concentrações baixas de surfactante, abaixo de 0,002 M, há a formação de micelas na solução.
- B.
em concentrações altas de surfactante, acima de 0,005 M, existe um sensivel aumento de carga na superfície líquido-ar.
- C.
a concentração de micelas aumenta para concentrações de surfactante acima de 0,005 M.
- D.
a concentração Kraft é aquela concentração de surfactante em que se inicia o processo de estabilização coloidal.
- E.
a CMC (Concentração Micelar Crítica) é definida pela máxima concentração, em torno de 0,018 M.

- A. 2,140
- B. 6,440
- C. 19,36
- D. 58,08
- E. 87,12
Admitindo-se que os componentes do fogo sejam simbolicamente representados por um triângulo, se uma das faces desse triângulo for retirada, o fogo
- A.
aumentará.
- B.
se espalhará.
- C.
será extinto.
- D.
produzirá mais chama.
- E.
causará uma explosão.
Um combustível líquido, após ter a sua temperatura elevada e atingir seu ponto de fulgor, gera
- A.
vapores inflamáveis, que reagirão com o oxigênio do ar produzindo fogo.
- B.
vapores inflamáveis, que reagirão com o gás carbônico do ar entrando em combustão.
- C.
vapores inflamáveis, que reagirão com o nitrogênio do ar produzindo chamas.
- D.
líquidos inflamáveis, que reagirão com o gás carbônico do ar entrando em combustão.
- E.
sólidos inflamáveis, que reagirão com o oxigênio do ar entrando em combustão.

- A. solução verdadeira, coloide e suspensão.
- B. suspensão, solução verdadeira e coloide.
- C. suspensão, coloide e solução verdadeira.
- D. coloide, solução verdadeira e suspensão.
- E. coloide, suspensão e solução verdadeira.
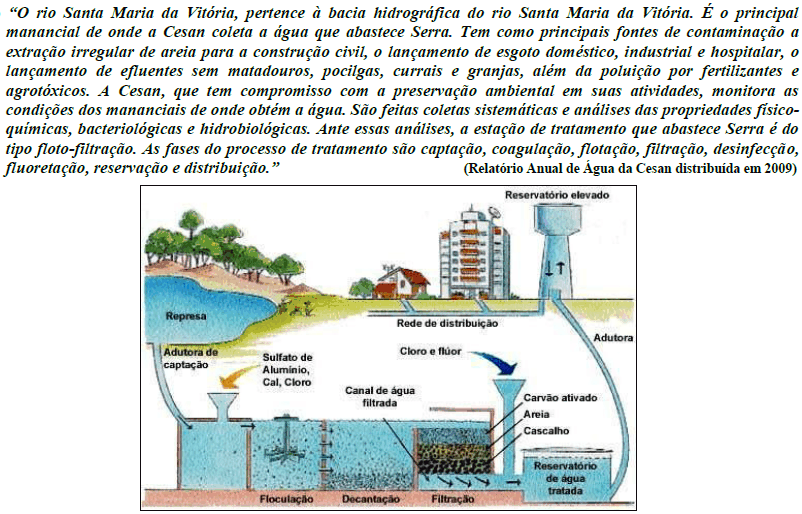
A fluoretação da água de abastecimento público representa uma das principais e mais importantes medidas de saúde pública no controle da cárie dentária. O flúor pode ser acrescentado à água potável a partir de seus compostos mais comuns: ácido fluorsilíaco (H2SiF6), fluoreto de cálcio (CaF2), fluorsilicato de sódio (Na2SiF6) e o fluoreto de sódio (NaF). A concentração ótima na maioria das cidades brasileiras (país tropical) é 0,7ppm. Considerando que uma pessoa deve tomar pelo menos dois litros de água por dia, qual a quantidade, em gramas, de flúor ingerimos?
- A.
1,4
- B.
1,4.103
- C.
7.101
- D.
1,4.103
- E.
7.101
Uma esfera sólida de diâmetro D e massa específica ρ1 é recoberta com uma camada de espessura uniforme D/2 constituída por um outro material sólido de massa específica ρ2. Tal corpo flutua em repouso na interface entre um líquido de massa específica ρ3 e um gás, ambos em equilíbrio estático. Os efeitos do gás podem ser desprezados. Para que o volume submerso do corpo seja igual ao volume da esfera de diâmetro D, o valor de ρ3 deve ser igual a
- A.
2p1 + 3p2
- B.
3p1 2p2
- C.
p1 + 7p2
- D.
5p1 3p2
- E.
p1 + 5p2

- A. Pb(NO3)2
- B. Pb(NO3)2 e NiSO4
- C. AgNO3
- D. AgNO3 e NiSO4
- E. AgNO3 e Pb(NO3)2
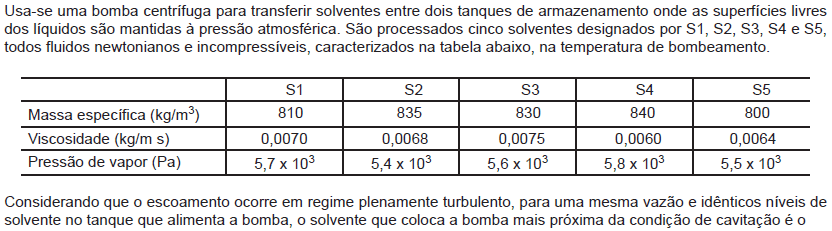
- A.
S1
- B.
S2
- C.
S3
- D.
S4
- E.
S5


