Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE)
Lista completa de Questões de Química da Centro de Seleção e de Promoção de Eventos UnB (CESPE) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Com relação à técnica de medição denominada PIV, julgue os itens seguintes.
Por meio do processamento de imagens, determinam-se as velocidades de várias zonas do escoamento.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Poluição e esgotamento das reservas de petróleo exigem a busca de fontes alternativas de energia. Processos como reações de fissão e fusão nucleares fornecem milhões de vezes mais energia que a obtida em combustões ou quaisquer outras reações químicas. Acerca desse tema, julgue os próximos itens.
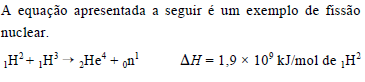
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
A produção de gasolina pelo tratamento primário do petróleo é muito pequena, mas o refino pode melhorar a quantidade e a qualidade da gasolina. Quanto à quantidade, podese obter gasolina submetendo frações menos voláteis ao craqueamento térmico na presença de catalisador. Normalmente, o catalisador é uma zeólita modificada. Outra forma de se obter gasolina é a síntese por alquilação.
Considerando o texto acima, assinale a opção correta.
- A.
Um exemplo de craqueamento é apresentado a seguir.
- B.
A reação
é um exemplo de cat. alquilação.
- C.
O processo primário de separação do petróleo é a destilação fracionada. No topo e na base da coluna de fracionamento, obtêm-se como resultado, respectivamente, as misturas menos e mais volátil.
- D.
Catalisadores heterogêneos, como as zeólitas, fornecem um novo caminho para a reação, com energia de ativação menor, o que permite que mais reagente se transforme em produto. Eles participam da reação, mas não são consumidos.
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Com relação à técnica de medição denominada PIV, julgue os itens seguintes.
Para a realização da medição, é necessária a introdução de partículas (tracers) no fluido e a gravação da imagem dos tracers em dois instantes distintos.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007

As duas substâncias citadas como produto da reação completa dos derivados do petróleo são componentes da atmosfera que apresentam a propriedade de reter a energia, na forma de calor, que a Terra reflete para o espaço, ocasionando o efeito estufa.
- C. Certo
- E. Errado
Politetrafluoretileno e polipropileno são exemplos de polímeros sintéticos compostos, nos quais cadeias e redes de pequenas unidades repetitivas formam moléculas gigantes. A respeito desse assunto, assinale a opção correta.
- A.
O monômero do polipropileno tem fórmula molecular C3H8.
- B.
Polímeros não possuem massas molares definidas.
- C.
Sacarose é o monômero dos polímeros naturais celulose e amido.
- D. Polímeros são substâncias compostas.
Química - Práticas Laboratoriais em química - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
Com relação à técnica de medição denominada PIV, julgue os itens seguintes.
Nesse tipo de técnica, é necessária a iluminação de uma fatia do escoamento para medição do campo de velocidade 3D.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007

Sabendo que M(C) = 12 g/mol e que M(H) = 1g/mol, para a combustão completa de 44 g de propano, presente no gás liquefeito de petróleo (GLP), são necessários 3 mol de oxigênio.
- C. Certo
- E. Errado
Carbonato de cálcio, na forma de rocha calcária, é freqüentemente utilizado como corretor de acidez do solo. A solubilidade da substância CaCO3 é baixa e, à temperatura de 25 ºC, uma solução saturada de carbonato de cálcio apresenta concentração em massa igual a 0,01 g/L. Considerando essas informações e também que M(CaCO3) = 100 g/mol, assinale a opção incorreta.
- A.
A concentração de uma solução saturada de carbonato de cálcio é igual a 1 × 10-4 mol/L.
- B.
A neutralização do solo é decorrente da reação apresentada a seguir.
CaCO3 (s) + 2 H+ (aq) → Ca2+ (aq) + H2O (l) + CO2 (g) - C.
Se, na atmosfera terrestre, ocorrer um aumento da concentração de óxidos de nitrogênio e de óxidos de enxofre, as águas das chuvas, ao caírem sobre um solo com calcário, acarretarão um aumento da rapidez da reação de neutralização do solo.
- D.
Considere-se que a adição de ácido clorídrico concentrado em uma amostra de 5 g de rocha calcária tenha provocado o desprendimento de 1,09 L de CO2 nas CNTP. Nesse caso, é correto concluir que a amostra apresentava 100% de pureza.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2007
A crescente preocupação mundial com o esgotamento das reservas petrolíferas tem gerado um grande número de pesquisas para a obtenção de energia a partir de outras fontes. Uma dessas alternativas, que está em desenvolvimento, é a utilização de hidrogênio gerado a partir da oxidação do metano, segundo a equação química a seguir.
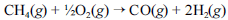
Na tabela a seguir, são fornecidas as entalpias de formação do metano e do monóxido de carbono.

A partir dessas informações, julgue os itens seguintes.
Considerando-se as massas atômicas fornecidas na tabela abaixo, é correto afirmar que, para produzir uma quantidade de massa de hidrogênio igual a m H, a partir da oxidação do metano descrita no texto, é necessário o consumo de uma massa de metano igual a 4 × m H .

- C. Certo
- E. Errado


