Questões sobre Reações, Soluções e Transformações Químicas
Lista completa de Questões sobre Reações, Soluções e Transformações Químicas para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
As partículas que devem ser removidas da água por tratamento iniciado pela coagulação são, em geral, negativamente carregadas e os coagulantes usados no tratamento de águas, normalmente, apresentam espécies positivamente carregadas. A eficiência do processo de coagulação depende, entre outros fatores, da natureza do cátion. Dessa forma, sulfatos de alumínio, cálcio ou sódio devem agir como coagulantes, porém com eficiência de coagulação diferenciadas.
Assinale a opção que expressa corretamente a tendência na eficiência de coagulação promovida pelos diferentes sais.
- A. Sulfato de sódio > sulfato de cálcio > sulfato de alumínio.
- B. Sulfato de sódio = sulfato de cálcio > sulfato de alumínio.
- C. Sulfato de sódio > sulfato de cálcio = sulfato de alumínio.
- D. Sulfato de sódio < sulfato de cálcio = sulfato de alumínio.
- E. Sulfato de sódio < sulfato de cálcio < sulfato de alumínio.
Uma mistura gasosa de 10 mmol de CO e 10 mmol de H2O é colocada em um reator de 500 mL e aquecida até 500 °C, atingindo o equilíbrio:
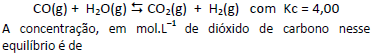
- A. 5,00 x 103.
- B. 1,33 x 102.
- C. 3,67 x 102.
- D. 4,00 x 102.
- E. 5,25 x 102.
A reação de cloro gasoso com uma base forte pode ser descrita pela equação

- A. 160 g.
- B. 60 g.
- C. 40 g.
- D. 10 g.
- E. 8 g.
Ao término de uma aula experimental, foi gerada uma solução aquosa com concentração de íons OH− igual a 1,010−2 mol.L−1. O técnico de laboratório providenciou a neutralização dessa solução e realizou o descarte adequado.
Com base nessa situação hipotética, assinale a alternativa que apresenta o pH dessa solução antes de ocorrer a neutralização.
- A. 12
- B. 10
- C. 7
- D. 4
- E. 2
3Para uma aula experimental em laboratório, será necessário preparar 500 mL de uma solução aquosa de carbonato de sódio 0,1 mol.L −1 (Na2CO3, com massa molar igual a 106 g.mol−1).
Considerando que, nessa situação hipotética, a pureza do Na2CO3 seja igual a 100%, assinale a alternativa que apresenta a massa de carbonato de sódio necessária para preparar essa solução.
- A. 2,12 g
- B. 5,30 g
- C. 10,6 g
- D. 21,2 g
- E. 50,0 g
Um técnico de laboratório preparou 100 mL de uma solução aquosa de hidróxido de sódio (com massa molar igual a 40 g.mol−1), utilizando 1,6 g de NaOH.
Considerando-se que, nesse caso hipotético, a pureza do hidróxido de sódio seja igual a 100%, a concentração dessa solução preparada, em mol por litro (mol.L−1), será igual a
- A. 0,016.
- B. 0,04.
- C. 0,4.
- D. 1,6.
- E. 2,5.
Uma solução tamponada resiste a uma mudança de pH quando pequenas quantidades de ácido ou base são adicionadas. Na bioquímica, soluções-tampão são muito importantes porque o funcionamento dos sistemas biológicos depende muito do pH. A propósito desse assunto, um tampão ácido é preparado utilizando-se uma solução aquosa que contenha
- A. NH3 e NH4 +.
- B. HCl e HNO3.
- C. HCl e NaOH.
- D. NaOH e NH3.
- E. CH3COOH e CH3CO2 −.
Química - Reações, Soluções e Transformações Químicas - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2016
Em laboratório, as soluções normalmente são preparadas dissolvendo-se uma massa determinada de soluto em uma certa quantidade de solvente. Ao se preparar uma solução aquosa, já são previamente conhecidas algumas características da solução, como, por exemplo, a massa do soluto e o volume final da solução. A massa de BaCl2, necessária para preparar 200 mL de solução de concentração 0,2 mol/L é igual a: (Considere: massas molares: Ba = 137 g/mol e Cl = 35,5 g/mol.)
- A. 4, 32 g.
- B. 6,72 g.
- C. 8, 28 g.
- D. 10,32 g.
Química - Reações, Soluções e Transformações Químicas - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2016
O hipoclorito de sódio (NaClO) é um potente desinfetante utilizado em laboratórios de análises clínicas. Foi constatado em 5,0 ml de um desinfetante à massa de 150 mg de hipoclorito de sódio. Qual é a concentração de hipoclorito de sódio nesta solução?
- A. 3,0 g/L.
- B. 4,0 g/L.
- C. 30 g/L.
- D. 40 g/L.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2015
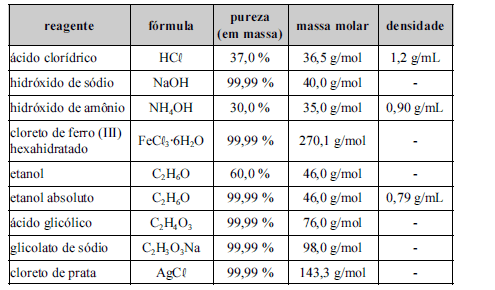
A tabela acima apresenta reagentes utilizados para o preparo de algumas soluções. Com base nessas informações, julgue os itens a seguir.
A mistura de 100 mL de etanol a 60,0 % com 100 mL de etanol absoluto produz uma solução final de concentração superior a 75,0 % em massa.- C. Certo
- E. Errado


