Questões sobre Reações, Soluções e Transformações Químicas
Lista completa de Questões sobre Reações, Soluções e Transformações Químicas para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
O cloreto de sódio é matéria-prima para a obtenção de cloro gasoso. A seqüência de equações não-balanceadas, a seguir, indicam as reações de obtenção desse gás a partir de salmoura (solução concentrada de NaC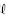 em água).
em água).
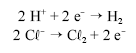
Com relação a esse processo, assinale a opção correta.
- A.
Nesse processo, o íon cloreto é oxidado.
- B.
Todas as espécies de cátions existentes no meio eletrolítico são reduzidas.
- C.
A eletrólise é capaz de gerar corrente elétrica a partir das reações químicas que se desenvolvem nesse processo.
- D.
A representação global do processo acima é a seguinte.

Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
Um experimento muito utilizado no ensino médio consiste na observação da reação de um comprimido efervescente com água em quatro diferentes situações, apresentadas a seguir.

O comprimido efervescente é composto de carbonato de sódio, bicarbonato de sódio, ácido cítrico e outras substâncias. Os resultados obtidos nesse experimento são os apresentados na tabela abaixo.

Considerando as informações acima, julgue os itens seguintes.
De modo geral, a diminuição da temperatura reduz a velocidade da reação.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
Um experimento muito utilizado no ensino médio consiste na observação da reação de um comprimido efervescente com água em quatro diferentes situações, apresentadas a seguir.

O comprimido efervescente é composto de carbonato de sódio, bicarbonato de sódio, ácido cítrico e outras substâncias. Os resultados obtidos nesse experimento são os apresentados na tabela abaixo.

Considerando as informações acima, julgue os itens seguintes.
O aumento da área de contato entre os reagentes aumentou a velocidade da reação.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
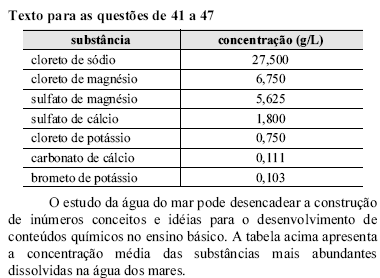
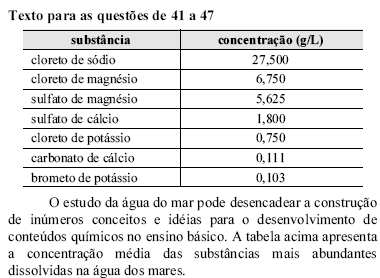
Considerando que o coeficiente de solubilidade do cloreto de sódio em água, a 20 ºC, é igual a 360 g/kg, é correto afirmar que a água do mar em relação a este sal é uma
- A.
solução saturada.
- B.
solução supersaturada.
- C.
solução insaturada.
- D.
mistura e, portanto, não pode ser considerada uma solução.
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
Um experimento muito utilizado no ensino médio consiste na observação da reação de um comprimido efervescente com água em quatro diferentes situações, apresentadas a seguir.

O comprimido efervescente é composto de carbonato de sódio, bicarbonato de sódio, ácido cítrico e outras substâncias. Os resultados obtidos nesse experimento são os apresentados na tabela abaixo.

Considerando as informações acima, julgue os itens seguintes.
O aumento da temperatura aumentou o tempo de reação.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A atmosfera da Terra no início de sua formação era muito diferente da atual e, provavelmente, passou por diversos estágios. Entre os gases geralmente postulados como presentes na atmosfera da Terra primitiva estão: amônia, gás sulfídrico, monóxido de carbono, dióxido de carbono, metano, hidrogênio e água na forma de vapor e líquida. Considerando esses gases e a interação de alguns deles com a água, julgue os itens a seguir.
Uma solução aquosa de H2S libera íons H3O+ e terá, como conseqüência, pH inferior a 7.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A atmosfera da Terra no início de sua formação era muito diferente da atual e, provavelmente, passou por diversos estágios. Entre os gases geralmente postulados como presentes na atmosfera da Terra primitiva estão: amônia, gás sulfídrico, monóxido de carbono, dióxido de carbono, metano, hidrogênio e água na forma de vapor e líquida. Considerando esses gases e a interação de alguns deles com a água, julgue os itens a seguir.
No sentido da reação direta em 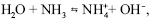 o NH3 é um doador de próton e a água, um receptor de próton; no sentido da reação inversa, o OH- é um doador de próton e o NH+4, um receptor de próton.
o NH3 é um doador de próton e a água, um receptor de próton; no sentido da reação inversa, o OH- é um doador de próton e o NH+4, um receptor de próton.
- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
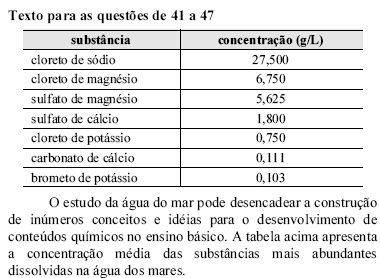
Com base na tabela, assinale a opção em que os cátions e ânions apresentados estão presentes na água do mar.
- A.

- B.

- C.

- D.

Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
Os primeiros bafômetros descartáveis consistiam em pequenos tubos contendo uma mistura sólida de sílica com solução aquosa de dicromato de potássio. A detecção da embriaguez por esse instrumento é visual, pois, da reação com o álcool, ocorre uma mudança de cor que pode ser interpretada pela equação a seguir.
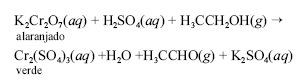
Considerando as informações acima, julgue os itens subseqüentes.
De acordo com a lei da conservação das massas, possíveis coeficientes da equação acima são 1:4:3:1:7:3:1.- C. Certo
- E. Errado
Química - Reações, Soluções e Transformações Químicas - Centro de Seleção e de Promoção de Eventos UnB (CESPE) - 2008
A teoria da ligação de valência (TLV) permite explicar como são associados os ligantes de um metal em um complexo, com base nos orbitais que participam dessas ligações coordenadas, além de fornecer o tipo de hibridação e a geometria do composto. Considerando que Z(H) = 1; Z(N) = 7; Z(F) = 9; Z(CR) = 17; Z(Co) = 27; Z(Ni) = 28; Z(Pt) = 78; assinale a opção que apresenta uma associação correta entre a fórmula do complexo, o tipo de hibridação.
- A.
[Co(NH3 )6 ]Cl3 — d2 sp3
- B.
[NiCR4 ]2- — sp3
- C.
[CoF6 ]3- — sp2 d
- D.
[PtCR4 ]2- — sp2 d


